原发梗阻性巨输尿管(primary obstructed megaureter, POM)是儿童常见先天性泌尿系畸形,也是小儿肾输尿管积水的重要病因之一[1]。气膀胱腹腔镜输尿管再植术可有效恢复肾功能、防止病情进展,是治疗进行性加重POM的根治性术式,在1岁以上患儿中应用广泛[2-3]。但1岁以下婴儿膀胱空间狭小,周围组织脆弱,如何选择适宜的气膀胱术式,在确保手术成功率的基础上,最大限度减少创伤、降低并发症发生率、促进远期功能恢复,是小儿外科临床面临的挑战。气膀胱Cohen输尿管再植术作为临床经典术式应用于婴儿时,常存在黏膜下隧道建立困难、术后解剖结构改变等问题。气膀胱改良乳头输尿管再植术作为新型术式,通过模拟输尿管斜行穿入膀胱、构建乳头状结构,操作相对简便,在抗反流的同时不改变输尿管走行,更符合生理状态。本研究旨在对比分析两种术式在婴儿POM患者中的综合疗效,为临床术式选择提供参考。
资料与方法 一、临床资料本研究为回顾性队列研究。以2015年1月至2024年10月山东大学附属齐鲁医院收治的婴儿POM患者为研究对象。病例纳入标准:①经排尿性膀胱尿道造影(voiding cystourethrography, VCUG)、泌尿系超声、肾核素显像、磁共振尿路造影等确诊为POM;②符合POM手术治疗指征,具体包括:保守治疗过程中出现临床症状(如发热性尿路感染、腰痛、结石等);胎儿泌尿外科协会(Society for Fetal Urology, SFU)分级为Ⅲ~Ⅳ级肾积水且持续不缓解或肾输尿管积水进行性加重;分肾功能受损(< 40%)或分肾功能进行性下降等;③手术方式为气膀胱改良乳头输尿管再植术或气膀胱Cohen输尿管再植术。排除标准:①合并其他泌尿系统畸形(如膀胱输尿管反流、重复肾集合系统、孤立肾、肾囊性病变、输尿管异位开口等);②术后失访或随访时间不足1年。本研究经山东大学附属齐鲁医院伦理委员会审核批准(KYLL — 2025 — 08 — 028)。患儿监护人均同意并签署知情同意书。
本研究共纳入56例POM患儿,根据手术方式不同分为改良乳头组和Cohen组。其中改良乳头组29例,男23例、女6例;平均手术年龄5.4个月(1.6~12个月);病变部位左侧17例、右侧9例、双侧3例;术前无明显临床症状21例,合并泌尿系感染8例;产前诊断23例,非产前诊断6例。Cohen组27例,男18例、女9例;平均手术年龄6.7个月(2~12个月);病变部位左侧15例、右侧9例、双侧3例;术前无明显临床症状16例,合并泌尿系感染10例、血尿1例;产前诊断19例,非产前诊断8例。
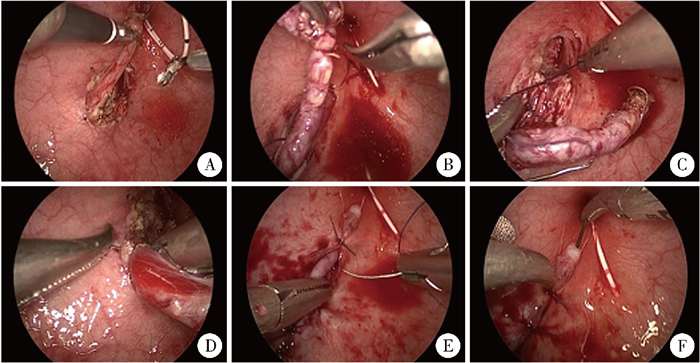
二、手术方法 (一) 气膀胱改良乳头输尿管再植术患儿仰卧,头低脚高,双下肢外展,经膀胱镜注入生理盐水使膀胱充盈至脐下,维持膀胱内压力6~10 mmHg(1 mmHg=0.133 kPa)。沿腹中线至膀胱顶下方1 cm处,用1 - 0带针线将膀胱顶悬吊于腹壁,紧贴悬吊线置入5 mm Trocar并捆绑固定。采用相同方式自下腹部左右两侧置入2个3 mm Trocar,并与5 mm Trocar约呈等腰三角形。退出膀胱镜并排空膀胱内液体,注入CO2并维持压力6~8 mmHg,建立气膀胱。膀胱内探查双侧输尿管开口,分别置入输尿管导管标记;于患侧输尿管末端缝合一针丝线并保留线尾。提起患侧输尿管,用电钩沿输尿管口切开膀胱黏膜,在输尿管浆膜层与膀胱肌层之间游离输尿管,彻底松解周围纤维组织,直至输尿管可无张力拖入膀胱,游离长度为3~5 cm,游离过程中注意保护输尿管血运。于输尿管移行段切除末端病变组织,根据输尿管扩张情况适当修剪输尿管末端,使其开口呈圆锥形;缝合并修补膀胱后壁浆肌层,恢复后壁完整性。于距输尿管末端开口3~5 cm处,用4 - 0可吸收线间断缝合输尿管浆肌层与膀胱肌层;距输尿管膀胱肌层吻合远端1.5 cm处,用5 - 0可吸收线间断缝合输尿管浆肌层与原输尿管开口处膀胱黏膜,将该段输尿管斜行包埋于膀胱壁内。保留末端输尿管1.5~2.0 cm,沿尿道内口方向将末端输尿管后壁浆肌层与膀胱黏膜缝合,固定于膀胱后壁。患侧输尿管口置入双J管,留置导尿管。手术过程见图 1。
|
图 1 气膀胱改良乳头式输尿管再植术的手术步骤 Fig.1 Surgical procedures of pneumovesical modified nipple ureteral reimplantation 注 A:切开膀胱黏膜,并于输尿管浆膜层与膀胱肌层之间游离输尿管;B:在输尿管移行段切除远端病变节段;C:缝合并修补膀胱后壁浆肌层;D:4-0可吸收线间断缝合输尿管浆肌层与膀胱肌层;E:用5-0可吸收间断缝线将膀胱黏膜缝合至输尿管浆肌层;F:置入适当型号的双J管 |
建立气膀胱及游离输尿管的方法同改良乳头组。针对松弛状态下直径>1.5 cm的显著扩张巨输尿管,行输尿管裁剪成形,将输尿管口直径缩小至6~8 mm。于对侧输尿管口上外方0.5~1.0 cm处切开膀胱黏膜,视情况用剪刀或血管钳潜行分离黏膜下层至患侧输尿管开口,建立足够长度的黏膜下隧道。将患侧输尿管经黏膜下隧道无张力拖至新开口处,并切除裁剪输尿管病变节段。采用5 - 0可吸收线间断吻合输尿管末端全层与新开口处膀胱壁,至少1针缝至肌层,缝合关闭患侧输尿管口膀胱切口。患侧输尿管口置入双J管,留置导尿管。
三、观察指标与随访比较两组患儿手术时间、术中出血量、术后血尿时间、术后住院时间、住院总费用、术后并发症发生率以及术后超声指标(输尿管直径、肾盂前后径以及肾皮质厚度)。患儿术后2~3个月拔除双J管,术后3、6、12个月及满1年后每6个月复查泌尿系超声(超声指标以术后12个月为评估节点)。术后3~6个月复查VCUG。术后并发症按Clavien-Dindo分级系统进行评估。
四、统计学处理采用R 4.5.1进行数据分析。服从正态分布的计量资料以x±s表示,组间比较采用两独立样本t检验;不服从正态分布的计量资料以M(Q1, Q3)表示,组间比较采用Mann-Witney检验。双侧输尿管再植术患儿术后超声指标按左右侧分别计入分析,采用线性混合效应模型(linear mixed-effects model, LMM)进行比较。计数资料以频数(%)表示,组间比较采用卡方检验,当T<1时采用Fisher精确概率法。P < 0.05为差异有统计学意义。
结果 一、基本情况两组年龄、性别、患病侧别、产前诊断、有无临床症状、术前输尿管直径、肾盂前后径、肾皮质厚度差异均无统计学意义(P>0.05)。见表 1。
| 表 1 Cohen组与改良乳头组原发梗阻性巨输尿管患儿基线资料比较 Table 1 Comparison of baseline characteristics between Cohen and Modified Nipple groups |
|
|
Cohen组中转开放手术2例,改良乳头组无一例中转手术。与Cohen组相比,改良乳头组手术时间、术后血尿时间及术后住院时间更短,差异均具有统计学意义(P<0.05)。而术中出血量、住院总费用方面差异无统计学意义(P>0.05)。两组随访时间13个月至9年。与Cohen组相比,改良乳头组术后输尿管直径更小,差异有统计学意义(P<0.05),肾盂前后径、肾皮质厚度差异无统计学意义(P>0.05)。改良乳头组2例、Cohen组3例在双J管留置期出现发热性尿路感染,经抗生素治疗后好转,拔管后未再复发。Cohen组术后3个月复查VCUG有1例Ⅰ°输尿管反流,无症状,随访1年后反流消退。术后6个月改良乳头组有1例Ⅱ°反流,无症状,随访10个月后复查VCUG,反流消失。两组围手术期及随访情况见表 2,典型病例影像见图 2。
| 表 2 Cohen组与改良乳头组原发梗阻性巨输尿管患儿围手术期及随访资料比较 Table 2 Perioperative and follow-up comparison between Cohen and Modified Nipple groups |
|
|
|
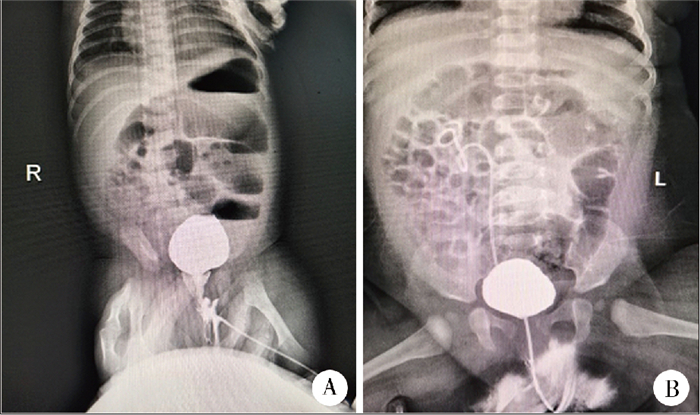
图 2 1例原发梗阻性巨输尿管患儿术前与术后排尿性膀胱尿道造影对比 Fig.2 Comparison of preoperative and postoperative voiding cystourethrography 注 A:术前造影见膀胱充盈良好,膀胱输尿管反流阴性;B:术后造影未见明确反流征象,提示术后无反流 |
婴儿POM膀胱容量小,膀胱壁薄,气膀胱操作难度较大,理论上多主张优先保守或替代性治疗[2, 4]。但对于已出现发热性尿路感染、肾输尿管积水进行性加重等情况的患儿,继续单纯保守治疗或仅行姑息性引流,可能会增加肾功能损伤、肾瘢痕形成及慢性肾脏病的风险[5-6]。输尿管再植术可以从病因上缓解临床症状,被视作POM治疗的金标准。有研究证实,婴儿期(甚至<3月龄)行输尿管再植术同样具有较高的成功率和较低的并发症发生率,且不会增加术后膀胱功能障碍风险[7]。气膀胱技术作为输尿管再植的一种微创途径,在婴幼儿群体中的适用性仍存在争议,有研究指出气膀胱手术受限于患儿膀胱容量,在婴儿群体中手术难度较大,可能会增加术后并发症和手术风险[8]。然而也有研究表明,气膀胱输尿管再植术在婴儿与>1岁患儿中的治疗效果和并发症发生率大致相当,在熟练掌握腹腔镜技术的前提下,在婴儿群体中同样能够获得满意的治疗效果[9]。这与本研究结果一致,因此笔者认为,在严格把握适应证和规范操作的前提下,由经验丰富的术者在婴儿群体中实施气膀胱输尿管再植术具有较好的安全性和有效性。
Cohen术式是目前临床报道最多、应用最广的输尿管再植术式[10]。作为经典的跨三角区手术,其核心在于构建长度为输尿管直径3~5倍的跨膀胱三角区黏膜下隧道,将输尿管包埋其中,从而形成独特的抗反流机制。但在婴儿中实施Cohen术存在明显局限性:①婴儿膀胱腔体狭小、壁薄且弹性差,难以构建3~5倍输尿管直径的黏膜下隧道长度,抗反流效果不稳定;②为构建跨三角区隧道,需较大范围行膀胱黏膜下剥离,可能对三角区神经肌肉结构的发育与功能造成影响;③Cohen输尿管再植术的黏膜下隧道开口于对侧输尿管口上方偏外侧,改变了正常的输尿管解剖位置,会增加后续逆行输尿管镜检查和操作的难度[11]。本研究Cohen组中2例2月龄患儿均因膀胱容量不足、操作受限而中转开放手术。对于低年龄婴儿,气膀胱下行Cohen手术路径较为复杂,需在有限空间内完成跨三角区长黏膜下隧道的建立,对术者的空间判断能力及显微缝合技术要求较高,一定程度上限制了气膀胱Cohen输尿管再植术在婴儿群体中的应用。
相比之下,气膀胱改良乳头输尿管再植术在婴幼儿中具有更佳的解剖适应性与操作可行性。与Cohen术相比,该术式保留了输尿管的自然走向,不跨越膀胱三角区,可避免因婴儿膀胱容量小、壁薄而导致操作困难及输尿管血供受损。其抗反流机制主要基于:①模拟输尿管自然斜行入膀胱的生理走行,增加输尿管在膀胱壁内的包埋长度,借助膀胱收缩与输尿管本身的蠕动形成动态压迫;②自移行段切除输尿管末端病变并塑形为圆锥状开口,可与三角区肌肉支撑形成“垂直喷嘴”效应,优化尿流动力学状态[12];③将游离后的输尿管后壁固定于膀胱壁,使其在排尿期膀胱内压升高时被动贴附于膀胱壁,形成类似“瓣膜压迫”的动态闭合效应;④术后膀胱黏膜覆盖输尿管,形成乳头状结构。上述结构协同作用,即使在膀胱容量较小的小月龄婴儿中,也能建立稳定且符合生理特性的抗反流屏障[13]。
本研究显示改良乳头组患儿手术时间、术后血尿持续时间及术后住院时间均显著短于Cohen组,这一差异可能与两种术式在婴儿群体中的技术特点及操作复杂程度密切相关。气膀胱改良乳头输尿管再植术通过原位构建抗反流结构,避免了气膀胱Cohen输尿管再植术中建立3 ∶ 1~5 ∶ 1长径比黏膜下隧道的复杂步骤,简化了手术过程,有效缩短了手术时间。同时,该术式显著减小了婴儿膀胱肌层的剥离范围,减少了对膀胱三角区的解剖干扰,减轻了术中组织损伤,避免了因输尿管过度牵拉和旋转所致的吻合口张力增加。上述技术优势共同促进患儿术后早期恢复,减轻了术后血尿程度并缩短血尿持续时间,而较小的手术创伤和较低的吻合口张力则为组织愈合创造了更有利的条件,最终术后住院时间显著缩短。本研究两组患儿输尿管直径均较术前显著缩小,且改良乳头组输尿管恢复优于Cohen组,提示气膀胱改良乳头输尿管再植术在远期输尿管形态恢复方面更具优势。其可能机制为:乳头状结构在膀胱充盈与排空过程中可发挥一定的动态压力调节作用,通过维持输尿管末端的张闭协调与压力梯度稳定,一定程度上促进了输尿管形态学恢复。
值得注意的是,由于婴儿膀胱容量较小、操作空间受限,Cohen组中部分病例未能达到推荐的黏膜下隧道比例,但该组患儿术后仍取得了良好的恢复效果。其可能原因包括:婴儿膀胱组织弹性较好、膀胱内压相对较低,且术中输尿管走行平顺、黏膜下固定稳固,使得即便隧道比例相对缩短,仍可建立有效的抗反流机制。韩文文等[14]研究发现,当输尿管黏膜下埋植长度与输尿管直径比≥2.5时,可获得较好的抗反流效果。这提示在婴幼儿膀胱容量受限的情况下,适当缩短隧道长度并不一定增加术后并发症风险,与本研究结果相符。综合来看,黏膜下隧道比例虽为建立抗反流机制的重要解剖学依据,但在婴儿Cohen术中,隧道的“功能性构建”可能比单纯追求固定比例更具临床意义。相较而言,气膀胱改良乳头输尿管再植术通过在原位构建乳头状抗反流结构,避免了长隧道形成的限制,更契合婴儿膀胱的解剖特征。
本研究为单中心回顾性分析,病例数较少,随访时间有限,可能存在选择偏倚和信息偏倚,对结果的代表性和统计效力造成一定影响。未来仍需开展多中心、大样本、前瞻性随机对照研究,结合术前影像学、术后尿动力学评估及长期肾功能随访等多维度指标,进一步验证本研究结果,优化婴儿POM的个体化术式选择策略。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 朱国栋、刘行健负责文献检索,李爱武、朱国栋负责论文调查设计, 朱国栋、刘行健负责数据收集与分析,朱国栋负责论文结果撰写为,李爱武、朱国栋、刘行健负责论文讨论分析,并对文章知识性内容进行审阅
| [1] |
陈鹏宇, 李守林. 儿童原发性巨输尿管症的诊疗现状[J]. 中华小儿外科杂志, 2023, 44(2): 182-188. Chen PY, Li SL. Current status of diagnosing and managing primary megaureter in children[J]. Chin J Pediatr Surg, 2023, 44(2): 182-188. DOI:10.3760/cma.j.cn421158-20211109-00546 |
| [2] |
Boswell TC. Advancements in surgical management of megaureters[J]. Curr Urol Rep, 2024, 25(9): 215-223. DOI:10.1007/s11934-024-01214-8 |
| [3] |
国家卫生健康委员会小儿内镜外科专家委员会, 中华医学会小儿外科学分会泌尿学组, 中国医师协会小儿外科医师分会, 等. 儿童腹腔镜气膀胱输尿管再植术操作指南(2024版)[J]. 临床小儿外科杂志, 2024, 23(11): 1001-1008. Expert Committee of Pediatric Endoscopy, National Health Commission, Group of Urology, Branch of Pediatric Surgery, Chinese Medical Association, Branch of Pediatric Surgery, Chinese Medical Doctor Association. Operative Guideline of Laparoscopic Pneumovesical Ureteric Reimplantation in Children (Edition 2024)[J]. J Clin Ped Sur, 2024, 23(11): 1001-1008. DOI:10.3760/cma.j.cn101785-202410048-001 |
| [4] |
Farrugia MK, Hitchcock R, Radford A, et al. British Association of Paediatric Urologists consensus statement on the management of the primary obstructive megaureter[J]. J Pediatr Urol, 2014, 10(1): 26-33. DOI:10.1016/j.jpurol.2013.09.018 |
| [5] |
Gökceoǧlu AU, Taş N. Renal scarring in children with febrile urinary tract infection[J]. J Pediatr (Rio J), 2025, 101(3): 370-374. DOI:10.1016/j.jped.2024.10.011 |
| [6] |
中华医学会小儿外科学分会小儿泌尿外科学组. 儿童原发性梗阻性巨输尿管症诊疗专家共识[J]. 中华小儿外科杂志, 2022, 43(8): 679-684. Group of Urology, Society of Pediatric Surgery, Chinese Medical Association. Expert Consensus on Diagnosing and Treating Primary Obstructed Megaureters in Children[J]. Chin J Pediatr Surg, 2022, 43(8): 679-684. DOI:10.3760/cma.j.cn421158-20220402-00233 |
| [7] |
Jude E, Deshpande A, Barker A, et al. Intravesical ureteric reimplantation for primary obstructed megaureter in infants under 1 year of age[J]. J Pediatr Urol, 2017, 13(1): 47.e1-47.e7. DOI:10.1016/j.jpurol.2016.09.009 |
| [8] |
Cui X, Huang WH, Wang YJ, et al. Effect of pneumovesicoscopic cohen surgery with adjustable suspension technique through the urethra on the treatment of primary vesicoureteral reflux disease in infants[J]. BMC Surg, 2023, 23(1): 105. DOI:10.1186/s12893-023-01996-7 |
| [9] |
刘颖, 毕允力. 气膀胱输尿管再植术治疗婴儿输尿管膀胱连接部梗阻临床分析[J]. 临床小儿外科杂志, 2014, 13(4): 287-290. Liu Y, Bi YL. Clinical analysis of pneumovesicoscopy ureteral reimplantation in treating infantile vesicoureteral junction obstruction[J]. J Clin Ped Sur, 2014, 13(4): 287-290. DOI:10.3969/j.issn.1671-6353.2014.04.007 |
| [10] |
Mattioli G, Lena F, Fiorenza V, et al. Robotic ureteral reimplantation and uretero-ureterostomy treating the ureterovesical junction pathologies in children: technical considerations and preliminary results[J]. J Robot Surg, 2023, 17(2): 659-667. DOI:10.1007/s11701-022-01478-7 |
| [11] |
Brown CT, Jayanthi VR. Percutaneous vesicoscopic approach for retrograde ureteroscopy following Cohen cross-trigonal ureteral reimplantation[J]. Urology, 2018, 111: 186-188. DOI:10.1016/j.urology.2017.09.028 |
| [12] |
Lyon RP, Marshall S, Tanagho EA. The ureteral orifice: its configuration and competency[J]. J Urol, 1969, 102(4): 504-509. DOI:10.1016/s0022-5347(17)62184-0 |
| [13] |
李爱武, 崔新海, 王健, 等. 腹腔镜气膀胱改良乳头式输尿管膀胱再植术的临床研究[J]. 中华小儿外科杂志, 2020, 41(2): 112-117. Li AW, Cui XH, Wang J, et al. Clinical trials of pneumovesicoscopic modified orthotopic nipple ureteral reimplantation[J]. Chin J Pediatr Surg, 2020, 41(2): 112-117. DOI:10.3760/cma.j.issn.0253-3006.2020.02.004 |
| [14] |
韩文文, 张潍平, 孙宁, 等. Cohen再植术后反流影响因素的研究[J]. 中华小儿外科杂志, 2016, 37(11): 846-850. Han WW, Zhang WP, Sun N, et al. Retrospective analysis of influencing factors of postoperative reflux after Cohen's reimplantation[J]. Chin J Pediatr Surg, 2016, 37(11): 846-850. DOI:10.3760/cma.j.issn.0253-3006.2016.11.010 |
 2026, Vol. 25
2026, Vol. 25


