2. 中南大学湘雅医学院附属儿童医院 湖南省儿童医院康复中心, 长沙 410007;
3. 邵阳县人民医院神经外科, 邵阳 422100
2. Rehabilitation Center, Affiliated Children's Hospital, Xiangya School of Medicine, Central South University (Hunan Children's Hospital), Changsha 410007, China;
3. Department of Neurosurgery, Shaoyang County People's Hospital, Shaoyang 422100, China
脑积水是儿童常见中枢神经系统疾病,其新生儿患病率在高收入国家为1/1 000~2/1 000,低收入国家则更高[1]。全球每年新增小儿脑积水病例超40万,80%以上集中在发展中国家[2]。该疾病可由先天性发育异常、肿瘤、出血、感染、外伤等多种病因引发,各月龄阶段均可能发病,尤其多见于婴幼儿群体。临床上,准确评估脑室扩大程度是脑积水诊断、治疗决策及预后判断的关键。传统评估指标Evans指数(Evans index, EI)仅通过测量双侧脑室额角最宽处与颅内径的比值反映额角宽度,存在评估维度单一的局限。额角- 枕角比(frontooccipital horn ratio, FOHR)是近年来应用于儿童脑积水诊治的新型简便指标,其测量方式为:在轴位经双侧室间孔(Monro孔)平面,测量双侧脑室额角与枕角内侧壁间距之和,再除以同层面最大颅内横径即双顶径(biparietal diameter, BPD)的2倍[3]。已有研究证实,FOHR与实际脑室体积高度相关,且观察者间一致性良好(组内相关系数intraclass correlation coefficient, ICC>0.9),评估效果优于主观分级[3]。目前FOHR已在多种影像模态中广泛应用于儿童脑积水的影像学评估[4]。尽管FOHR应用前景良好,但当前关于该指标与儿童月龄的关联,以及不同病因、不同解剖生理类型患儿基线FOHR分布的全龄段、分层研究仍较为匮乏。基于此,本研究系统评估FOHR的月龄依赖性及分层特征,并与EI进行并行对照,旨在为儿童脑积水的临床量化评估与治疗决策提供更全面的依据。
资料与方法 一、研究对象本研究为回顾性队列研究。收集中南大学湘雅医学院附属儿童医院(湖南省儿童医院)神经外科2017年8月至2025年8月收治的223例脑积水患儿临床资料,其中男136例、女87例;月龄6.0(3.0,19.5)个月。病例纳入标准:①首次手术治疗前完成颅脑影像学检查,并行FOHR与EI测量;②月龄≤18岁;③经临床症状与影像学检查综合评估确诊为脑积水,或影像学检查提示存在侧脑室扩张。排除标准:①影像资料缺失无法测量FOHR;②月龄信息缺失;③明确为脑萎缩/代偿性脑室扩大,且临床未诊断脑积水;④明显颅骨重塑或严重颅骨畸形,无法测量BPD。收集患儿月龄(早产儿以矫正月龄为准)、性别、胎龄、病因、解剖生理类型、术前是否行脑脊液临时引流等资料。本研究通过中南大学湘雅医学院附属儿童医院(湖南省儿童医院)伦理委员会审核批准(HCHLL — 2025 — 369),并因回顾性研究豁免患儿及家属知情同意。
二、分组方式按照不同病因将患儿分为3组:①出血相关组:由颅内出血引起的脑积水(如早产儿脑室内出血后脑积水等);②结构性梗阻组:由解剖结构异常导致脑脊液循环受阻的脑积水,包括先天性发育畸形(如中脑导水管狭窄、Dandy-Walker综合征等)、脑肿瘤及囊肿引起的阻塞性脑积水;③获得性损伤/炎症组:由后天损伤或炎症导致的脑积水,如外伤后脑积水、感染后脑积水。根据脑积水的不同解剖生理类型分为:①非交通性脑积水:脑室系统某处阻塞导致的脑脊液积聚;②交通性脑积水:脑脊液吸收障碍或过度分泌导致脑室系统积液,脑室与蛛网膜下腔交通通畅;③混合型脑积水:兼有梗阻及交通性因素的脑积水。本研究在统计分析中将非交通性与混合型合并为一组,与交通性构成二分类,病因分组和解剖生理类型分组相互独立交叉,每例患儿可分别归类于上述病因组和解剖生理类型组。
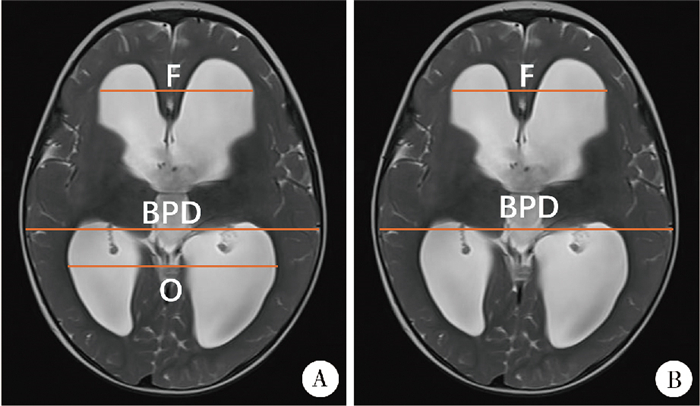
三、主要变量及观察指标① 月龄:指患儿入院时实际月龄(早产儿以矫正月龄为准)。本研究预先将月龄划分为0~6个月(不含6个月)、6~12个月(不含12个月)、12~24个月(不含24个月)、24~60个月(不含60个月)、≥60个月5个阶段,用以刻画影像线性指标(FOHR、EI)在不同发育阶段的分布与一致性[5-9]。②FOHR:入院时FOHR测量值(未手术干预时),在轴位室间孔水平测量双侧额角最大内径(F)和双侧后角(三角部/枕角)侧壁间最大内径(O),再测量该层面双顶径的距离(BPD),计算$\mathrm{FOHR}=\frac{\mathrm{F}+\mathrm{O}}{2 \times \mathrm{BPD}}$(图 1A)。③EI:入院时Evans指数测量值(未手术干预时),在轴位室间孔水平测量双侧额角最大内径(F),测量该层面双顶径的距离(BPD),计算$\mathrm{EI}= \frac{\mathrm{F}}{\mathrm{BPD}}$(图 1B)。④病因分组:出血相关组63例(28.3%)、结构性梗阻组113例(50.7%)、获得性损伤/炎症组47例(21.1%)。⑤解剖生理类型分组:交通性114例(51.1%)、非交通性88例(39.5%)、混合型21例(9.4%)(为便于统计比较,表中合并呈现为“非交通性/混合”)。⑥术前临时引流:记录患儿在最终手术(分流或脑室镜等)前是否接受过脑脊液临时引流措施(如外引流等)。该因素可能影响基线影像时脑室大小,用于敏感性分析。⑦FOHR与EI比较时的月龄分层:参考儿童颅骨生长、囟门发育以及在脑积水治疗中已被验证的月龄分层。其生物学合理性包括:前囟多在12~18个月闭合,总体脑体积2岁时达成人的80% ~90%,5~6岁接近成人水平(约95%),提示12个月、24个月、60个月为具有可解释性的发育切点[5-9]。
|
图 1 额角- 枕角比与Evans index测量的示意图 Fig.1 Schematic Diagram of FOHR and EI Measurements 注 A:FOHR测量的方式; B:EI测量的方式; F:双侧额角最大内径; O:双侧后角(三角部/枕角)侧壁间最大内径; BPD:双顶径的距离 |
使用SPSS 26.0进行统计分析。连续变量经Shapiro-Wilk正态性检验均不服从正态分布,故以M(Q1,Q3) 描述;分类变量以频数、构成比表示。采用Spearman秩相关分别评估月龄与FOHR、EI的相关性,并计算FOHR与EI的相关性;为获得区间估计,使用Bootstrap(300次)计算95%CI。采用Kruskal-Wallis秩和检验比较病因分组与解剖生理类型分组之间FOHR、EI的分布差异;采用卡方检验比较FOHR严重度分层[<0.50(不含0.50)、0.50~0.60(不含0.60)、≥0.60]的构成比。分别比较各分层内FOHR、EI的分布差异(Kruskal-Wallis秩和检验),并行两两Mann-Whitney U检验(Holm法校正多重比较);各层内拟合EI=a×FOHR+b并报告a、b、R2。通过比较含交互项与不含交互项的线性模型,F检验评估斜率是否随月龄层改变。为检验主要结论的稳健性,设置两类敏感性分析:①剔除术前行脑脊液临时引流者后,按上述流程重复相关分析、组间比较与分层线性拟合;②采用ETVSS月龄层替代主分析分层,重复分层比较、线性拟合与交互项检验,以验证不同月龄分层体系下结论的一致性。P<0.05为差异具有统计学意义。
结果 一、FOHR与年龄的相关性Spearman秩相关显示,月龄与FOHR呈显著负相关(ρ=-0.337,P<0.001;Bootstrap〔B=300〕95%CI:-0.462~-0.203),提示月龄越大,基线脑室扩大量级相对越轻。以log(月龄)替代后,相关方向与强度基本一致(ρ=-0.337,P<0.001;Bootstrap 95%CI:-0.462~-0.203),表明不同月龄转换方式对相关性结论无明显影响。见表 1。
| 表 1 脑积水患儿FOHR与月龄的相关性分析 Table 1 Correlation analysis of FOHR and age |
|
|
出血相关组FOHR 0.572(0.515, 0.614)、结构性梗阻组FOHR 0.559(0.492, 0.617)、获得性损伤/炎症组FOHR 0.546(0.489, 0.599), 3组FOHR分布差异无统计学意义(P=0.529);交通性组FOHR 0.568(0.504, 0.611)、非交通性组/混合型组FOHR 0.550(0.492, 0.618), 差异亦无统计学意义(P=0.530)。
三、FOHR与EI的对照分析FOHR与EI整体呈显著正相关(表 1),按预设月龄层分别拟合线性模型EI=a×FOHR+b(表 2)。含交互项与不含交互项模型的F检验结果显示,FOHR对EI的影响斜率是否随月龄层改变的总体检验P=0.053,但存在边缘差异趋势,提示发育阶段可能对FOHR与EI的映射强度存在轻度调制。
| 表 2 223例脑积水患儿EI与FOHR的月龄分层线性拟合 Table 2 Age-stratified linear fits for EI and FOHR |
|
|
按预设阈值分层,FOHR<0.50、0.50~0.60、≥ 0.60分别占28.3%、40.4%、31.4%。出血相关组中重度(FOHR≥0.60)比例为34.9%,略高于结构性梗阻组(32.7%)与获得性损伤/炎症组(23.4%);非交通性/混合组FOHR<0.50的比例(35.2%)高于交通性组(23.7%)。不同病因分组(χ2=2.154,P=0.373)与不同解剖生理类型分组(χ2=2.786,P=0.251)下,FOHR严重度构成比差异均无统计学意义。
五、敏感性分析月龄与FOHR的负相关方向与显著性保持一致(ρ=-0.289,P<0.001),FOHR与EI的相关性仍维持较高水平(ρ=0.774,P<0.001)。层内EI于不同FOHR严重度的差异在前3个月龄层均有统计学意义(P<0.001),≥10岁层因样本量较小(n=12,P=0.103), 提示研究结果具有良好稳健性。
讨论FOHR与患儿月龄呈中等负相关(ρ=-0.337,P<0.001),这一结果揭示了儿童脑积水脑室扩张的关键发育相关性特征,月龄越小,基线FOHR值越高,脑室扩张程度相对更显著。这一现象的核心机制与不同月龄儿童的颅脑结构发育特点直接相关:婴幼儿(尤其是1岁以内)前囟未闭、颅缝松动,颅骨可塑性强,脑脊液积聚时头围可代偿性增大,脑室能在较低颅内压下明显扩张,因此就诊时多表现为头颅增大、囟门饱满,而颅内压增高症状较隐匿。年长儿童(≥2岁)颅缝已闭合,颅腔容积固定,脑脊液积聚后脑室扩张空间受限,可更早出现头痛、呕吐、视乳头水肿等颅内高压症状,往往在脑室未达到重度扩张时即接受干预,导致基线FOHR值相对较低。需强调的是,月龄与FOHR的负相关并非提示年长患儿病情更轻。随着神经系统发育成熟,大脑对脑积水的耐受性下降,即使中度脑室扩张(FOHR 0.50~0.60)也可能造成明显神经功能损害,临床需结合症状而非单纯的FOHR值判断病情严重程度[10]。
本研究显示,不同病因(出血相关/结构性梗阻/获得性损伤/炎症)及解剖生理类型(交通性/非交通性/混合型)患儿的FOHR分布差异无统计学意义(P>0.05),但存在值得关注的临床趋势:出血相关组(多为早产儿脑室出血后脑积水)的重度FOHR占比(34.9%)略高于其他组,因围产期脑室出血后的脑积水进展迅速,部分低收入地区患儿未及时干预,可出现极度脑室扩张(FOHR>0.6甚至0.7以上)。结构性梗阻组(如脑肿瘤、中脑导水管狭窄)的FOHR中位数(0.56)相对较低,因患儿常因明显颅内高压症状在脑室中度扩张时即接受手术治疗,避免了重度扩张的发生。获得性损伤/炎症组的重度FOHR比例最低(23.4%),感染后脑积水患儿常伴随脑膜脑实质粘连,部分病例虽脑室仅轻中度扩张,但颅内高压症状已较明显,无需进展至重度即启动治疗。上述结果提示:所有类型的儿童脑积水均有1/4~1/3可能进展为重度脑室扩张(FOHR≥0.60),临床需摒弃“特定病因类型风险更低”的固有认知,对所有患儿需密切监测脑室大小变化,及时干预[11-12]。
EI是传统脑室扩张评估指标,仅反映额角宽度,而FOHR通过整合额角与枕角间距,能更全面反映脑室整体扩张程度。本研究证实,FOHR与EI呈高度正相关(ρ=0.762,P<0.001),且在不同月龄分层中均保持良好一致性。0~6个月、6~12个月、12~24个月、24~60个月、≥60个月各分层中,EI与FOHR的线性拟合R2均在0.35以上,提示两者量化一致性稳定。月龄分层对两者的映射关系存在轻度调制趋势(P=0.053),婴幼儿期(0~24个月)拟合斜率更高,说明该阶段FOHR对脑室体积变化的敏感性可能更强。这一结果支持临床采用“FOHR+EI双指标并行评估”策略:FOHR适用于全龄段儿童脑积水随访,EI可作为补充互证,尤其在颅骨畸形、测量条件受限等场景下,两者结合能提升评估准确性[13-14]。
本研究为单中心回顾性设计,导致样本病因构成和诊治策略存在区域特异性,结果普适性需多中心大样本研究验证。未纳入健康儿童的月龄匹配参照数据,也未报告测量者间一致性,可能影响指标的外部推广与测量精度。影像学数据来源于临床常规检查,不同患儿的扫描条件存在差异,虽已测量流程标准化,但仍可能存在轻微测量误差。仅分析基线横断面数据,缺乏术后FOHR变化与临床结局(如神经功能恢复、并发症)的关联分析,无法明确FOHR对预后的预测价值。未量化后颅窝缩窄、蛛网膜粘连程度等解剖学差异,这些因素可能影响脑脊液动力学及脑室扩张规律,需在后续研究中纳入[15-16]。尽管存在上述局限,本研究敏感性分析显示核心结论保持稳定,证实研究结果具有一定稳健性。
综上所述,FOHR具有显著月龄依赖性,与EI量化一致性高,适用于儿童脑积水全龄段随访;临床解读需结合月龄与症状,以EI互证,不同病因/类型均需警惕重度脑室扩张风险。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 张津维负责文献检索;张津维负责论文调查设计,张津维、袁丽平、阳治国负责数据收集与统计学分析;张津维负责论文结果撰写;张津维、袁丽平、吴水华负责论文讨论分析;张津维、吴水华负责对文章知识性内容进行审阅
| [1] |
Haizel-Cobbina J, Coompson C, Addy S, et al. Pediatric hydrocephalus management at a major neurosurgical referral center in Kumasi, Ghana[J]. Childs Nerv Syst, 2025, 41(1): 299. DOI:10.1007/s00381-025-06960-9 |
| [2] |
Dai YW, Zhong ZS, Qin Y, et al. AI model integrating imaging and clinical data for predicting CSF diversion in neonatal hydrocephalus: a preliminary study[J]. Hum Brain Mapp, 2025, 46(14): e70363. DOI:10.1002/hbm.70363 |
| [3] |
Kulkarni AV, Drake JM, Armstrong DC, et al. Measurement of ventricular size: reliability of the frontal and occipital horn ratio compared to subjective assessment[J]. Pediatr Neurosurg, 1999, 31(2): 65-70. DOI:10.1159/000028836 |
| [4] |
Sabeti M, Alikhani S, Shakoor MH, et al. Automatic determination of ventricular indices in hydrocephalic pediatric brain CT scan[J]. Interdiscip Neurosurg, 2023, 31: 101675. DOI:10.1016/j.inat.2022.101675 |
| [5] |
Radhakrishnan R, Brown BP, Kralik SF, et al. Frontal occipital and frontal temporal horn ratios: comparison and validation of head ultrasound-derived indexes with MRI and ventricular volumes in infantile ventriculomegaly[J]. AJR Am J Roentgenol, 2019, 213(4): 925-931. DOI:10.2214/AJR.19.21261 |
| [6] |
SarıE, Sarı S, Akgün V, et al. Measures of ventricles and Evans' index: from neonate to adolescent[J]. Pediatr Neurosurg, 2015, 50(1): 12-17. DOI:10.1159/000370033 |
| [7] |
Gilmore JH, Knickmeyer RC, Gao W. Imaging structural and functional brain development in early childhood[J]. Nat Rev Neurosci, 2018, 19(3): 123-137. DOI:10.1038/nrn.2018.1 |
| [8] |
Kulkarni AV, Drake JM, Kestle JRW, et al. Predicting who will benefit from endoscopic third ventriculostomy compared with shunt insertion in childhood hydrocephalus using the ETV Success Score[J]. J Neurosurg Pediatr, 2010, 6(4): 310-315. DOI:10.3171/2010.8.PEDS103 |
| [9] |
Durnford AJ, Kirkham FJ, Mathad N, et al. Endoscopic third ventriculostomy in the treatment of childhood hydrocephalus: validation of a success score that predicts long-term outcome[J]. J Neurosurg Pediatr, 2011, 8(5): 489-493. DOI:10.3171/2011.8.PEDS1166 |
| [10] |
Hodler J, Kubik-Huch RA, von Schulthess GK. Diseases of the brain, head and neck, spine 2020-2023: diagnostic imaging[M]. Cham: Springer, 2020. DOI:10.1007/978-3-030-38490-6
|
| [11] |
Reynolds RA, Ahluwalia R, Krishnan V, et al. Risk factors for unchanged ventricles during pediatric shunt malfunction[J]. J Neurosurg Pediatr, 2021, 28(6): 703-709. DOI:10.3171/2021.6.PEDS2125 |
| [12] |
Raybaud C, Krishnan P. Hydrocephalus in children: a neuroradiological perspective[J]. Neurol India, 2021, 69(Supplement): S283-S291. DOI:10.4103/0028-3886.332282 |
| [13] |
Riva-Cambrin J, Kulkarni AV, Burr R, et al. Impact of ventricle size on neuropsychological outcomes in treated pediatric hydrocephalus: an HCRN prospective cohort study[J]. J Neurosurg Pediatr, 2021, 29(3): 245-256. DOI:10.3171/2021.8.PEDS21146 |
| [14] |
Otun A, Morales DM, Garcia-Bonilla M, et al. Biochemical profile of human infant cerebrospinal fluid in intraventricular hemorrhage and post-hemorrhagic hydrocephalus of prematurity[J]. Fluids Barriers CNS, 2021, 18(1): 62. DOI:10.1186/s12987-021-00295-8 |
| [15] |
刘祎, 秦齐, 张佳, 等. 婴幼儿脑室出血后脑积水的危险因素分析[J]. 临床小儿外科杂志, 2024, 23(3): 242-246. Liu Y, Qin Q, Zhang J, et al. Analysis of risk factors of hydrocephalus after intraventricular hemorrhage in infants[J]. J Clin Ped Sur, 2024, 23(3): 242-246. DOI:10.3760/cma.j.cn101785-202208008-008 |
| [16] |
Paturu M, Triplett RL, Thukral S, et al. Does ventricle size contribute to cognitive outcomes in posthemorrhagic hydrocephalus? Role of early definitive intervention[J]. J Neurosurg Pediatr, 2022, 29(1): 10-20. DOI:10.3171/2021.4.PEDS212 |
 2026, Vol. 25
2026, Vol. 25


