肾母细胞瘤(Wilms tumor, WT)是儿童最常见的肾脏恶性肿瘤,起源于未成熟肾脏残留组织,占全球儿童实体肿瘤的6% ~7%,95%以上的患儿年龄≤10岁[1-3]。目前,联合化疗+手术的标准化治疗使WT总体治愈率接近90%,国际儿科肿瘤学会(the International Society of Pediatric Oncology,SIOP)-2001方案术前化疗患儿的两年无事件生存率和总生存率分别达87%和93%,儿童肿瘤协作组(Children's Oncology Group, COG)研究也得出相似结果[4-5]。但间变病理类型及复发患者的预后仍较差,因此探究WT发生发展的分子机制,对阐明致病机理、提高诊治效率及改善预后具有重要意义。过氧化物酶体增殖物激活受体α(peroxisome proliferator-activated receptor alpha, PPARα)属于类固醇/甲状腺核激素受体超家族,是配体激活的转录因子,其家族成员包括PPARα、PPARβ/δ及PPARγ[6]。PPARα可调控脂肪酸摄取、氧化及运输相关基因表达,参与脂蛋白代谢调节,同时在肿瘤发生发展中发挥重要作用,羟酰辅酶A脱氢酶三功能多酶复合物亚基α(hydroxyacyl-CoA dehydrogenase trifunctional multienzyme complex subunit α, HADHA)是线粒体脂肪酸β氧化途径的关键限速酶,可通过介导脂质代谢重编程调节肝癌、淋巴瘤等恶性肿瘤的生物学行为[7-8]。已有研究表明,HADHA在WT中呈低表达[9]。但PPARα与HADHA在WT中的相互作用及调控机制尚未明确。基于上述背景,本研究以WT细胞系及临床样本为研究对象,通过生物信息学分析、细胞实验及动物实验,探讨PPARα和HADHA在WT中的表达规律,明确PPARα对WT肿瘤细胞生物学行为的影响,并验证其是否通过调控HADHA及脂质代谢发挥作用,为WT的分子靶向治疗提供实验依据。
资料与方法 一、实验材料 (一) 标本及细胞系来源肾母细胞瘤组织及瘤旁对照组织均来自湖南省儿童医院泌尿外科手术标本,患儿未接受手术、放疗或化疗,排除其他部位恶性肿瘤,标本经病理科确诊。肾母细胞瘤细胞系WiT49(上海青旗生物技术发展有限公司)、HFWT(RIKEN生物资源中心)及HEK293T细胞(武汉普诺赛生物技术有限公司)用于体外实验。本研究经湖南省儿童医院伦理委员会批准(HCHLL — 2022 — 83),患儿家属签署知情同意书。
(二) 主要试剂与耗材DMEM培养液、胎牛血清、胰蛋白酶(武汉普诺赛生物技术有限公司);Trizol试剂、逆转录试剂盒、RT-PCR试剂盒(长沙艾科瑞生物科技有限公司);细胞裂解液、细胞周期试剂盒、细胞凋亡试剂盒、Transwell试剂盒、TUNEL试剂盒、Lipofectamine 2000(北京索莱宝科技有限公司);PPARα抗体、HADHA抗体、β-actin抗体、ACAT1抗体、ACLY抗体、FASN抗体、羊抗兔二抗、羊抗鼠二抗(武汉三鹰生物技术有限公司);PPARα过表达载体及HADHA干扰RNA(苏州吉玛生物技术有限公司);CCK-8试剂盒(北京阿匹斯生物技术有限公司);双荧光素酶报告试剂盒(Promega公司);油红O染色试剂盒(湖北百奥斯生物科技有限公司)。
二、实验方法 (一) 生物信息学筛选基因从GEO数据库下载WT测序数据集GSE138869(基于GPL11154平台,Illumina HiSeq 2000),包含5例WT组织及5例正常对照组织。使用R语言处理芯片原始数据,通过GEO2R在线工具筛选差异基因,筛选条件为调整P值(adj.P) < 0.05且|log 2FC|>1。利用DAVID数据库进行基因本体论分析及KEGG通路富集分析,通过STRING数据库预测蛋白质-蛋白质相互作用。
(二) 细胞培养所有细胞采用含10%胎牛血清、100 U/mL青霉素及0.1 mg/mL链霉素的DMEM培养液,置于37℃、5%CO2培养箱中常规培养。
(三) 质粒及干扰RNA转染将对数生长期细胞接种于6孔板,按照LipofectaminTM操作手册进行转染,每孔转染4 μg质粒或100 nmol小干扰RNA(small interfering RNA, siRNA),转染6 h后更换培养液。质粒转染后采用嘌呤霉素筛选稳定表达细胞系。实验分组:OE-NC组(过表达对照)、OE-PPARα组(过表达PPARα)、OE-PPARα+siNC组(过表达PPARα+siRNA对照)、OE-PPARα+siHADHA组(过表达PPARα+沉默HADHA)。
(四) Western-Blot检测收集细胞后,用RIPA裂解液冰上裂解30 min,13 000 r/min离心取上清液,BCA法测定蛋白浓度。每孔上样30 μg蛋白样本,经SDS-PAGE凝胶电泳后转移至PVDF膜,5%脱脂奶粉室温封闭2 h,加入一抗4℃孵育过夜,TBST洗膜3次后,二抗室温孵育2 h,洗膜后曝光显影。
(五) qRT-PCR检测采用TRIzol法提取组织或细胞总RNA,检测RNA浓度后,按逆转录试剂盒说明书将RNA逆转录为cDNA。以cDNA为模板进行RT-PCR检测,β-actin作为内参,采用2-ΔCt法计算PPARα和HADHA的mRNA相对表达水平。
(六) CCK-8检测细胞活力细胞传代后以1 500个/孔接种于96孔板,分别培养0、24、48、72 h,每孔加入10 μl CCK-8试剂,继续孵育2 h,酶标仪检测450 nm处吸光值,反映细胞活力及增殖情况。
(七) 划痕愈合实验检测细胞迁移以5×105/孔的密度将细胞接种于6孔板,待细胞融合度达90%时,更换无血清培养基(细胞死亡过多时可加入1%血清维持渗透压),用100 μl无菌枪头在细胞单层划垂直直线,分别于0、24、48 h观察创口并拍照,计算划痕愈合率。
(八) Transwell实验检测细胞侵袭收集各组转染细胞制备悬液,以1×105/200 μL/ 孔接种于铺有基质胶的Transwell小室上室,下室加入600 μL含10%胎牛血清的培养液。37℃、5% CO2培养箱培养24 h后,取出小室,PBS清洗2次,4%多聚甲醛固定,结晶紫染色,显微镜下拍照并计数侵袭细胞数。
(九) 流式细胞仪检测细胞周期及凋亡① 细胞周期:胰酶消化细胞,离心后PBS洗涤2次,70%预冷乙醇4℃固定过夜,次日离心去除上清液,PBS洗涤后PI/RNase染色,流式细胞仪检测。②细胞凋亡:胰酶消化细胞,离心后PBS洗涤2次,加入Binding Buffer悬浮细胞,按说明书加入10 μL Annexin V-FITC与PI,避光孵育30 min,流式细胞仪检测。
(十) 油红O染色检测脂质蓄积去除细胞培养基,加入4%多聚甲醛固定15 min,彻底清洗后加入异丙醇孵育5 min,油红O染料孵育10 min,苏木素复染2 min,显微镜下观察并拍照。
(十一) 双荧光素酶报告实验以5×104/孔的密度将细胞接种于24孔板,待细胞密度达70%时,共转染野生型载体HADHA-WT或突变型载体HADHA-MUT与PPARα质粒,转染48 h后,弃培养基,加入100 μL报告基因裂解缓冲液冰上裂解5 min,离心后取20 μL上清液,加入荧光素酶底物,Promega荧光测定仪测定荧光素酶活性。
(十二) 动物实验12只6周龄BALB/c裸鼠(湖南斯莱克景达实验动物有限公司)适应性喂养5天后,随机分为OE-PPARα组和OE-NC组(每组6只)。将稳定表达的WiT49细胞制成悬液,与基质胶按1 ∶ 1比例混匀,每只裸鼠单侧皮下腋窝注射6×106个细胞,构建WT皮下移植瘤模型。每隔4天用游标卡尺测量肿瘤长径和短径,计算肿瘤体积(体积=0.5×长径×短径2),连续测定3周。处死小鼠后,无菌获取肿瘤组织,进行免疫组化染色、Tunel染色及WB检测。本动物实验经湖南省儿童医院伦理委员会批准(HCHDWLL — 2024 — 22)。
三、统计学处理采用GraphPad Prism 8.0进行统计分析及作图。服从正态分布的计量资料以x±s表示,组间比较采用两独立样本t检验。P < 0.05表示差异有统计学意义。
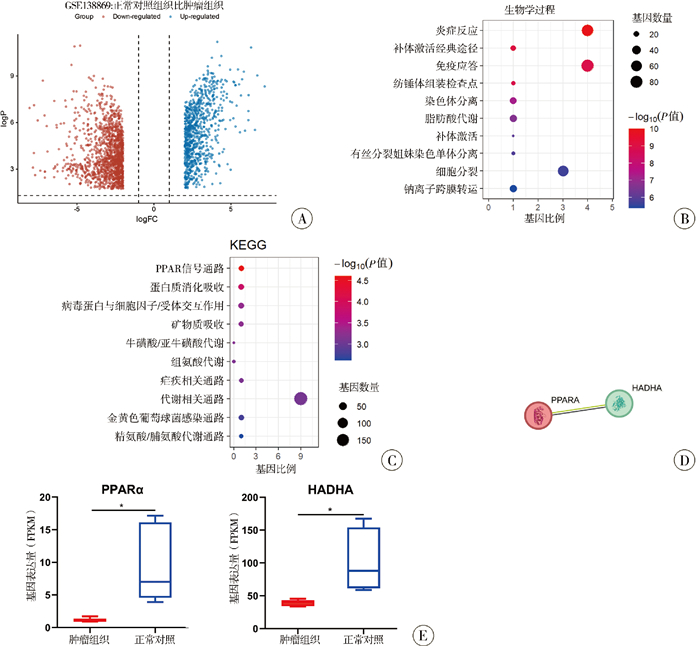
结果 一、GEO数据库WT差异表达基因筛选及分析GSE138869数据集共检测到41 316个基因,经筛选得到4 433个差异基因,其中上调基因2 251个(log FC>1,adj P < 0.05),下调基因2 182个(log FC<-1,adj P < 0.05)(图 1A)。GO分析显示,差异基因主要涉及炎症反应、补体激活、免疫应答、纺锤体组装检查点、染色体分离及脂肪酸代谢等生物学过程(图 1B);KEGG分析显示,差异基因富集于PPAR通路、蛋白质消化吸收通路、病毒蛋白-细胞因子/受体交互通路等(图 1C)。STRING数据库分析提示PPARα与HADHA存在潜在相互作用(图 1D),且二者在WT组织中均呈显著低表达(P < 0.05),见图 1E。
|
图 1 肾母细胞瘤GSE138869数据集差异基因筛选、功能富集及PPARα与HADHA的相互作用和表达分析 Fig.1 Differential gene screening, functional enrichment, interaction and expression analysis of PPAR α and HADHA in the GSE138869 dataset of nephroblastoma 注 A: 差异基因火山图;B: 差异基因GO功能富集分析;C: 差异基因KEGG通路富集分析;D: PPARα与HADHA的蛋白质相互作用网络;E: PPARα和HADHA在数据集肿瘤组织与正常组织中的表达水平对比 |
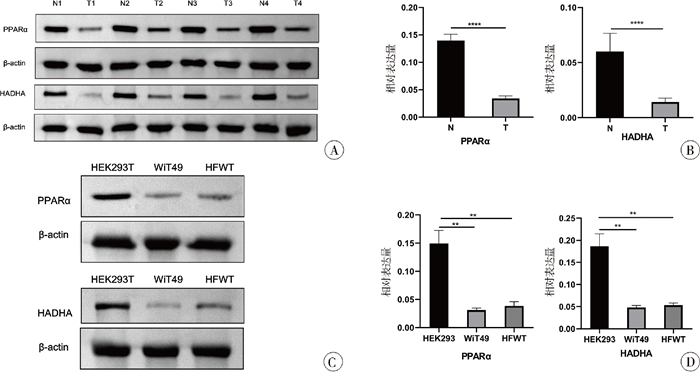
WB及qRT-PCR检测结果显示,与瘤旁组织相比,WT组织中PPARα和HADHA的蛋白及mRNA表达水平均显著降低(P < 0.05)(图 2A、2B);与HEK293T细胞相比,WT细胞系WiT49和HFWT中PPARα和HADHA的蛋白及mRNA表达也显著下调(P < 0.05),见面图 2C、2D。
|
图 2 WB和qRT-PCR检测PPARα与HADHA在肾母细胞瘤组织及细胞系中的表达 Fig.2 WB and qRT PCR detection of PPAR α and HADHA expression in clinical tissues and cell lines of nephroblastoma 注 A: WB检测PPARα和HADHA在瘤旁组织(N)与肿瘤组织(T)中的蛋白表达;B: qRT-PCR检测PPARα和HADHA在瘤旁组织与肿瘤组织中的mRNA表达;C:WB检测PPARα和HADHA在HEK293T细胞及肾母细胞瘤WiT49、HFWT细胞系中的蛋白表达;D:qRT-PCR检测PPARα和HADHA在HEK293T细胞及肾母细胞瘤WiT49、HFWT细胞系中的mRNA表达 |
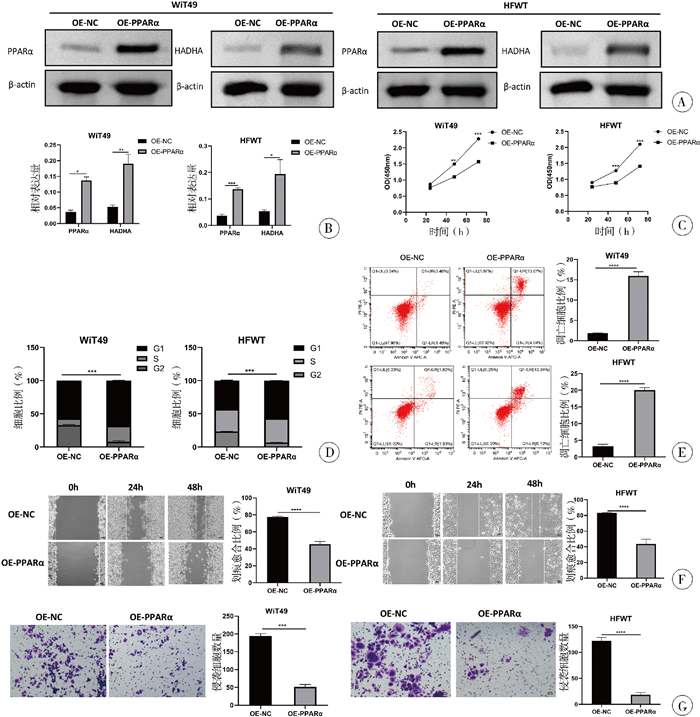
通过细胞转染质粒构建PPARα过表达细胞,建立过表达组和对照组:OE-PPARα, OE-NC,并用Westen-blot,RT-PCR证实PPARα过表达细胞能稳定表达PPARα,同时发现过表达PPARα后HADHA出现上调(图 3A、3B)。
|
图 3 PPARα过表达对肾母细胞瘤WiT49/HFWT细胞生物学行为的影响及转染效率验证 Fig.3 Effect of PPAR α overexpression on biological behaviors of nephroblastoma WiT49/HFWT cells and validation of transfection efficiency 注 A: WB验证PPARα过表达质粒转染效果及HADHA蛋白表达变化;B: qRT-PCR验证PPARα过表达质粒转染效果及HADHA mRNA表达变化;C: CCK-8实验检测细胞增殖能力;D: 流式细胞仪检测细胞周期分布;E: 流式细胞仪检测细胞凋亡率;F: 划痕愈合实验检测细胞迁移能力;G: Transwell实验检测细胞侵袭能力 |
CCK-8实验中PPARα过表达后细胞增殖能力呈现明显抑制,72小时OE-PPARα组WiT49、HFWT细胞OD值分别为(1.57±0.04)、(1.41±0.02),对照组OD值为(2.28±0.02)、(2.10±0.04),差异均具有统计学意义(P < 0.05),见图 3C。
细胞周期和凋亡方面,相较于对照组,PPARα过表达后细胞出现G1期阻滞(P < 0.05)。两种细胞系细胞凋亡百分比在过表达组[(15.93±0.86,20.05±0.57)%]均显著高于对照组[(1.83±0.08,3.17±0.52)%],差异具有统计学意义(P < 0.05),见图 3D、3E。
细胞迁移和侵袭方面,划痕实验中PPARα过表达组细胞划痕愈合率[(45.62±2.58,43.64±4.88)%]显著低于过表达对照组[(77.53±0.76,83.02±0.78)%],提示PPARα抑制细胞迁移作用(图 3F);Transwell侵袭实验中PPARα过表达组穿通基质胶微孔膜的细胞数[(51.33±5.73)%,(18.33±3.68)%]显著低于过表达对照组[(193.67±5.91) %,(122.33±5.25)%],提示PPARα抑制细胞侵袭能力(图 3G)。
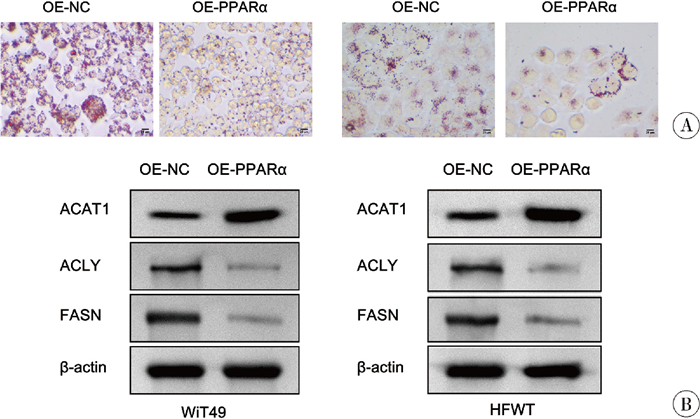
脂质代谢:油红O染色显示,OE-PPARα组细胞内红色脂质颗粒显著减少(图 4A);WB检测显示,OE-PPARα组乙酰辅酶A乙酰转移酶1(acetyl-coa acetyltransferase 1, ACAT1)表达上调,ATP柠檬酸裂解酶(ATP citrate lyase, ACLY)及脂肪酸合成酶(fatty acid synthase, FASN)表达下调,见图 4B。
|
图 4 PPARα过表达对肾母细胞瘤WiT49/HFWT细胞脂质代谢的影响 Fig.4 Effect of PPAR α overexpression on lipid metabolism in WiT49/HFWT nephroblastoma cells 注 A: 油红O染色观察细胞内脂质蓄积情况;B: WB检测脂质代谢相关酶ACAT1、ACLY及FASN的蛋白表达水平 |
本研究利用siRNA对PPARα过表达细胞进行HADHA敲减(siHADHA),用Westen-blot、RT-PC验证敲减效率,证实小干扰RNA siHADHA能显著降低细胞内HADHA基因表达(图 5A、5B)。
|
图 5 HADHA敲减对PPARα过表达肾母细胞瘤WiT49/HFWT细胞生物学行为的逆转作用及敲减效率验证 Fig.5 Reversal effect and knockdown efficiency verification of HADHA knockdown on biological behaviors of PPAR α overexpressing Wilms tumor WiT49/HFWT cells 注 A: WB验证HADHA siRNA敲减效率及PPARα蛋白表达;B: qRT-PCR验证HADHA siRNA敲减效率及PPARα mRNA表达;C: CCK-8实验检测细胞增殖能力恢复情况;D: 流式细胞仪检测细胞周期阻滞缓解情况;E: 流式细胞仪检测细胞凋亡率变化;F: 划痕愈合实验检测细胞迁移能力恢复情况 |
CCK-8实验中PPARα过表达后细胞增殖能力呈现明显抑制[(1.84±0.03)、(1.41±0.01)],而进一步将HADHA表达敲减后细胞的增殖能力呈现出一定程度的恢复[(2.02±0.04)、(1.59±0.01)],差异具有统计学意义(P < 0.05)。见图 5C。
细胞周期和凋亡方面,流式细胞仪分析细胞周期表明,相较于OE-PPAR+siNC组,OE-PPARα+ siHADHA组G1期细胞的比例较前者显著减少,G1期阻滞现象缓解(P < 0.05)。两种细胞系细胞凋亡百分比在HADHA敲减组中[(7.87±0.55)%,(11.21±0.75)%]均显著低于敲减对照组[(16.55±1.01)%,(20.19±1.83)%],差异具有统计学意义(P < 0.05)。见图 5D、5E。
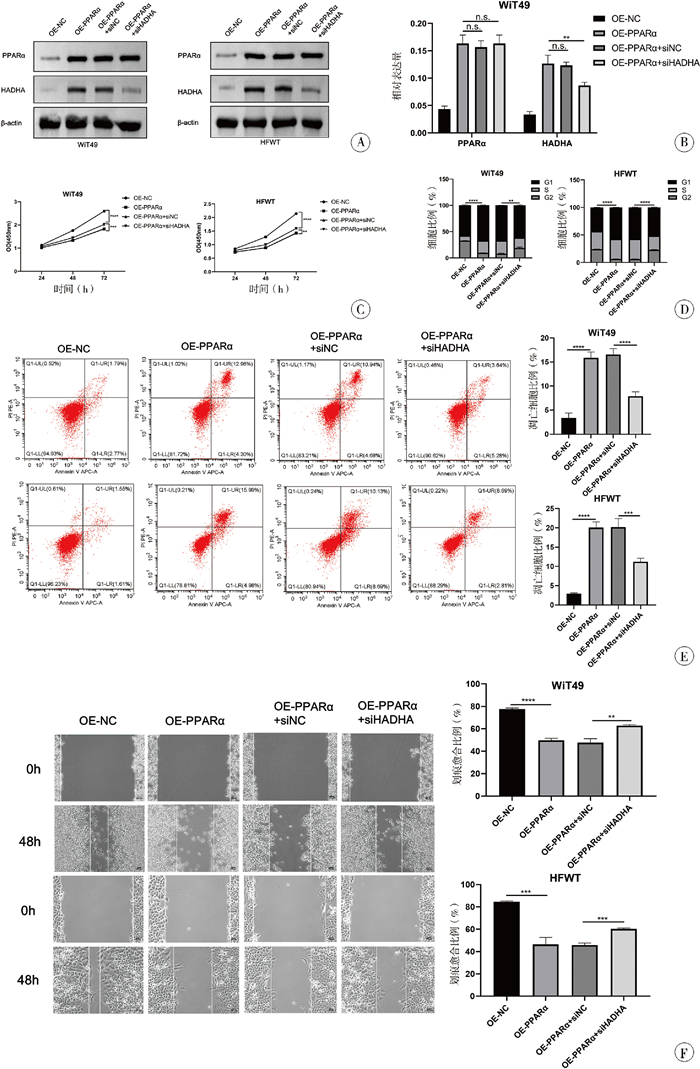
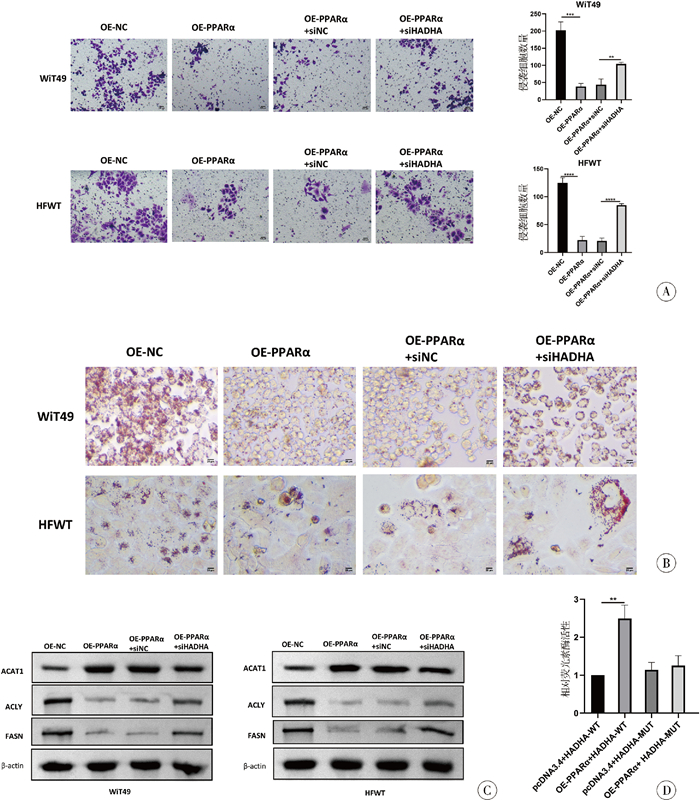
细胞迁移和侵袭方面,两种细胞系在划痕实验中OE-PPARα+siHADHA组细胞划痕愈合率[(62.87±0.78)%、(60.38±0.69)%]虽然低于OE-NC组[(77.5±0.93)%、(84.60±0.66)%],但仍显著高于OE-PPARα+siNC组[(47.72±2.85)%、(45.90±1.38)%] (图 5F);同样在Transwell侵袭实验中,OE-PPARα+siHADHA组[(104.00±4.08)、(85.00±2.16)]细胞穿膜数量低于OE-NC组[(202.00±20.31)、(124.67±7.76)],但显著高于OE-PPARα+siNC组[(43.67±13.81)、(20.67±4.19)],提示HADHA下调后可逆转PPARα过表达导致的侵袭能力抑制作用(图 6A);油红O染色显示,OE-PPARα+siHADHA组细胞内红色脂质颗粒显著多于OE-PPARα+siNC组(图 6B);WB检测显示,OE-PPARα+siHADHA组ACAT1表达减弱,ACLY及FASN表达上调,见图 6C。
|
图 6 HADHA敲减对PPARα过表达肾母细胞瘤WiT49/HFWT细胞脂质代谢的逆转作用及PPARα对HADHA的转录调控验证 Fig.6 Reversal effect of HADHA knockdown on lipid metabolism in PPAR α overexpressing Wilms tumor WiT49/HFWT cells and validation of PPAR α transcriptional regulation of HADHA 注 A: Transwell实验检测细胞侵袭能力恢复情况;B: 油红O染色观察细胞内脂质蓄积恢复情况;C: WB检测脂质代谢相关酶ACAT1、ACLY及FASN的蛋白表达变化;D: 双荧光素酶报告实验验证PPARα对HADHA启动子的转录调控作用 |
双荧光素酶报告实验显示,与pcDNA3.4+HADHA-WT组相比,OE-PPARα+HADHA-WT组细胞荧光信号强度显著升高(P < 0.05);而pcDNA3.4+HADHA-MUT组与OE-PPARα+HADHA-MUT组荧光信号强度无显著差异(图 6D),提示PPARα可正向调控HADHA转录活性。
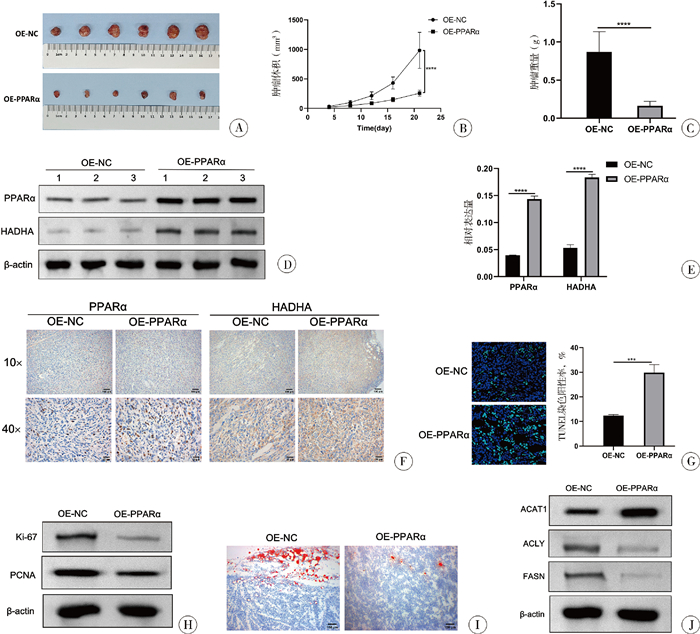
六、体内实验验证PPARα对WT的抑制作用裸鼠成瘤实验显示,造模第8天可见明显肿瘤形成,随时间推移肿瘤逐渐生长,OE-NC组肿瘤体积(983.15±279.11)mm3及质量(0.87±0.24)g均显著高于OE-PPARα组(257.74±45.45)mm3、(0.16±0.05)g,差异具有统计学意义(P < 0.05);见图 7A至7C。WB及qRT-PCR检测显示,OE-PPARα组肿瘤组织中PPARα和HADHA表达上调,差异有统计学意义(P < 0.05),见图 7D、7E;免疫组化染色显示,OE-PPARα组PPARα和HADHA阳性细胞比例显著高于OE-NC组(图 7F);Tunel染色显示,OE-PPARα组细胞凋亡比例显著增加(图 7G);WB检测显示,OE-PPARα组Ki-67、PCNA、ACLY及FASN表达下调,ACAT1表达上调,见图 7H、7J;油红O染色显示,OE-PPARα组肿瘤组织内脂质沉积减少(图 7I)。
|
图 7 裸鼠皮下移植瘤实验验证PPARα过表达对肾母细胞瘤生长的抑制作用 Fig.7 Experimental verification of subcutaneous transplantation of tumors in nude mice for examining the inhibitory effect of PPAR α overexpression on the growth of nephroblastoma 注 A: 两组裸鼠移植瘤大体形态;B: 移植瘤体积动态生长曲线;C: 移植瘤重量统计;D: WB检测瘤组织中PPARα和HADHA的蛋白表达;E: qRT-PCR检测瘤组织中PPARα和HADHA的mRNA表达;F: 免疫组化检测瘤组织中PPARα和HADHA的阳性表达情况;G: TUNEL染色检测瘤组织中细胞凋亡率;H: WB检测瘤组织中增殖标志物Ki-67和PCNA的蛋白表达;I: 油红O染色观察瘤组织内脂质沉积情况;J: WB检测瘤组织中脂质代谢相关酶ACAT1、ACLY及FASN的蛋白表达水平 |
WT是儿童最常见的肾脏恶性肿瘤,其发病与胚胎祖细胞发育异常相关,肾源性剩余被认为是WT的前体病变[10]。目前已发现WT1、CTNNB1、AMER1等40余种基因的异常表达与WT发生发展相关[11]。但关键分子及调控网络仍不明确,探索其分子机制对WT的个体化治疗及预后改善具有重要意义。
PPARα作为核激素受体超家族成员,是脂质代谢的关键调控因子,主要在肝脏、心脏、肾脏等代谢活跃组织中高表达[12]。PPARα与配体结合后,可与视黄酸X受体形成异二聚体,结合靶基因启动子区域的PPAR反应元件,调控下游基因转录,参与脂肪酸摄取、氧化及脂蛋白代谢等过程[12]。近年来研究表明,PPARα在肿瘤中发挥抑癌作用:如结肠癌组织中PPARα低表达,其缺失可通过增强DNMT1介导的P21甲基化和PRMT6介导的p27甲基化诱导肿瘤发生[13];PPARα可通过抑制GLUT1转录遏制肿瘤细胞糖代谢[14];本研究通过GSE138869数据集分析发现,PPAR通路是WT的关键通路,差异基因富集于脂肪酸代谢过程,且PPARα在WT组织中低表达;细胞及动物实验进一步证实,PPARα过表达可抑制WT细胞增殖、迁移及侵袭,诱导细胞凋亡,减少脂质沉积,提示PPARα在WT中具有抑癌作用。但PPARα在WT中低表达的具体原因仍需进一步研究。
HADHA是线粒体三功能蛋白的α亚基,参与长链脂肪酸β氧化过程:肾透明细胞癌中,HADHA过表达可调控ACAT1、ACLY及FASN表达,抑制细胞增殖并减少脂质蓄积[15];肝细胞癌中,UBE2O可通过泛素化HADHA促进其降解,参与脂质代谢重编程及肿瘤进展[8]。本研究发现,PPARα过表达可上调HADHA表达,双荧光素酶报告实验证实PPARα可正向调控HADHA转录活性;在PPARα过表达细胞中敲减HADHA后,PPARα的抑癌作用被部分逆转,提示HADHA是PPARα下游调控的关键靶点,二者协同参与WT的发生发展。
脂质代谢重编程是肿瘤细胞的重要特征,通过改变能量利用模式维持细胞生存并促进转移。ACAT1参与酮体生成及脂肪酸氧化,ACLY是连接糖代谢与脂质合成的关键酶,为脂肪酸合成提供原料,FASN则催化乙酰辅酶A与丙二酰辅酶A生成棕榈酸,参与脂肪酸从头合成[16-18]。研究表明,ACAT1过表达可促进脂肪酸氧化,抑制肾透明细胞癌进展, ACLY抑制剂可减小肝癌瘤体体积[19-20];FASN可通过重编程胆固醇代谢增强宫颈癌迁移侵袭能力[21]。本研究发现,PPARα过表达可上调ACAT1表达、下调ACLY及FASN表达,减少WT细胞脂质蓄积;敲减HADHA后,该效应被逆转,提示PPARα-HADHA轴可通过调控脂质代谢相关酶表达,改变WT细胞能量利用模式,发挥抑癌作用。
综上所述,本研究证实PPARα和HADHA在WT中均呈低表达,PPARα可通过转录调控HADHA表达,调控ACAT1、ACLY及FASN介导的脂质代谢过程,从而抑制WT细胞增殖、迁移及侵袭,促进细胞凋亡,减少脂质沉积。本研究为WT的分子机制研究提供了新的视角,PPARα-HADHA轴可能成为WT靶向治疗的潜在靶点。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 文献检索为王智,涂磊,宁峰;标本收集及实验开展实施为王智,涂磊,宁峰;实验结果分析为王智,何军,赵夭望;论文撰写为王智,何军,论文讨论分析为王智,赵夭望,宁峰,何军
| [1] |
Cunningham ME, Klug TD, Nuchtern JG, et al. Global disparities in Wilms tumor[J]. J Surg Res, 2020, 247: 34-51. DOI:10.1016/j.jss.2019.10.044 |
| [2] |
van den Heuvel-Eibrink MM, Hol JA, Pritchard-Jones K, et al. Position paper: rationale for the treatment of Wilms tumour in the UMBRELLA SIOP-RTSG 2016 protocol[J]. Nat Rev Urol, 2017, 14(12): 743-752. DOI:10.1038/nrurol.2017.163 |
| [3] |
Spreafico F, Fernandez CV, Brok J, et al. Wilms tumour[J]. Nat Rev Dis Primers, 2021, 7(1): 75. DOI:10.1038/s41572-021-00308-8 |
| [4] |
Brok J, Treger TD, Gooskens SL, et al. Biology and treatment of renal tumours in childhood[J]. Eur J Cancer, 2016, 68: 179-195. DOI:10.1016/j.ejca.2016.09.005 |
| [5] |
Dome JS, Graf N, Geller JI, et al. Advances in Wilms tumor treatment and biology: progress through international collaboration[J]. J Clin Oncol, 2015, 33(27): 2999-3007. DOI:10.1200/jco.2015.62.1888 |
| [6] |
Małodobra-Mazur M, Ołdakowska M, Dobosz T. Exploring PPAR gamma and PPAR alpha's regulation role in metabolism via epigenetics mechanism[J]. Biomolecules, 2024, 14(11): 1445. DOI:10.3390/biom14111445 |
| [7] |
朱金澳, 陈沙沙, 胡朗, 等. HADHA的乙酰化修饰在心血管疾病中的作用研究进展[J]. 心血管病学进展, 2025, 46(10): 906-911. Zhu JA, Chen SS, Hu L, et al. Role of HADHA acetylation modification in cardiovascular diseases[J]. Adv Cardiovasc Dis, 2025, 46(10): 906-911. DOI:10.16806/j.cnki.issn.1004-3934.2025.10.010 |
| [8] |
Ma ML, Zhang CH, Cao R, et al. UBE2O promotes lipid metabolic reprogramming and liver cancer progression by mediating HADHA ubiquitination[J]. Oncogene, 2022, 41(48): 5199-5213. DOI:10.1038/s41388-022-02509-1 |
| [9] |
Wu XY, Feng R, Wang XQ, et al. Roles of hydroxyacyl-CoA dehydrogenase trifunctional multienzyme complex subunit alpha, a lipid metabolism enzyme, in Wilms tumor patients[J]. J Cancer Res Ther, 2021, 17(5): 1281-1285. DOI:10.4103/jcrt.jcrt_1388_21 |
| [10] |
覃善璐, 董岿然. 肾母细胞瘤胚胎学起源的研究进展[J]. 临床小儿外科杂志, 2024, 23(7): 697-700. Qin SL, Dong KR. Research advances in embryological origin of Wilms tumor[J]. J Clin Ped Sur, 2024, 23(7): 697-700. DOI:10.3760/cma.j.cn101785-202207041-018 |
| [11] |
Treger TD, Chowdhury T, Pritchard-Jones K, et al. The genetic changes of Wilms tumour[J]. Nat Rev Nephrol, 2019, 15(4): 240-251. DOI:10.1038/s41581-019-0112-0 |
| [12] |
Wagner N, Wagner KD. Peroxisome proliferator-activated receptors and the hallmarks of cancer[J]. Cells, 2022, 11(15): 2432. DOI:10.3390/cells11152432 |
| [13] |
Luo YH, Xie C, Brocker CN, et al. Intestinal PPARα protects against colon carcinogenesis via regulation of methyltransferases DNMT1 and PRMT6[J]. Gastroenterology, 2019, 157(3): 744-759.e4. DOI:10.1053/j.gastro.2019.05.057 |
| [14] |
You ML, Jin JH, Liu Q, et al. PPARα promotes cancer cell Glut1 transcription repression[J]. J Cell Biochem, 2017, 118(6): 1556-1562. DOI:10.1002/jcb.25817 |
| [15] |
Liu S, Liu XL, Wu F, et al. HADHA overexpression disrupts lipid metabolism and inhibits tumor growth in clear cell renal cell carcinoma[J]. Exp Cell Res, 2019, 384(1): 111558. DOI:10.1016/j.yexcr.2019.111558 |
| [16] |
He W, Li YF, Liu SB, et al. From mitochondria to tumor suppression: ACAT1's crucial role in gastric cancer[J]. Front Immunol, 2024, 15: 1449525. DOI:10.3389/fimmu.2024.1449525 |
| [17] |
Xiao YC, Yang YH, Xiong HB, et al. The implications of FASN in immune cell biology and related diseases[J]. Cell Death Dis, 2024, 15(1): 88. DOI:10.1038/s41419-024-06463-6 |
| [18] |
Du F, Zhang HJ, Shao W, et al. Adenosine diphosphate-ribosylation factor-like 15 can regulate glycolysis and lipogenesis related genes in colon cancer[J]. J Physiol Pharmacol, 2022, 73(3): 403-411. DOI:10.26402/jpp.2022.3.08 |
| [19] |
Gu L, Zhu YH, Lin X, et al. The IKKβ-USP30-ACLY axis controls lipogenesis and tumorigenesis[J]. Hepatology, 2021, 73(1): 160-174. DOI:10.1002/hep.31249 |
| [20] |
Zheng M, Zhang SH, Zhou JJ, et al. ACAT1 suppresses clear cell renal cell carcinoma progression by AMPK mediated fatty acid metabolism[J]. Transl Oncol, 2024, 47: 102043. DOI:10.1016/j.tranon.2024.102043 |
| [21] |
Du QQ, Liu P, Zhang CY, et al. FASN promotes lymph node metastasis in cervical cancer via cholesterol reprogramming and lymphangiogenesis[J]. Cell Death Dis, 2022, 13(5): 488. DOI:10.1038/s41419-022-04926-2 |
 2026, Vol. 25
2026, Vol. 25


