2. 东南大学附属徐州市中心医院普通外科, 徐州 221000;
3. 东南大学附属徐州市中心医院介入科, 徐州 221000
2. Department of General Surgery, Affiliated Xuzhou Central Hospital, Southeast University, Xuzhou 221000, China;
3. Department of Interventional Radiology, Affiliated Xuzhou Central Hospital, Southeast University, Xuzhou 221000, China
神经母细胞瘤(neuroblastoma, NB)是儿童常见的颅外恶性实体肿瘤之一,其发病率和患病率呈上升趋势[1-2]。目前临床主要治疗方式包括手术、放化疗及免疫治疗等,但复发率和死亡率仍较高[3]。因此探索新的治疗靶点至关重要。糖基转移酶(glycosyltransferases, GT)是参与糖基化过程的关键酶,在细胞信号传导以及肿瘤细胞解离、转移、代谢、血管形成等过程中发挥着重要作用[4]。研究证实,GT可通过影响转录因子的转录调控、磷酸化或蛋白质稳定性,参与多种肿瘤的发生、进展和预后调控[5-6]。作为调控糖基化的重要酶类,靶向GT已成为一种极具潜力的治疗策略,但GT在NB中的具体功能尚未得到充分研究。本研究通过筛选GT差异表达基因构建GT相关预后模型,用于评估患儿预后,为NB的个体化诊疗、预后风险评估提供潜在治疗靶点。
资料与方法 一、资料来源从基因表达综合数据库(gene expression ommibus, GEO,https://www.ncbi.nlm.nih.gov/geo/)下载NB患儿样本的表达谱数据及临床信息(269例,生存时间>0,ID:GSE85047),作为模型构建的训练集。从UCSC Xena网站(https://xenabrowser.net/datapages/)获取TARGET数据库中NB患儿样本的基因表达谱数据以及临床信息(142例),作为模型验证的验证集。见表 1、表 2。
| 表 1 TARGET数据库中神经母细胞瘤患儿样本临床信息 Table 1 Clinical profiles of neuroblastoma children in the TARGET database |
|
|
| 表 2 GSE85047来源神经母细胞瘤患儿样本临床信息 Table 2 Clinical profiles of samples in GSE85047 in neuroblastoma children |
|
|
从MSigDb数据库(https://www.gsea-msigdb.org/gsea/msigdb)中下载获得213个糖基转移酶相关基因(GTs)。
二、临床实验标本收集2012年2月至2025年4月于徐州市中心医院接受手术或穿刺、经病理检查明确诊断的81例NB和25例神经节神经瘤患儿肿瘤组织标本。患儿监护人均知情并签署知情同意书。本研究通过徐州市中心医院研究伦理委员会审核批准(XZXY — LK — 20250213 — 0022)。
三、预后模型的构建和验证取训练集、验证集与213个GTs的交集,筛选出两个数据集共有的GTs,对交集后的GTs,在训练集中行单因素Cox回归分析,筛选预后相关的糖基转移酶基因(glycosyltransferase genes, GTGs),以P < 0.05为预后价值判定标准。采用最小绝对值收缩和选择算子(least absolute shrinkage and selection operator, LASSO)法进一步缩小候选基因范围,构建预后模型。基于该预后模型,分别计算训练集、验证集中患者的风险评分:Risk Score=∑geneEXP*coef,其中Coef表示回归系数,gene表示GTGs,EXP为各GTGs的相对表达值,∑表示基因之和。根据模型计算所得危险系数中位数,将患儿样本分为高、低风险两组。采用Log-rank检验及Kaplan-Meier法,评估高、低风险两组之间总体生存期(overall survival, OS)的差异;绘制受试者操作特征(receiver operating characteristic, ROC)曲线,计算1、3、5年生存率对应的曲线下面积(area under curve, AUC),确定该预后模型的预测精度。
四、鉴定差异表达基因及富集分析利用R语言“limma”包分析高、低风险组的基因表达数据,以差异倍数|logFC|>0.585、显著性阈值FDR < 0.01为标准,在两个数据集中筛选差异表达基因。采用R语言“ClusterProfiler”包对差异表达基因进行基因本体论(gene ontology,GO)功能和京都基因与基因组百科全书(kyoto encyclopedia of genes and genomes,KEGG)通路富集分析。
五、单样本基因集富集分析(single sample GSEA,ssGSEA)利用R语言“GSVA”包中的ssGSEA方法,分析高、低风险组适应性免疫细胞和固有免疫细胞的浸润水平差异。
六、细胞培养、转染及分组NB小鼠细胞系9464D和975A2(由西雅图儿童研究所Rimas Orentas博士赠予),培养于含有10%胎牛血清(以色列BI公司)和1%青霉素/链霉素(Gibco)的高葡萄糖杜尔贝科改良鹰培养基(Dulbecco's modified eagle medium, DMEM)中。将细胞置于5%CO2、37℃培养箱中培养,待细胞铺满培养瓶80% ~90%,且培养基颜色呈黄色时进行传代。实验均在无支原体感染的情况下开展。
B3GALT4敲低慢病毒(Sh-B3GALT4, 5'-CCTACTACTGGTGATCATCTG-3')、B3GALT4敲低空载体慢病毒(Scramble)、B3GALT4过表达慢病毒(OE-B3GALT4)及B3GALT4过表达空载体慢病毒(Vector)均由广州锐博生物有限公司合成。采用Lipo 2000TM转染试剂(美国Invitrogen公司)将上述慢病毒转染至9464D和975A2细胞,分为Sh-B3GALT4组、Scramble组、OE-B3GALT4组及Vector组;采用嘌呤霉素(北京索莱宝生物科技有限公司)筛选稳定转染的细胞用于后续实验。975A2细胞嘌呤霉素筛选浓度为4 μg/mL,9464D细胞嘌呤霉素筛选浓度为3 μg/mL。
七、转录实时荧光定量聚合酶链式反应(quantitative real-time polymerase chain reaction, qRT-qPCR)实验使用Trizol溶液裂解细胞提取总RNA,PrimScript RT主混合剂用于逆转录。使用SYBR Green PCR试剂盒(日本Takara公司)在Q5型荧光定量PCR仪(美国ABI公司)中进行qRT-PCR检测。循环特性如下:94℃,30 s;94℃,5 s;60℃,30 s;共40个循环。按照△△Ct法计算基因相对表达量。B3GALT4引物序列:上游:5'-CTCCTGGCGGTCCTACTACT-3',下游:5'-CCACCACAGGCATGAGAGTT- 3';GAPDH引物序列:上游:5'-GGTATGACACACAATTTGGC-3',下游:5'-GAGCACAGGGTACTATTG-3'。
八、Western blot收集样本后,采用RIPA缓冲液在冰上溶解30 min;于12 000 rpm、4℃下离心5 min后,取上清液,采用二辛可酸法测定法测定上清液中的蛋白质浓度。随后,将蛋白质转移到十二烷基硫酸钠聚丙烯酰胺凝胶分离后转移至聚偏二氟乙烯膜,用5%脱脂牛奶在室温下封闭1 h;裁剪条带放入对应一抗中孵育,4℃摇床上过夜。次日清洗膜后,将其与对应的二抗在室温下孵育1 h。采用GelView 6000Plus系统进行条带曝光拍照,采用Image J软件进行定量分析,以β-actin为内参蛋白。
九、细胞增殖实验(cell counting kit-8, CCK-8)将2×104/mL细胞接种在96孔板中,孵育24、48和72 h后,用CCK-8溶液(北京索莱宝生物科技有限公司)取代培养基,培养物孵育2 h;样品吸光度(450 nm)通过酶标仪(Biotek Instruments Inc, USA)测量,每个样品测量3次。
十、集落形成实验将细胞接种于6孔板中,2周后将菌落固定在4%多聚甲醛中,并用0.1%结晶紫溶液染色、洗涤、晾干后拍照。采用ImageJ软件对菌落进行计数。
十一、Transwell实验将悬浮在无血清RMPI1640培养基的细胞接种到孔径为8 μm的Transwell小室的上室。侵袭实验中基质胶按1 ∶ 4稀释(BD Biosciences,美国)后接种,后将600 μL全培养基添加到下室中,48 h后棉棒轻柔擦去上室未穿膜细胞,磷酸盐缓冲盐水(phosphate buffered saline,PBS)洗涤后用4%多聚甲醛固定,用0.1%结晶紫溶液染色、拍照。
十二、免疫组化染色(immunohistochemistry,IHC)将4 μm厚组织病理学切片置于60℃烤箱中烘烤过夜,随后行脱蜡、脱水处理。依次完成抗原修复和内源性过氧化物酶活性阻断后,将切片与各种一抗在4℃潮湿容器中孵育24 h,再与匹配的二抗在环境温度下孵育1 h。采用二氨基联苯胺显色5 min,直至观察到棕色反应结果。使用20倍光学显微镜获取数字图像。
IHC检测结果由两位对实验流程实施盲法的专业病理学家共同分析。阳性细胞的频率分为5类:0级(阴性)、1级(1% ~25%)、2级(26% ~50%)、3级(51% ~75%)和4级(76% ~100%);染色度分为4类:0级(阴性)、1级(弱)、2级(中等)、3级(强)。IHC评分通过上述两项指标相乘得出。
十三、统计学处理采用R 4.1.1、SPSS 23.0及GraphPad Prism 8进行统计学分析。服从正态分布的计量资料以x ± s表示,两组间比较采取Student's t检验,多组间比较采用One-way ANOVA。计数资料采用频数、构成比表示,组间比较采用卡方检验;单变量、多变量Cox回归模型用于评估风险模型的独立预后价值;采用Mann-Whitney检验比较两组之间免疫细胞浸润和免疫相关通路差异。P < 0.05为差异有统计学意义。
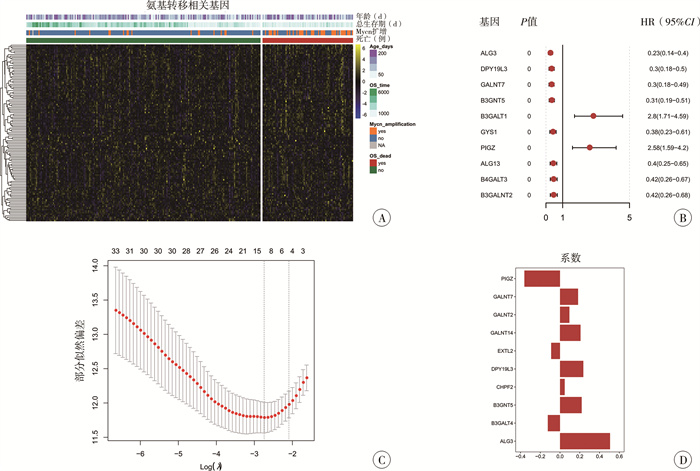
结果 一、预后相关GTs筛选及预后模型构建共获取TARGET、GSE85047数据集交集GTs 113个(图 1A)。基于训练集对113个GTs进行单因素Cox生存分析,共筛选出35个与预后相关的基因(P<0.05)。根据P值从小到大进行排序,选取预后相关性最强的10个基因并绘制森林图,分别为磷脂酰肌醇聚糖, 类Z(phosphatidylinositol glycan, class Z,PIGZ)、多肽N-乙酰半乳糖胺基转移酶7 (polypeptide N-acetylgalactosaminyltransferase 7,GALNT7)、多肽N-乙酰半乳糖胺基转移酶2(Polypeptide N-acetylgalactosaminyltransferase 2,GALNT2)、多肽N-乙酰半乳糖氨基转移酶14(polypeptide N-acetylgalactosaminyltransferase 14,GALNT14)、外生性骨疣样糖基转移酶2(exostosin-like glycosyltransferase 2,EXTL2)、dpy-19样C-甘露糖基转移酶3(dpy-19 like C-mannosyltransferase 3,DYP19L3)、软骨素聚合因子2(chondroitin polymerizing factor 2,CHPF2)、β-1, 3-N-葡糖胺基转移酶5(UDP-GlcNAc: betaGal beta-1, 3-N-acetylglucosaminyltransferase 5,B3GNT5)、B3GALT4、天冬酰胺连接糖基化3(asparagine-linked glycosylation 3,ALG3)(图 1B)。最后,通过LASSO回归模型及交叉优化,确定10个基因组成的预后模型(图 1C、1D)。
|
图 1 神经母细胞瘤预后相关基因筛选并构建模型 Fig.1 Screening of prognosis related genes for model constructing 注 A:GTGs表达量z-score归一化热图;B:top10预后相关GTGs森林图展示;C:LASSO回归交叉验证误差曲线展示每个Lambda的置信区间;D:10个预后相关GTGs的LASSO回归系数 |
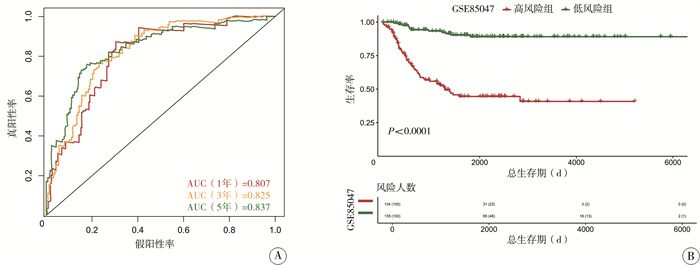
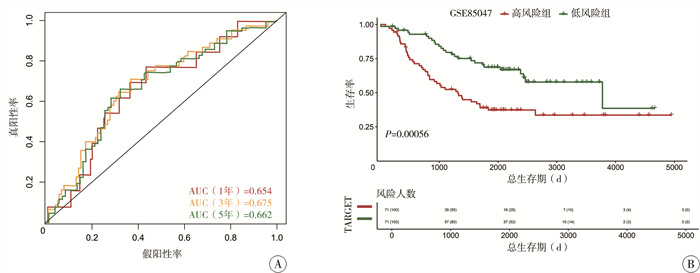
在训练集中,该预后模型预测患儿1、3、5年的AUC值分别为0.807、0.825和0.837(图 2A);验证集中,其预测患儿1、3、5年的AUC值分别为0.654、0.675和0.662(图 3A)。在训练集、验证集中,高风险组的OS显著短于低风险组(P < 0.05)(图 2B,图 3B)。
|
图 2 神经母细胞瘤训练集预后模型效能评估 Fig.2 Performance of the prognostic model in training set 注 A:模型预测神经母细胞瘤患儿1、3、5年生存率的ROC曲线;B:高风险和低风险组Kaplan-Meier生存曲线;AUC:受试者操作特征曲线下面积 |
|
图 3 神经母细胞瘤验证集预后模型效能评估 Fig.3 Performance of the prognostic model in training set 注 A:模型预测神经母细胞瘤患儿1、3、5年生存率的ROC曲线;B:高风险和低风险组Kaplan-Meier生存曲线 |
训练集中,单变量Cox分析结果显示,年龄(HR=4.39,95%CI=2.71~7.12,P < 0.001)、INSS分期(HR=1.68,95%CI=1.36~2.09,P < 0.001)、MYCN状态(HR=5.92,95%CI=3.71~9.43,P < 0.001)和风险评分(HR=4.54,95%CI=3.24~6.35,P < 0.001)均与预后显著相关(图 4A);多变量Cox分析结果显示,年龄(HR=2.82,95%CI=1.72~4.63,P < 0.001)、INSS分期(HR=1.61,95%CI=1.17~2.22,P < 0.001)和风险评分(HR=2.42,95%CI=1.47~3.99,P < 0.001)为预后的独立影响因素(图 4B)。

|
图 4 神经母细胞瘤预后模型风险评分与临床特征森林图 Fig.4 Forest plot of model risk score versus clinical profiles 注 A:训练集单因素Cox回归森林图;B:训练集多因素Cox回归森林图;C:验证集单因素Cox回归森林图;D:验证集多因素Cox回归森林图 |
验证集中,单变量Cox分析结果显示,年龄(HR=2.43,95%CI=1.33~4.45,P < 0.01)和风险评分(HR=1.73,95%CI=1.20~2.51,P < 0.01)均与预后显著相关(图 4C);多变量Cox分析结果显示,年龄(HR=2.17,95%CI=1.18~3.98,P < 0.05)和风险评分(HR=1.62,95%CI=1.09~2.39,P < 0.05)为预后的独立影响因素(图 4D)。
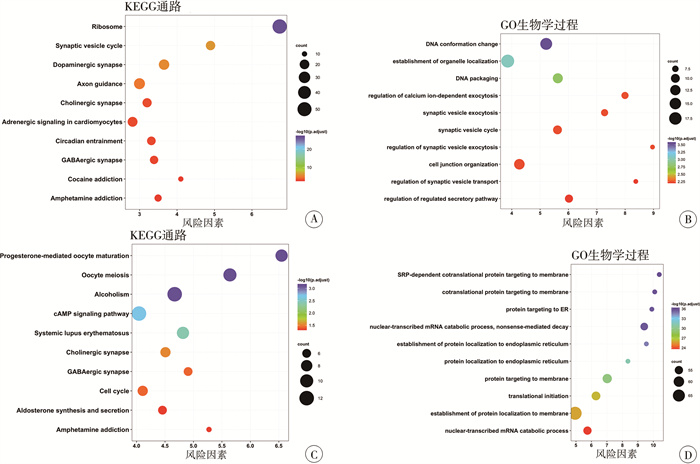
四、差异表达基因的富集分析训练集差异基因显著富集于DNA构象变化、钙离子依赖性胞吐作用的调节及细胞连接组织结构等生物学过程(图 5A、5B);验证集差异基因显著富集于蛋白靶向内质网、细胞膜以及核转录的mRNA分解过程等生物学过程(图 5C、5D)。
|
图 5 高低风险组神经母细胞瘤差异基因富集分析 Fig.5 Differential gene enrichment analysis between high-risk and low-risk groups 注 A、B:训练集;C、D:验证集 |
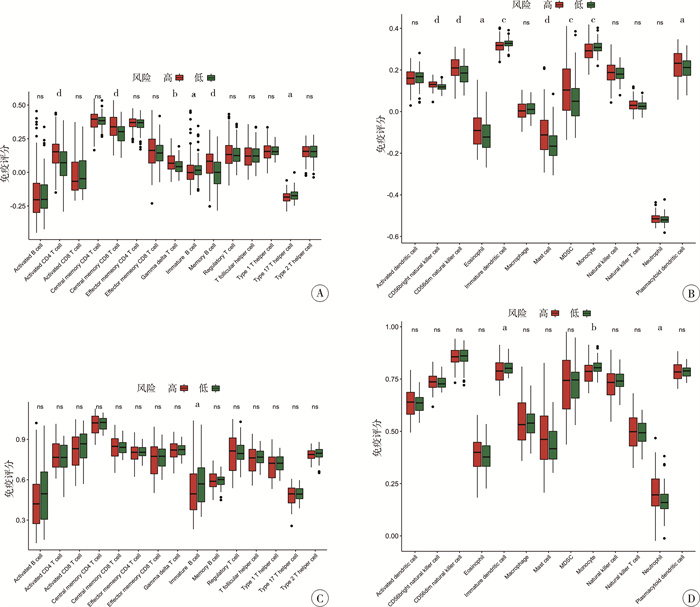
训练集中,活化CD4+T细胞、中心记忆CD8+T细胞、γδT细胞、记忆B细胞、CD56dim NK细胞、CD56bright NK细胞、嗜酸性粒细胞、肥大细胞、骨髓来源抑制细胞及浆细胞在高风险组患儿中浸润程度高。而未成熟B细胞、未成熟树突细胞及单核细胞在高风险组患儿中浸润程度低于低风险组患儿(图 6A、6B)。验证集中,浆细胞在高风险组患儿中浸润程度高,而未成熟B细胞、未成熟树突细胞及单核细胞在高风险组患儿中浸润程度低于低风险组患儿(图 6C、6D)。
|
图 6 神经母细胞瘤高低风险组患儿28种免疫细胞浸润分布 Fig.6 Immune infiltration profiles of 28 immune cell types in high-risk and low-risk groups 注 A:训练集中15种Adaptive免疫细胞分布;B:训练集中13种Innate免疫细胞分布;C:验证集中15种Adaptive免疫细胞分布;D:验证集中13种Innate免疫细胞分布;a: P < 0.05,b: P < 0.01,c: P < 0.001,d: P < 0.0001 |
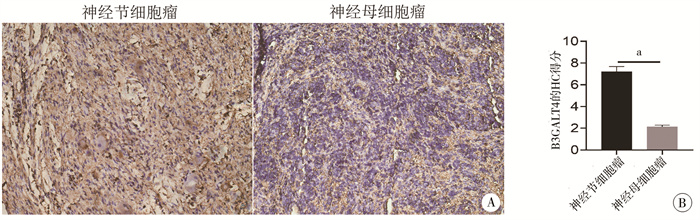
B3GALT4阳性黄色颗粒主要定位于细胞质。神经节细胞瘤组织B3GALT4免疫组化评分高于神经母细胞瘤组织,差异有统计学意义(图 7A、7B,P < 0.0001)。
|
图 7 B3GALT4在神经节细胞瘤及神经母细胞瘤组织中的表达情况 Fig.7 Expression of B3GALT4 in ganglioneuroma and neuroblastoma tissues 注 A:神经节细胞瘤和神经母细胞瘤组织中B3GALT4表达的典型免疫组化图片(20×);B:神经节细胞瘤和神经母细胞瘤组织中B3GALT4的IHC评分, a: P < 0.0001 |
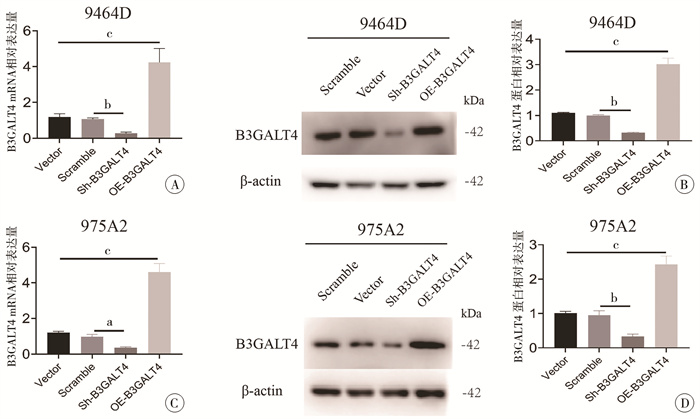
在NB细胞中,分别从mRNA、蛋白水平验证B3GALT4敲低和过表达的转染效果。qRT-PCR和Weston blot结果显示,在9464D、975A2细胞中,OE-B3GALT4组细胞B3GALT4基因mRNA及蛋白表达水平均显著高于Vector组(图 8A、8C;P < 0.0001);Sh-B3GALT4组mRNA和蛋白水平均显著低于Scramble组,差异均具有统计学意义(图 8B、8D;P < 0.0001)。
|
图 8 qRT-PCR及Weston blot检测9464D、975A2细胞B3GALT4基因mRNA、蛋白水平 Fig.8 Detection of B3GALT4 mRNA and protein expression levels in 9464D and 975A2 cells via qRT-PCR and Western blot 注 A:qRT-PCR检测9464D细胞B3GALT4基因mRNA表达水平;B:Weston blot检测9464D细胞B3GALT4蛋白水平及统计分析结果;C:qRT-PCR检测975A2细胞B3GALT4基因mRNA表达水平;D:Weston blot检测975A2细胞B3GALT4蛋白水平及统计分析结果。a: P < 0.01,b: P < 0.001,c: P < 0.0001 |
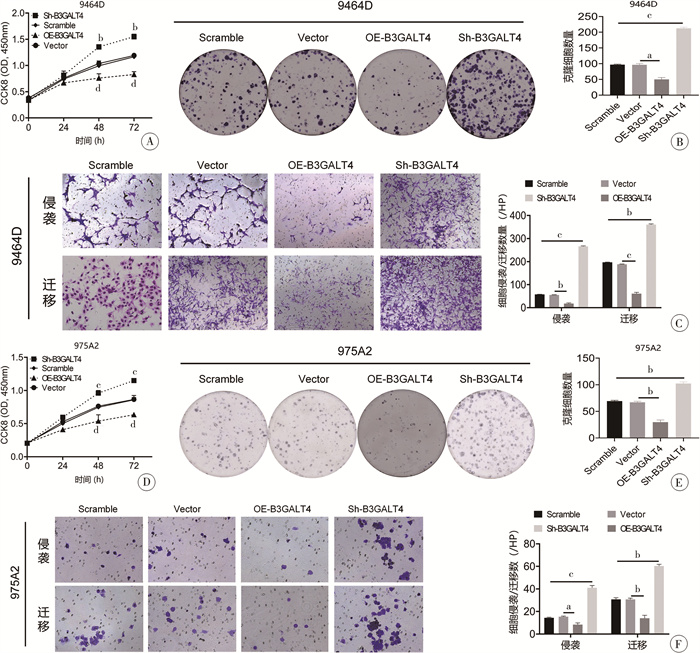
在9464D、975A2细胞中,CCK8和集落形成实验结果显示,敲低B3GALT4明显促进NB细胞的增殖(图 9A、9B、9D、9E),而过表达B3GALT4则可抑制NB细胞的增殖;Transwell实验结果显示,敲低B3GALT4可促进NB细胞的迁移侵袭,过表达B3GALT4则可能抑制NB细胞的迁移侵袭(图 9C、9F)。
|
图 9 敲低或过表达B3GALT4对神经母细胞瘤肿瘤细胞增殖与侵袭的影响 Fig.9 Effects of knockdown or overexpression of B3GALT4 on proliferation and invasion of NB cells 注 A、D:CCK-8检测上调或下调B3GALT4对9464D、975A2细胞增殖能力的影响;B、E:集落形成实验检测上调或下调B3GALT4对9464D、975A2细胞增殖的影响及统计分析结果;C、F:Transwell实验检测上调或下调B3GALT4对9464D、975A2细胞侵袭的影响(×20)及统计分析结果;a: P < 0.01,b: P < 0.001,c: P < 0.0001,d: P < 0.0001 |
NB是儿童常见颅外实体瘤之一,探索新的预后标志物有助于NB的分级管理与精准治疗。本研究构建了NB糖基转移酶预后模型,分析了不同风险病人的临床特征,验证结果显示该模型预测NB生存性能良好;多因素Cox回归提示该模型为NB患儿重要的独立预后因素;同时,探讨了高低风险患儿预后差异的可能分子机制,为NB的临床决策及深入研究提供了参考。
糖基转移酶是蛋白糖基化催化过程中的重要酶类,负责将特定的糖基与对应受体结合形成糖链;细胞糖基转移酶的差异表达可引起糖基化异常,进而导致细胞生物学行为改变。神经节苷脂是一种特殊的糖基化产物,其中双唾液酸神经节苷脂GD2靶点的免疫治疗已应用于高危NB患儿的治疗,并取得一定疗效。本模型纳入的10个GTs中,B3GALT4是参与GD2代谢的关键酶。该基因属于β1, 3-半乳糖基转移酶家族,可通过β1, 3连接方式将半乳糖转移到GM2/GD2的N-乙酰基半乳糖-甲苯胺残基,参与多种肿瘤的发生、发展。既往研究发现B3GALT4可以通过抑制脂筏的形成,促进趋化因子CXCL9/10的产生,影响肿瘤免疫微环境。而本研究发现,过表达B3GALT4可显著抑制NB细胞的增殖、迁袭。但与该基因在乳腺癌中表达完全相反,研究证实,B3GALT4在乳腺癌中高表达,不仅可以诱导乳腺癌上皮间质转化过程,还可以促进乳腺癌的增殖和迁袭[7];此外,该基因结合乳腺癌的超声特征可用于术前腋窝淋巴结转移的预测[8]。在结直肠癌中,B3GALT4通过影响鞘脂代谢,有望成为新型的治疗靶点[9]。PIGZ也作为脂质代谢相关基因,被纳入胃癌风险预测模型[10]。EXTL2为α1, 4-N-乙酰己糖胺基转移酶,具有双重体外催化活性。在胃癌细胞中,敲除EXTL2会促进癌细胞硫酸乙酰肝素(heparan sulfate, HS)的过度产生和上调Syndecan-4,进而增强细胞运动能力和侵袭性[11]。在肝脏中,敲除肿瘤抑制基因EXTL2可通过Toll样4受体激活炎症并促进肿瘤发生[12]。由此可见,EXTL2在胃癌[11]、结直肠癌[13]、脑膜瘤[10]中大多为肿瘤保护基因,这与NB模型中预测基因的性质相一致。研究表明,多肽N-乙酰半乳糖转移酶(polypeptide N-acetylgalactosaminyltransferase, GALNT)家族成员的表达在各种肿瘤中失调,与肿瘤发生及肿瘤细胞生长、转移、粘附密切相关,是肿瘤发展的重要早期指标。例如,GALNT7上调可以促进前列腺癌[14]、甲状腺癌[15]及胶质瘤[16]的增殖和侵袭;先前研究表明,GALNT2表达是NB患者生存的影响因素,GALNT2可以调节胰岛素样生长因子-1受体(IGF-1R)的O-糖基化,干扰IGF-1触发的二聚化和IGF-1R活性,从而调控NB细胞特性[17]。N-乙酰半乳糖胺基转移酶-14(N-acetylgalactosaminyltransferase 14, GALNT14)是启动O-糖基化的关键酶,研究表明,GALNT14过表达可以促进乳腺癌的干性、远处转移[18]。此外,GALNT14也可作为预测晚期肝癌[19]、胰腺癌[20]、晚期食管癌[21]等多种恶性肿瘤生存期及治疗效果的标志物。CHPF2是组成硫酸软骨素合酶家族蛋白一员,Wen等[22]发现丝裂原活化蛋白激酶介导的CHPF2磷酸化通过激活核因子激活的B细胞κ-轻链增强复合物信号传导,促进结直肠癌细胞增殖和转移;CHPF2的表达与肝细胞癌患者预后不良呈正相关,可通过激活上皮间质转化通路促进肝癌细胞的增殖和迁移[23]。B3GNT5是β-1, 3-N-乙酰氨基葡萄糖基转移酶家族的成员,在乳糖生物合成中起着至关重要的作用。研究证实B3GNT5的高表达与神经胶质瘤[24]、胰腺癌[25]的进展显著相关。α-1, 3-甘露糖基转移酶(α-1, 3 mannosyltransferase, ALG3)定位于高尔基体和内质网,参与早期N-聚糖的合成。Xue等[26]通过单细胞转录组测序研究发现,ALG3的表达量影响乳腺癌中缺氧、细胞凋亡、DNA修复等过程,抑制ALG3的活性可降低乳腺癌细胞生长代谢速度。同时,ALG3的敲除可以调节肿瘤微环境和程序性死亡配体1(programmed cell death Ligand 1, PD-L1)的糖基化,增强免疫治疗的效果[27]。综合以上模型预后基因的分析可见,绝大多数基因在不同类型肿瘤中具有关键的调节作用,这也在一定程度上证实了本预后模型的可靠性。
本研究存在一定的局限性:首先,本研究主要基于公共数据库的数据分析,可能限制了地域引起的患者差异,未来有待多中心临床数据进一步验证;其次,虽然本研究验证了B3GALT4的生物学功能,B3GALT4调控NB的机制仍需进一步探索。
总之,本研究构建了NB的GTs预后风险模型,该模型可较好地预测患儿预后,B3GALT4可能成为NB治疗的新靶点。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 贺士卿负责文献检索,实施实验,论文撰写;沙永亮负责实验设计和实施、全文知识性内容的审读与修正;王美德负责数据收集、研究结果分析与讨论
| [1] |
Yue CY, Zhang Q, Sun FY, et al. Global, regional and national burden of neuroblastoma and other peripheral nervous system tumors, 1990 to 2021 and predictions to 2035:visualizing epidemiological characteristics based on GBD 2021[J]. Neoplasia, 2025, 60: 101122. DOI:10.1016/j.neo.2025.101122 |
| [2] |
Siegel RL, Giaquinto AN, Jemal A. Cancer statistics, 2024[J]. CA Cancer J Clin, 2024, 74(1): 12-49. DOI:10.3322/caac.21820 |
| [3] |
Siegel DA, Li J, Henley SJ, et al. Geographic variation in pediatric cancer incidence-United States, 2003-2014[J]. MMWR Morb Mortal Wkly Rep, 2018, 67(25): 707-713. DOI:10.15585/mmwr.mm6725a2 |
| [4] |
Lin Y, Lubman DM. The role of N-glycosylation in cancer[J]. Acta Pharm Sin B, 2024, 14(3): 1098-1110. DOI:10.1016/j.apsb.2023.10.014 |
| [5] |
Čaval T, Alisson-Silva F, Schwarz F. Roles of glycosylation at the cancer cell surface: opportunities for large scale glycoproteomics[J]. Theranostics, 2023, 13(8): 2605-2615. DOI:10.7150/thno.81760 |
| [6] |
Wang ZF, Liu JX, Wang XM, et al. Glycosyltransferase B4GALNT1 promotes immunosuppression in hepatocellular carcinoma via the HES4-SPP1-TAM/Th2 axis[J]. Mol Biomed, 2024, 5(1): 65. DOI:10.1186/s43556-024-00231-w |
| [7] |
Sha YL, Zhuang HJ, Shi J, et al. B3GALT4 modulates tumor progression and autophagy by AKT/mTOR signaling pathway in breast cancer[J]. Discov Oncol, 2024, 15(1): 488. DOI:10.1007/s12672-024-01371-9 |
| [8] |
Sha YL, Ge S, Wang YQ, et al. Ultrasound-based radiomics combined with B3GALT4 level to predict sentinel lymph node metastasis in primary breast cancer[J]. Front Oncol, 2025, 15: 1570493. DOI:10.3389/fonc.2025.1570493 |
| [9] |
Shi LP, Mao NQ, Zheng ZH, et al. Glycosphingolipids-dependent phospholipid metabolism enhances cancer initiation and progression through SMPD1/GLTP/B3GALT4/ST8SIA6 signaling axis: a novel therapeutic target[J]. Int J Med Sci, 2025, 22(3): 604-615. DOI:10.7150/ijms.103834 |
| [10] |
Wei XL, Luo TQ, Li JN, et al. Development and validation of a prognostic classifier based on lipid metabolism-related genes in gastric cancer[J]. Front Mol Biosci, 2021, 8: 691143. DOI:10.3389/fmolb.2021.691143 |
| [11] |
Marques C, Poças J, Gomes C, et al. Glycosyltransferases EXTL2 and EXTL3 cellular balance dictates heparan sulfate biosynthesis and shapes gastric cancer cell motility and invasion[J]. J Biol Chem, 2022, 298(11): 102546. DOI:10.1016/j.jbc.2022.102546 |
| [12] |
Nadanaka S, Hashiguchi T, Kitagawa H. Aberrant glycosaminoglycan biosynthesis by tumor suppressor EXTL2 deficiency promotes liver inflammation and tumorigenesis through Toll-like 4 receptor signaling[J]. FASEB J, 2020, 34(6): 8385-8401. DOI:10.1096/fj.201902076R |
| [13] |
Wang ZR, Li TA, Sun MY, et al. Metabolomics-and proteomics-based disease diagnostic classifier model for the prediction and diagnosis of colorectal carcinoma[J]. J Proteome Res, 2025, 24(4): 2096-2111. DOI:10.1021/acs.jproteome.5c00010 |
| [14] |
Scott E, Hodgson K, Calle B, et al. Upregulation of GALNT7 in prostate cancer modifies O-glycosylation and promotes tumour growth[J]. Oncogene, 2023, 42(12): 926-937. DOI:10.1038/s41388-023-02604-x |
| [15] |
Li YT, Miao JH, Liu CZ, et al. Kushenol O regulates GALNT7/NF-κB axis-Mediated macrophage M2 polarization and efferocytosis in papillary thyroid carcinoma[J]. Phytomedicine, 2025, 138: 156373. DOI:10.1016/j.phymed.2025.156373 |
| [16] |
Hua S, Li HY, Liu YG, et al. High expression of GALNT7 promotes invasion and proliferation of glioma cells[J]. Oncol Lett, 2018, 16(5): 6307-6314. DOI:10.3892/ol.2018.9498 |
| [17] |
Ho WL, Chou CH, Jeng YM, et al. GALNT2 suppresses malignant phenotypes through IGF-1 receptor and predicts favorable prognosis in neuroblastoma[J]. Oncotarget, 2014, 5(23): 12247-12259. DOI:10.18632/oncotarget.2627 |
| [18] |
Gadwal A, Purohit P, Khokhar M, et al. GALNT14 in association with GDF-15 promotes stemness and drug resistance through β-catenin signalling pathway in breast cancer[J]. Mol Biol Rep, 2024, 51(1): 691. DOI:10.1007/s11033-024-09645-9 |
| [19] |
Lin CL, Chien RN, Chen LW, et al. Rs9679162 genotype predicts prognosis of real-world advanced hepatocellular carcinoma treated by sorafenib[J]. Cancer Biomark, 2023, 36(3): 251-266. DOI:10.3233/CBM-220042 |
| [20] |
Shu TT, Zhang Y, Sun T, et al. Polypeptide N-acetylgalactosaminyl transferase 14 is a novel mediator in pancreatic β-cell function and growth[J]. Mol Cell Endocrinol, 2024, 591: 112269. DOI:10.1016/j.mce.2024.112269 |
| [21] |
Tsou YK, Liang KH, Lin WR, et al. GALNT14 genotype as a response predictor for concurrent chemoradiotherapy in advanced esophageal squamous cell carcinoma[J]. Oncotarget, 2017, 8(17): 29151-29160. DOI:10.18632/oncotarget.16253 |
| [22] |
Wen XQ, Qin JL, Zhang X, et al. MEK-mediated CHPF2 phosphorylation promotes colorectal cancer cell proliferation and metastasis by activating NF-κB signaling[J]. Cancer Lett, 2024, 584: 216644. DOI:10.1016/j.canlet.2024.216644 |
| [23] |
Liang ZH, Ye YY, Deng ZH, et al. CHPF2 as a novel biomarker and ponicidin as a potential therapeutic agent in hepatocellular carcinoma[J]. Pharmacol Res, 2025, 215: 107698. DOI:10.1016/j.phrs.2025.107698 |
| [24] |
Jeong HY, Park SY, Kim HJ, et al. B3GNT5 is a novel marker correlated with stem-like phenotype and poor clinical outcome in human gliomas[J]. CNS Neurosci Ther, 2020, 26(11): 1147-1154. DOI:10.1111/cns.13439 |
| [25] |
Yao W, Wang YH, Zhang X, et al. B3GNT5 is a novel marker correlated with malignant phenotype and poor outcome in pancreatic cancer[J]. iScience, 2024, 27(10): 110889. DOI:10.1016/j.isci.2024.110889 |
| [26] |
Xue XL, Feng QL, Hong X, et al. Comprehensive analysis of ALG3 in pan-cancer and validation of ALG3 as an onco-immunological biomarker in breast cancer[J]. Aging (Albany NY), 2024, 16(3): 2320-2339. DOI:10.18632/aging.205483 |
| [27] |
Luo B, Liu XD, Zhang Q, et al. ALG3 predicts poor prognosis and increases resistance to anti-PD-1 therapy through modulating PD-L1 N-link glycosylation in TNBC[J]. Int Immunopharmacol, 2024, 140: 112875. DOI:10.1016/j.intimp.2024.112875 |
 2026, Vol. 25
2026, Vol. 25


