神经母细胞瘤(neuroblastoma, NB)是起源于交感神经系统的胚胎性肿瘤,其临床表现具有高度多样性,可从局限性病变发展至广泛转移的恶性进程[1]。目前,临床常规采用基于年龄、MYCN基因扩增状态以及国际神经母细胞瘤风险组(International Neuroblastoma Risk Group, INRG)分期等的风险分层,以指导治疗决策。然而,即便在同一风险组内,患儿预后仍然存在显著差异,部分患儿仍会出现疾病进展或复发[2-3]。既往研究证实,肿瘤的发生、发展与全身性炎症反应和患者营养状态密切相关。在肿瘤微环境中,凝血系统(特别是纤维蛋白原)可促使肿瘤进展与转移[4]。血清白蛋白水平降低常提示预后不良[5]。目前,基于炎症与营养指标的综合评估体系已被证实对多种实体瘤具有显著预后预测价值[6]。然而,纤维蛋白原与白蛋白比值(fibrinogen-to-albumin ratio, FAR)在儿童NB中的应用价值尚不明确。因此,本研究探索FAR与NB预后之间的关系,并构建基于FAR及其他临床因素的预后模型,为临床治疗决策及预后判断提供参考。
资料与方法 一、研究对象本研究为回顾性队列研究。收集2014年1月至2025年1月重庆医科大学附属儿童医院收治的283例NB患儿临床及病理资料。病例纳入标准:①经组织病理学检查确诊为NB;②年龄≤18岁;③接受规范治疗。排除标准:①临床资料不完整,初诊时纤维蛋白原或白蛋白数据缺失(无法计算FAR),缺失MYCN基因扩增状态、INRG分期或病理分型等关键预后变量,或随访数据缺失;②合并其他恶性肿瘤;③失访。本研究最终纳入279例患儿作为研究对象,按照7 ∶ 3比例采用随机数字表法分为训练集(n=195)和验证集(n=84)。本研究符合《赫尔辛基宣言》原则,研究方案经重庆医科大学附属儿童医院医学研究伦理委员会审查批准[(2024)年伦审(研)第(103)号]。因本研究为回顾性数据分析,且对患者隐私进行了严格保密,经伦理委员会批准豁免患儿监护人知情同意。
二、分析指标从电子病历系统中收集患儿临床资料、病理资料和实验室检查结果。其中,临床及病理资料包括性别、诊断时年龄、肿瘤大小、Shimada分型、INRG分期、危险度分层、MYCN扩增状态以及初诊时24 h尿香草扁桃酸(vanillylmandelic acid,VMA)水平;实验室检查指标包括初诊时纤维蛋白原、白蛋白、C反应蛋白、D-二聚体、神经元特异性烯醇化酶(neuron-specific enolase, NSE)及乳酸脱氢酶(lactate dehydrogenase, LDH)。FAR定义为纤维蛋白原与白蛋白浓度(g/L)比值。患儿术后通过门诊或电话随访,第1年每3个月随访1次,第2~3年每6个月随访1次,之后每年随访1次。总体生存期(overall survival, OS)定义为从确诊日期至由于各种原因死亡的日期或最后1次随访日期(2025年2月1日)。
三、统计学处理采用SPSS 25.0、R 4.3.3进行统计学分析。非正态分布的计量资料采用M(Q1, Q3)描述,组间比较采用独立样本秩和检验。采用受试者操作特征(receiver operator characteristic, ROC)曲线分析训练集数据,确定基线FAR的最佳截断值。采用卡方检验或Fisher精确概率法评估FAR与各临床、病理特征之间的关联性。采用单因素及多因素Cox比例风险回归模型筛选独立预后因素,构建FAR相关列线图模型及Kaplan-Meier曲线。采用双重模型验证策略:独立队列验证计算验证集的一致性指数(C-index),并绘制验证集的校准曲线和ROC曲线,评估模型对未参与建模数据的预测能力;训练集采用Bootstrap法重复抽样1 000次进行内部验证,计算校正后的C-index、校准度(校准曲线)。采用决策曲线分析(decision curve analysis, DCA)评估临床净收益,最后以模型总分进行风险分层,采用Kaplan-Meier法比较组间生存情况差异。P < 0.05为差异具有统计学意义。
结果 一、基线资料283例患儿中,临床资料不完整3例,失访1例,最终纳入279例患儿,其中男140例(50.2%)、女139例(49.8%);中位年龄29个月,中位随访时间55.1个月;INRG分期为M期164例(58.8%),MYCN扩增62例(22.2%)。
训练集(n=195)与验证集(n=84)的临床基线资料比较见表 1。除肿瘤类型(P=0.049)和肿瘤大小(P=0.037)差异有统计学意义外,年龄、性别、INRG分期、风险分组、MYCN状态等关键指标差异均无统计学意义(P>0.05),具有可比性。
| 表 1 279例神经母细胞瘤患儿临床基线资料[例(%)] Table 1 Baseline clinical profiles of 279 children with neuroblastoma[n(%)] |
|
|
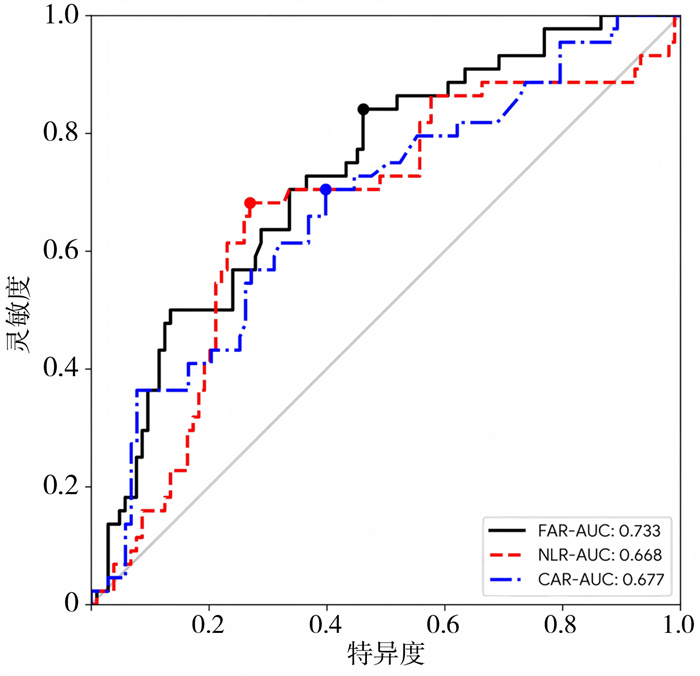
训练集FAR值的中位数为0.0692,均值为0.0883,范围为0.0136~0.5690。通过ROC曲线分析并计算OS的曲线下面积(area under the receiver operating characteristic curve, AUC),确定FAR的最佳截断值为0.0734(图 1),具体指标如下:AUC=0.733(该AUC值高于中性粒细胞与淋巴细胞比值和C反应蛋白与白蛋白比值),95%CI:0.714~0.826,P < 0.001,灵敏度78.2%,特异度78.7%。
|
图 1 神经母细胞瘤患儿纤维蛋白原与白蛋白比值及其他指标预测总生存期的受试者操作特征曲线比较 Fig.1 Comparison of receiver operating characteristic curves of fibrinogen-to-albumin ratio and other indicators for predicting overall survival in children with neuroblastoma 注 FAR:纤维蛋白原与白蛋白比值;NLR:中性粒细胞与淋巴细胞比值;CAR:C反应蛋白与白蛋白比值;AUC:受试者操作特征曲线下面积 |
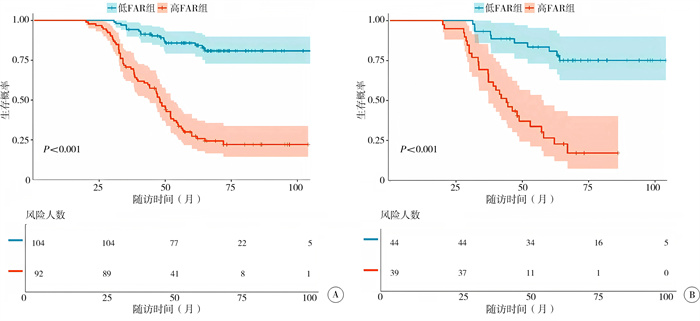
依据上述FAR截断值,将纳入的279例患儿分为高FAR组(FAR≥0.0734,n=130)和低FAR组(FAR < 0.0734,n=149)。如表 2所示,FAR与年龄、Shimada分型、MYCN扩展状态、INRG分期、危险度分组、CRP、白蛋白、纤维蛋白原和生存状态呈显著关联性,且不同FAR组别患儿的生存差异具有统计学意义(图 2)。
| 表 2 不同FAR风险分层神经母细胞瘤患儿临床特征比较 Table 2 Relationship between FAR risk stratification and independent variables in children with neuroblastoma |
|
|
|
图 2 不同FAR分层神经母细胞瘤患儿的生存曲线 Fig.2 Survival curves of children with neuroblastoma stratified by different FAR levels 注 A:训练集患儿生存曲线;B:验证集患儿生存曲线。曲线下方的表格为各随访时间点的风险人数(Number at risk);FAR:纤维蛋白原与白蛋白比值 |
单因素分析结果显示,年龄≥18个月、Shimada分型为uFH、INRG分期为M期、高危组、MYCN扩增、NSE异常、骨髓转移、淋巴结转移、LDH升高以及高FAR均与较差的OS相关(P < 0.05)。将上述单因素分析有统计学意义的变量纳入多因素Cox回归分析,结果显示,尽管Shimada分型、NSE异常、骨髓转移、LDH异常及淋巴结转移在单因素分析中与OS显著相关,但调整了FAR、年龄、INRG分期和MYCN状态等因素后,上述指标在多因素Cox模型中均无统计学意义(P值分别为0.2、0.2、0.9、0.4和0.4)。最终多因素Cox回归分析结果表明:高FAR(HR=2.58)、年龄≥18个月(HR=1.87)、INRG M期(HR=3.16)、MYCN扩增(HR=2.94)是NB患儿OS缩短的独立危险因素(P < 0.05)。见表 3。
| 表 3 279例神经母细胞瘤患儿单因素和多因素Cox比例风险回归分析结果 Table 3 Results of univariate and multivariate Cox proportional hazards regression analyses in 279 children with neuroblastoma |
|
|
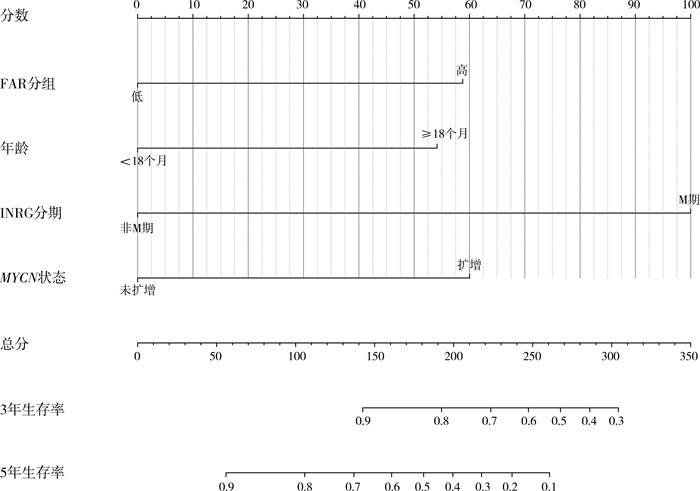
基于多因素分析筛选出4个独立预后因子(年龄、MYCN状态、INRG分期、FAR),构建了预测NB患儿术后3年和5年OS的列线图模型, 见图 3。
|
图 3 纤维蛋白原/白蛋白比值预测神经母细胞瘤患儿总体生存期的列线图 Fig.3 Nomogram based upon fibrinogen-to-albumin ratio for predicting overall survival in children with neuroblastoma 注 该模型中各变量根据回归系数被赋予相应分值,将各变量得分相加得到总分,即可在总分轴向下对应查得患儿3年及5年生存概率; FAR: 纤维蛋白原与白蛋白比值;INRG:国际神经母细胞瘤风险组 |
为评估FAR在特定临床特征人群中的适用性,本研究在具有完整关键协变量及明确干预信息的亚队列(n=148)中,根据年龄、INRG分期及MYCN扩增状态进行亚组分析(表 4)。结果显示,FAR在关键亚组中具有显著的风险区分能力,在年龄≥18个月的患儿中,高FAR是总体生存期缩短的独立危险因素(HR=2.74, 95%CI: 1.29~5.84, P < 0.05)。值得注意的是,在MYCN未扩增的亚组中,FAR显示出极强的预后预测效能(本研究有5例因MYCN基因处于临界扩增获得状态,为避免混杂因素干扰被排除在MYCN分层分析之外),高FAR患儿的死亡风险显著升高(HR=4.47, 95%CI: 1.22~16.41, P < 0.05)。此外,在INRG分期M期的亚组中,未发现FAR与预后之间存在具有统计学意义的相关性(HR=1.16, 95%CI: 0.52~2.60, P=0.722)。
| 表 4 不同亚组神经母细胞瘤患儿术前FAR与总体生存期的关联分析 Table 4 Subgroup analysis of the association between preoperative FAR and overall survival in children with neuroblastoma |
|
|
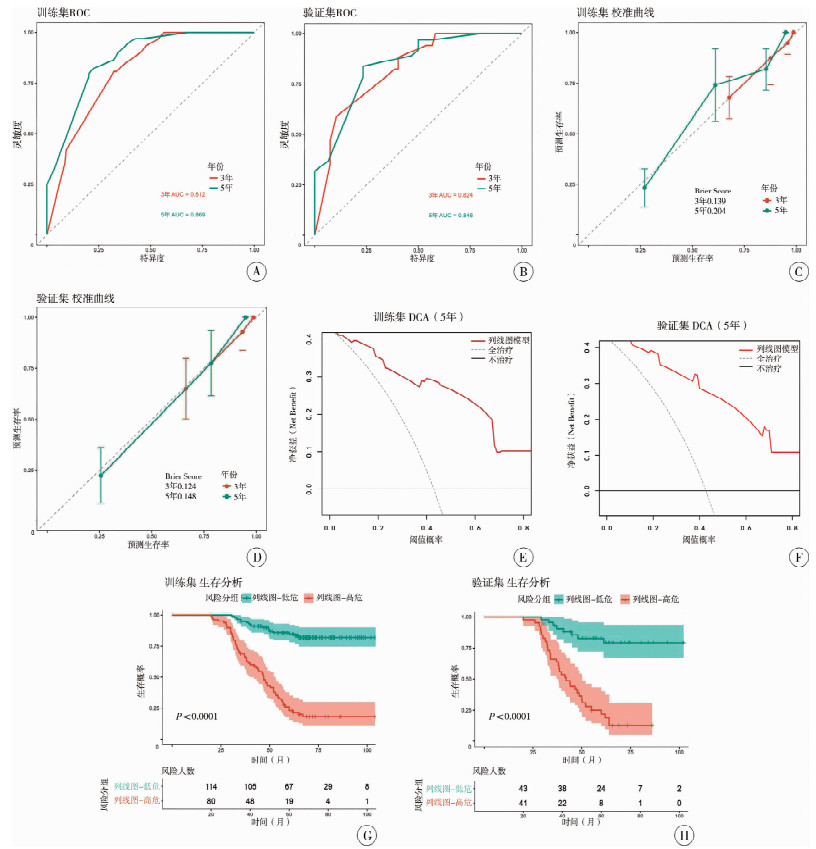
训练集中,该列线图模型的C-index为0.790,经Bootstrap内部验证校正后的C-index为0.782,训练集模型预测3年、5年OS的AUC分别为0.812、0.869;验证集模型预测3年、5年OS的AUC分别为0.824、0.846(图 4A、4B),其区分能力优于单一指标。
|
图 4 列线图预测模型对于神经母细胞瘤训练集和验证集患儿的综合评估情况 Fig.4 Comprehensive evaluations of nomogram prediction model for children with neuroblastoma in training and validation cohorts 注 A、B:训练集(A)和验证集(B)中用于预测3年和5年总体生存率的受试者操作特征曲线;C、D:训练集(C)和验证集(D)3年和5年生存率的校准曲线及Brier评分;E、F:训练集(E)和验证集(F)中预测5年生存率的决策曲线分析;G、H:训练集(G)和验证集(H)的Kaplan-Meier生存分析曲线 |
采用Bootstrap法对数据进行1 000次重复自抽样,并绘制预测模型的校准曲线,以比较3年、5年的预测生存概率与实际观测概率。如图 4C、4D所示,NB患儿术后3年、5年预后预测模型的校准曲线与理想曲线(对角线)拟合度较高。此外,训练集3年及5年的Brier评分(Brier score)分别为0.124和0.148;验证集3年及5年的Brier评分分别为0.139、0.204。较低的Brier评分进一步从量化角度证实,模型的预测生存概率与实际观测概率之间具有较好的一致性,提示模型具有良好的预测效能。
DCA结果表明,本研究构建的NB患儿预后预测列线图模型,在广泛的阈值概率范围内呈现显著正向净获益,提示该模型在NB患儿预后预测、指导早期治疗方面具有较高的临床实用性(图 4E、4F)。根据本列线图预测模型的截断值(193.4分),将患儿分为高风险组(n=163,58.42%)和低风险组(n=116,41.58%),在基于列线图评分划分的不同风险组之间,生存曲线差异具有统计学意义(P<0.001,图 4G、4H)。
讨论本研究将FAR引入儿童NB预后评估体系,结合年龄、MYCN扩增状态及INRG分期构建列线图模型。FAR作为反映全身炎症与营养状态的复合指标,具有良好的客观性、易得性与经济性,适合临床推广。该模型内部验证显示出较好的预测性能与临床实用性,有望为NB患儿的个体化治疗提供量化工具。
本研究评估了FAR对NB的预后预测价值,结果表明,初诊时高FAR(≥0.0734)是NB患儿总生存期缩短的独立危险因素。基于此,我们整合了年龄、INRG分期M期、MYCN状态及FAR这4个相对易获取的指标,构建了预测3年及5年OS的列线图模型。内部验证显示,该模型具有良好的区分度(C-index=0.782)与校准度,且决策曲线分析证实其具有广泛的临床净获益。不同临床亚组分层分析结果显示,FAR在MYCN扩增及未扩增亚组、年龄大于18个月的患儿中均保持了显著的独立预后价值,提示该指标具有较好的适用性。尽管该指标在M期患儿中区分度有限,但在非M期患儿中展现出极高的风险识别能力,这为NB患儿的个体化预后评估提供了一个客观、经济且实用的新工具。
FAR作为一种复合指标,其预后价值具有明确的生物学基础。一方面,纤维蛋白原作为重要的急性期反应蛋白,其水平升高不仅反映全身炎症状态,还直接参与肿瘤进展的多个关键环节。研究表明,在胶质母细胞瘤等实体瘤中,纤维蛋白原可显著促进肿瘤局部浸润[7]。纤维蛋白原及其降解产物(如纤维蛋白E片段)可直接刺激血管内皮细胞增殖、迁移与管腔形成,并与VEGF、bFGF等生长因子协同促进肿瘤血管生成[8]。在全身性转移过程中,纤维蛋白原通过形成纤维蛋白基质屏障,保护循环肿瘤细胞免受自然杀伤细胞清除,并促进其在远处器官定植[9]。此外,纤维蛋白原还与肿瘤相关高凝状态密切相关,其通过抑制蛋白C抗凝途径,促进血栓形成,为转移细胞提供“避难所”并促进转移前生态位形成[10]。另一方面,血清白蛋白水平降低通常预示着癌症相关的恶病质、免疫功能抑制及治疗耐受性下降[11]。而肿瘤微环境释放的促炎细胞因子(如白细胞介素-6)可导致血清白蛋白水平显著下降。高FAR值不仅综合反映了纤维蛋白原介导的肿瘤侵袭、血管生成及免疫逃逸等恶性进展行为,更揭示了低白蛋白水平所隐含的宿主系统性炎症负荷、营养恶病质及生理防御储备的衰竭。这种同时具备反映“肿瘤攻击性增强”与“机体防御力崩塌”的双重病理状态特性,使FAR相较于单一指标更能稳健地预测疾病的不良预后。
FAR的预测意义基于NB起源于交感神经系统的生物学特性,而非单纯的非特异性炎症反应。首先,低白蛋白反映NB特有的儿茶酚胺驱动型高代谢状态,NB瘤体分泌的儿茶酚胺导致机体基础代谢率激增,加速蛋白质分解;加之胚胎性肿瘤的极速增殖掠夺,致使患儿迅速出现恶病质。其次,高纤维蛋白原与NB的“嗜骨髓”转移及免疫逃逸相关。纤维蛋白原作为支架蛋白,不仅协助循环肿瘤细胞聚集成团,抵抗血流剪切力并定植于骨髓(NB最常见的致死性转移部位),还构筑物理屏障阻碍免疫细胞浸润,维持NB的典型“冷肿瘤”微环境。因此,高FAR可以敏锐捕捉到NB患儿高代谢消耗与高转移风险的双重病理状态。
近年来,随着分子生物学和影像技术的进步,针对NB预后评估的研究正朝着微观化和多模态化发展。如Mondal等[12]研究揭示,超级增强子驱动的长链非编码RNA(lncRNA)PRKCQ-AS1可通过与MSI2蛋白相互作用促进NB的发生,是潜在的治疗靶点和预后因子;Jahangiri等[13]系统阐述了外泌体(exosomes)作为液体活检标志物在反映肿瘤微环境和治疗耐药方面的潜力;亦有研究分析了RAS-MAPK通路突变在复发性NB中的临床意义[14]。
与上述高精尖的分子或影像标志物相比,本研究提出的FAR在机制特异性上虽不如基因或外泌体深入,但在临床转化和卫生经济学方面具有不可替代的创新优势。本研究所构建的列线图模型纳入了4个指标共同构成了一个多维度的预后评估框架[15]。其中,年龄≥18个月与MYCN扩增是NB经典的、反映肿瘤内在侵袭性的生物学标志[16-17];INRG分期M期则直观体现了疾病的肿瘤负荷与扩散程度。而FAR的加入,将反映全身炎症与营养状态的“宿主因素”系统性纳入该疾病的预后模型。这四大要素分别从“宿主状态”、“肿瘤生物学”及“疾病程度”3个层面提供了互补的预后信息,从而保证模型的综合预测效能。内部验证显示,该模型在3年及5年时间点的AUC值均高于0.82,校准曲线贴近理想对角线,表明其预测准确性良好。更重要的是,基于模型总分的风险分层能够将患儿清晰地划分为生存差异显著的高危与低危组(P < 0.001),这为临床识别需要强化治疗与密切随访的高风险群体提供了直接的量化依据。
目前,尽管INRG分期系统、Shimada分型等传统指标已广泛应用于NB的风险分层,但其在同一风险组内对预后异质性的鉴别能力尚有限[18]。近年来,一些反映系统性炎症的指标,如中性粒细胞与淋巴细胞比值也开始被探索[19]。然而,FAR的优势在于其同时整合了凝血与营养两个系统,信息维度更为全面。本研究结果与FAR在肝细胞癌、胃癌等成人实体瘤中的预后价值相符[20-21]。将这一标志物拓展至儿童NB领域,是一项重要的补充与创新。亚组分析结果进一步明确了FAR的最佳临床应用场景。既往研究公认MYCN扩增是预后不良的强驱动因子,但对于MYCN未扩增患儿,临床往往缺乏简便的指标来进一步细分风险。本研究发现,FAR在MYCN未扩增亚组中的HR高达4.47,提示对于缺乏这一关键分子标志物的患儿,FAR可作为一种强有力的补充工具来识别潜在的高危个体。同时,在年龄≥18个月的患儿中,FAR同样保持了显著的预测价值。值得注意的是,在INRG分期M期亚组中,FAR不具有统计学意义(P=0.722)。这可能与晚期肿瘤本身极差的预后主导了生存结局,在一定程度上掩盖了炎症-营养指标的预后权重有关,也可能受限于该亚组的样本量。尽管如此,FAR在非M期或整体人群中的稳健表现,仍支持其作为现有分期系统的有效补充。
本研究存在一定局限性。首先,这是一项单中心回顾性研究,样本量有限,受限于回顾性数据采集的局限性,本研究缺乏完整的PFS数据,仅分析了FAR对OS的预测价值,且随访时间不足以评估更长期的生存结局。其次,本研究数据收集时间长达11年(2014—2025年),尽管在此期间,本中心始终由固定的高年资小儿肿瘤外科团队手术,并严格遵循中国抗癌协会小儿肿瘤专业委员会(Chinese Children's Cancer Group,CCCG)及INRG的诊疗规范进行标准化管理,以最大程度确保治疗策略的一致性,然而,长周期内不可避免的医疗技术进步(如支持治疗、微创手术设备更新)以及不同时期具体化疗药物的微调,仍可能导致一定的治疗异质性偏倚。这种时间跨度带来的潜在影响难以通过回顾性分析完全消除。此外,模型仅通过了Bootstrap和内部验证集验证,其普适性仍需通过多中心、前瞻性的外部独立队列进一步验证。最后,FAR值为初诊单次测量,未能动态监测其在治疗过程中的变化及其与治疗反应之间的相关性,未来可开展前瞻性研究动态监测治疗过程中FAR的变化,并纳入PFS等更多终点指标,以进一步验证该模型的普适性及其与治疗反应的相关性。
综上所述,初诊FAR是儿童NB的一个独立、易得且经济的预后评估生物标志物。基于FAR、年龄、MYCN状态及INRG分期M期构建的列线图模型,能有效预测患儿的个体化生存概率,实现精准的风险分层,有望辅助临床医师制定更合理的治疗与随访策略,具有显著的临床转化潜力。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 杨超负责实验设计、研究指导、论文审阅;习成军负责数据整理、文章撰写、数据统计分析、作图
| [1] |
Jia X, Wang WQ, Liang JW, et al. Application of amide proton transfer imaging to pretreatment risk stratification of childhood neuroblastoma: comparison with neuron-specific enolase[J]. Quant Imaging Med Surg, 2023, 13(5): 3001-3012. DOI:10.21037/qims-22-780 |
| [2] |
Zheng L, Li C, Yang X, et al. GD2-targeted theranostics of neuroblastoma with[64Cu]Cu/[77Lu]Lu-hu3F8[J]. Eur J Nucl Med Mol Imaging, 2025, 52(5): 1764-1777. DOI:10.1007/s00259-024-07033-w |
| [3] |
王鹏程, 董瑞. 神经母细胞瘤4S期预后不良相关因素的研究进展[J]. 临床小儿外科杂志, 2022, 21(4): 394-398. Wang PC, Dong R. Research advances on poor prognostic factors of children with stage 4S neuroblastoma[J]. J Clin Ped Sur, 2022, 21(4): 394-398. DOI:10.3760/cma.j.cn101785-202108053-019 |
| [4] |
Jafri SHR, Previgliano C, Khandelwal K, et al. Cachexia index in advanced non-small-cell lung cancer patients[J]. Clin Med Insights Oncol, 2015, 9: 87-93. DOI:10.4137/CMO.S30891 |
| [5] |
Li Q, Ma F, Tsilimigras DI, et al. The value of the Advanced Lung Cancer Inflammation Index (ALI) in assessing the prognosis of patients with hepatocellular carcinoma treated with camrelizumab: a retrospective cohort study[J]. Ann Transl Med, 2022, 10(22): 1233. DOI:10.21037/atm-22-5099 |
| [6] |
Fang JM, Liang H, Lu SL, et al. Association of preoperative high C-reactive protein to albumin ratio with adverse outcomes after elective non-cardiac surgery in older patients: a multicenter prospective study[J]. J Inflamm Res, 2024, 17: 9255-9268. DOI:10.2147/JIR.S492568 |
| [7] |
Bootle-Wilbraham CA, Tazzyman S, Thompson WD, et al. Fibrin fragment E stimulates the proliferation, migration and differentiation of human microvascular endothelial cells in vitro[J]. Angiogenesis, 2001, 4(4): 269-275. DOI:10.1023/a:1016076121918 |
| [8] |
Palumbo JS, Talmage KE, Massari JV, et al. Platelets and fibrin (ogen) increase metastatic potential by impeding natural killer cell-mediated elimination of tumor cells[J]. Blood, 2005, 105(1): 178-185. DOI:10.1182/blood-2004-06-2272 |
| [9] |
Akita N, Ma N, Okamoto T, et al. Host protein C inhibitor inhibits tumor growth, but promotes tumor metastasis, which is closely correlated with hypercoagulability[J]. Thromb Res, 2015, 135(6): 1203-1208. DOI:10.1016/j.thromres.2015.03.026 |
| [10] |
Li XH, Zeng MR, Liu JL, et al. Identifying potential biomarkers for the diagnosis and treatment of IgA nephropathy based on bioinformatics analysis[J]. BMC Med Genomics, 2023, 16(1): 63. DOI:10.1186/s12920-023-01494-y |
| [11] |
Wang R, Zeng HH, Shi MT, et al. Dynamic variations in peripheral blood indices and their association with efficacy and adverse reactions of PD-1 inhibitor combined chemotherapy in patients with advanced gastric cancer[J]. BMC Gastroenterol, 2025, 25(1): 264. DOI:10.1186/s12876-025-03883-2 |
| [12] |
Mondal S, Liu PY, Seneviratne J, et al. The super enhancer-driven long noncoding RNA PRKCQ-AS1 promotes neuroblastoma tumorigenesis by interacting with MSI2 protein and is targetable by small molecule compounds[J]. Adv Sci (Weinh), 2025, 12(18): e2412520. DOI:10.1002/advs.202412520 |
| [13] |
Jahangiri L, Ishola T. Exosomes in neuroblastoma biology, diagnosis, and treatment[J]. Life (Basel), 2022, 12(11): 1714. DOI:10.3390/life12111714 |
| [14] |
Mlakar V, Morel E, Mlakar SJ, et al. A review of the biological and clinical implications of RAS-MAPK pathway alterations in neuroblastoma[J]. J Exp Clin Cancer Res, 2021, 40(1): 189. DOI:10.1186/s13046-021-01967-x |
| [15] |
陈伟明, 白建喜, 张炳, 等. 神经母细胞瘤患儿生存预测模型的构建和验证[J]. 临床小儿外科杂志, 2025, 24(3): 243-249. Chen WM, Bai JX, Zhang B, et al. Establishment and validation of a survival prediction model for children with neuroblastoma[J]. J Clin Ped Sur, 2025, 24(3): 243-249. DOI:10.3760/cma.j.cn101785-202207009-008 |
| [16] |
Tangella AV, Gajre AS, Chirumamilla PC, et al. Difluoromethylor-nithine (DFMO) and neuroblastoma: a review[J]. Cureus, 2023, 15(4): e37680. DOI:10.7759/cureus.37680 |
| [17] |
Orlandini LF, Pimentel FF, de Andrade JM, et al. Obesity and high neutrophil-to-lymphocyte ratio are prognostic factors in non-metastatic breast cancer patients[J]. Braz J Med Biol Res, 2021, 54(10): e11409. DOI:10.1590/1414-431X2021e11409 |
| [18] |
Deng C, Zhang SJ, Ling J, et al. Prognostic value of the fibrinogen albumin ratio index (FARI) in nasopharyngeal carcinoma patients undergoing radiotherapy[J]. Sci Rep, 2023, 13(1): 20630. DOI:10.1038/s41598-023-48029-0 |
| [19] |
Wang SS, Feng YH, Xie YC, et al. High fibrinogen-albumin ratio index (FARI) predicts poor survival in head and neck squamous cell carcinoma patients treated with surgical resection[J]. Eur Arch Otorhinolaryngol, 2022, 279(9): 4541-4548. DOI:10.1007/s00405-022-07391-x |
| [20] |
Liu H, Qiu GT, Hu FJ, et al. Fibrinogen/albumin ratio index is an independent predictor of recurrence-free survival in patients with intrahepatic cholangiocarcinoma following surgical resection[J]. World J Surg Oncol, 2021, 19(1): 218. DOI:10.1186/s12957-021-02330-2 |
| [21] |
Cao X, Cui J, Yu T, et al. Fibrinogen/albumin ratio index is an independent prognosis predictor of recurrence-free survival in patients after surgical resection of gastrointestinal stromal tumors[J]. Front Oncol, 2020, 10: 1459. DOI:10.3389/fonc.2020.01459 |
 2026, Vol. 25
2026, Vol. 25


