神经母细胞瘤(neuroblastoma, NB)是婴幼儿最常见的颅外实体瘤,其临床表现具有高度异质性,部分低危肿瘤可自发消退,部分高危病例接受强化治疗后预后仍不理想[1]。目前临床风险分层主要依赖诊断年龄、国际神经母细胞瘤分期系统(International Neuroblastoma Staging System, INSS)分期、组织学分型以及MYCN扩增状态[2]。即使相同危险度患儿其预后仍然存在显著差异,提示现有临床指标无法完全揭示NB的复杂生物学本质。
蛋白质是生命功能的直接执行者,其表达、修饰及相互作用网络直接决定了肿瘤的生物学行为。近年来,高通量蛋白质组学技术的发展为解析肿瘤分子特征提供了新的视角。基因组和转录组研究已揭示NB的部分关键驱动因素,但蛋白质水平的改变往往与基因表达水平不完全同步,尤其在翻译后修饰调控及代谢重组方面存在显著差异[3]。因此,从蛋白质层面系统刻画NB的分子特征,对于完善其风险分层、发现新型生物标志物及治疗靶点具有重要意义。本研究对150例NB肿瘤组织进行深度定量蛋白质组学分析,通过聚类分析解析不同临床风险等级及原发部位的分子差异,鉴定出一批关键预后相关蛋白及通路。进一步采用无监督聚类方法定义4种具有独特生物学特征的蛋白质组亚型(PAM 1~4),并重点揭示高危亚型PAM4对脂肪酸氧化(fatty acid oxidation, FAO)和线粒体代谢的依赖性,旨在为NB的分子分型提供蛋白质组学证据,并为高危患者的精准治疗提供潜在新靶点。
资料与方法 一、研究对象与样本本研究为回顾性队列研究,并结合体外实验验证。选取2012年10月至2015年2月在上海交通大学医学院附属新华医院小儿外科接受手术治疗的NB患儿作为研究对象。疾病诊断经3名病理科医师独立完成并符合国际神经母细胞瘤病理学分类标准,肿瘤分期依据INSS分期标准判定。患儿均接受常规随访,随访终点为死亡或末次随访日期。本研究通过上海交通大学医学院附属新华医院临床研究伦理委员会审核批准(XHEC — C — 2017 — 210),患儿监护人均知情并签署知情同意书。
二、细胞培养与材料人NB细胞系购自中国科学院干细胞库。细胞株使用含10%胎牛血清(Fetal Bovine Serum,FBS)的RPMI 1640培养基,于37℃、含5% CO2的恒温加湿培养箱中常规培养。采用CCK8试剂盒在规定时间点内测量450 nm吸光度,评估细胞增殖。
三、液相色谱-质谱联用(LC-MS/MS)分析采用尿素裂解法提取组织内总蛋白,随后按常规方法进行胰蛋白酶消化。细胞裂解液经5 mM二硫苏糖醇55℃还原30 min,再经15 mM碘乙酰胺室温下避光烷基化30 min。随后按1 ∶ 100(酶/底物,w/w)比例加入胰蛋白酶,于37℃过夜消化。利用高pH反相液相色谱进行分离,收集60个组分并合并为10个。每个组分溶解于溶剂(0.1%甲酸,2%乙腈)后,通过Q ExactiveTM Plus质谱仪进行分析。使用Maxquant和Perseus软件进行蛋白质鉴定、定量及统计分析。
四、统计学处理使用R语言和GraphPad Prism 5进行数据分析;实验数据以x±s表示;根据实验设计采用单侧或双侧配对Student's t检验或Mann-Whitney检验进行分析;生存曲线采用Kaplan-Meier法及Log-rank检验评估差异;P < 0.05为具有统计学意义。通路富集分析使用R语言的clusterProfiler包完成。多变量Cox比例风险回归模型校正年龄、INSS分期、MYCN扩增状态等混杂因素,完成蛋白质组学亚型独立预后价值的评估,通路富集分析采用Benjamini-Hochberg方法完成多重假设检验校正,筛选阈值设定为错误发现率(false discovery rate,FDR)小于0.05。为保证分型稳定性,研究选用一致性聚类算法,重抽样次数设置为1 000次,采样比例设定为80%,评估一致性累积分布函数和Delta Area曲线后,最终确定最佳聚类数k=4,该聚类数下簇间一致性最高,簇内变异最小。
结果 一、基于危险度水平的蛋白质组学监督聚类分析本研究共纳入150例NB患儿。如表 1所示,该队列在性别分布上较为均衡(男78例,女72例)。约30.7%的患儿诊断时年龄小于18个月,低危组63例、中危组45例、高危组42例。10例检出MYCN扩增。肾上腺来源100例,非肾上腺来源50例。
| 表 1 神经母细胞瘤临床风险度分层研究队列临床特征 Table 1 Clinical characteristics of aneuroblastoma cohort for risk stratification |
|
|
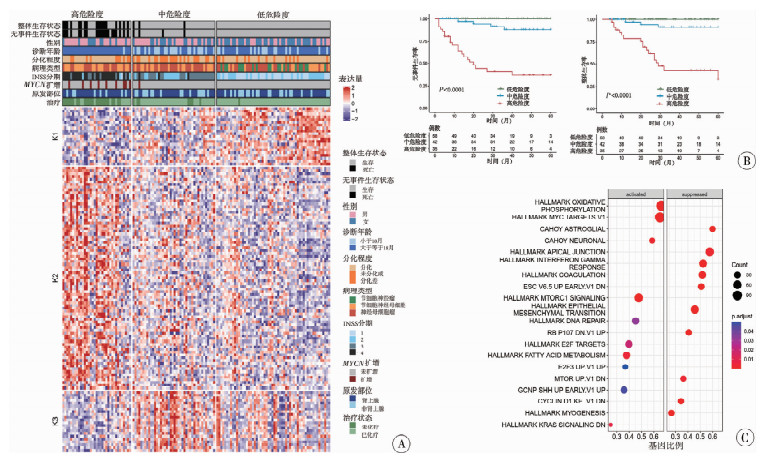
为了探究不同临床风险等级之间的分子差异,我们对高、中、低危组进行了监督聚类分析(图 1A)。蛋白质表达热图将样本清晰分为K1、K2、K3三个主要蛋白质表达谱簇。K1簇内部,高危组存在特异性蛋白上调,低危组样本多集中在K3簇,显示蛋白质组表达谱与临床风险分层具有较高的相似性。生存曲线提示,3个风险组在总体生存率(overall survival,OS)和无事件生存率(event-free survival,EFS)上差异具有统计学意义(P < 0.0001)。高危组5年生存率显著低于中、低危组,鉴于高危组极差的生存预后,本研究进一步将样本按照预后差和预后好进行深度挖掘(图 1B)。通过对预后好与预后差的两组进行信号通路富集分析发现(图 1C),预后较差的亚组中,氧化磷酸化、MYC靶点、E2F靶点、DNA修复相关通路维持激活状态,高危且预后差的NB拥有更高的代谢活性和增殖潜能,预后较差组上皮间质转化、凝血、肌生成以及KRAS信号通路的表达水平更低,这类现象对应低风险肿瘤的分化特征,也对应肿瘤微环境的不同调控方式。
|
图 1 神经母细胞瘤临床风险分层相关蛋白质组学图谱 Fig.1 Proteomic landscape associated with clinical risk stratification in neuroblastoma 注 A: 根据危险度进行差异表达蛋白的监督聚类热图,揭示与临床风险等级高度对应的3个蛋白质组簇(K1、K2、K3); B: 3个风险组的总生存期和无事件生存期Kaplan-Meier曲线(Log-rank检验,P < 0.0001); C: 通路富集分析显示,预后差组显著富集氧化磷酸化和MYC靶点,预后好组富集EMT通路 |
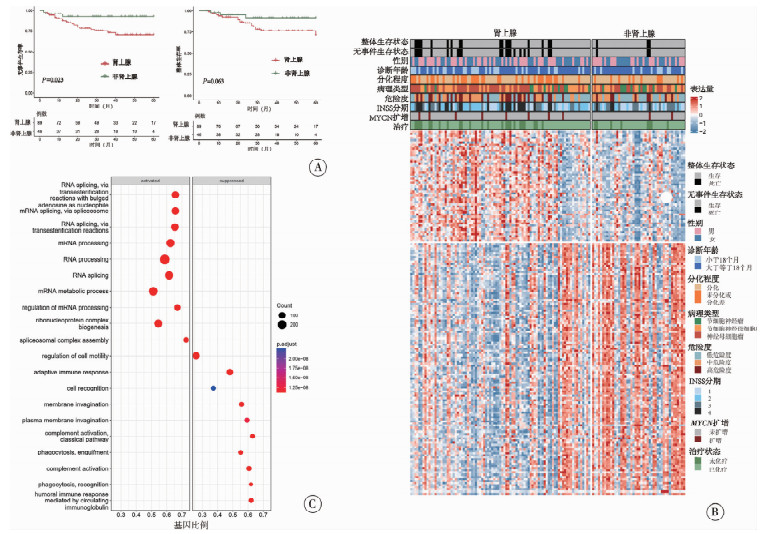
本研究结果显示,肿瘤原发于肾上腺的患儿生存率更低;生存分析进一步证实(图 2A),原发于肾上腺组无事件生存率和总体生存率均低于非肾上腺组,原发部位会影响NB预后,是这类疾病重要的生物学因素,探究不同原发部位NB的分子差异时,本研究依照肿瘤来源,把样本分为肾上腺来源和非肾上腺来源两类,对蛋白质组数据进行监督聚类分析。结果显示(图 2B),肾上腺来源的肿瘤显著富集于分化程度较低的病理类型、高危组以及临床分期较晚(INSS 4期)的患者;相比之下,非肾上腺来源的肿瘤则更多见于分化程度较高的节细胞神经瘤、中低危组及3期患者。随后,对样本进行监督聚类分析发现,两组在蛋白质表达水平上呈现截然不同的特征。为了明确差异蛋白介导的生物学功能,本研究进行了GSEA(Hallmark)和GO通路富集分析(图 2C):肾上腺组显著富集于MYC靶点、G2M检查点、氧化磷酸化、DNA修复及HEME代谢等通路,这些通路的高度激活通常与细胞快速增殖、代谢重组及高侵袭性密切相关。非肾上腺组则主要富集于上皮- 间质转化、凝血功能、骨骼肌发育以及顶端连接等通路。此外,GO分析显示该组与免疫激活(如补体激活、体液免疫)及细胞识别相关,提示该组肿瘤可能具有更强的分化倾向和更活跃的微环境免疫反应。
|
图 2 肾上腺与非肾上腺来源神经母细胞瘤的肿瘤独特分子特征 Fig.2 Distinct molecular signatures of adrenal and non-adrenal primary tumors 注 A-B:原发部位与临床特征的相关性分析显示,肾上腺来源与高危、晚期及未分化组织学相关;C:GSEA富集分析显示,肾上腺肿瘤(左)以MYC靶点、氧化磷酸化及胚胎发育蛋白上调为特征(去分化状态),非肾上腺肿瘤(右)显示显著的免疫激活及细胞分化特征 |
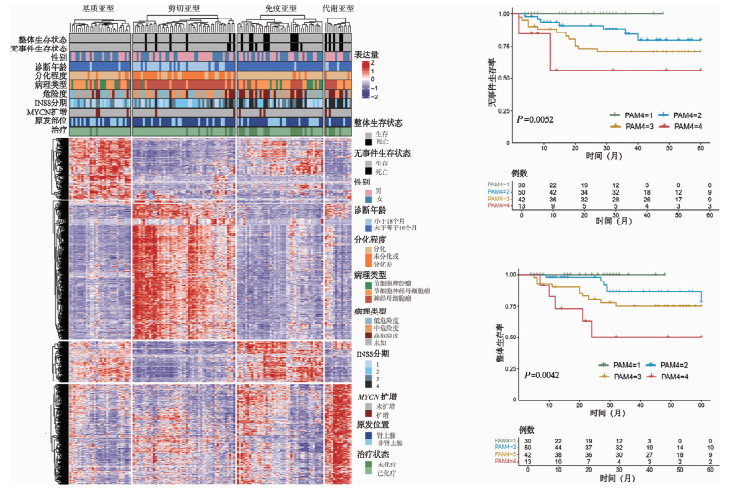
对全样本集进行无监督聚类分析,在蛋白质组水平上绘制NB的分子景观图。首先将年龄、INSS分期及MYCN扩增状态作为协变量纳入分析,多因素Cox回归分析显示,在校正了年龄、INSS分期及MYCN扩增后,PAM4亚型仍然是独立不良预后因素(HR=3.25, 95%CI: 1.5~6.8, P<0.05),说明该分子分型拥有超越传统临床指标的额外预后评估价值。基于无监督聚类分析,可见样本清晰地划分为4个各具特征的蛋白质组亚型(PAM1~PAM4)(图 3)。随后进行临床特征关联分析,发现这4个亚型与患儿预后及临床表型高度相关。PAM1(低危/基质型):表现出极佳的临床预后,无事件生存率和总体生存率较高,该亚型主要由大年龄诊断、高分化、低分期(INSS 1期、2期)、未接受化疗及非肾上腺来源的患儿组成。PAM2(中危/剪切型):预后相对较好,特征为诊断年龄较小、病理分化程度低但MYCN不扩增,且主要为肾上腺来源。PAM3(高危/免疫型):具有较高的复发和死亡风险,主要富集高危组、分期较高(INSS 3期、4期)且接受了强化化疗的节细胞神经母细胞瘤患儿。PAM4(极高危/代谢型):临床结局最差,病理分化呈高度恶性状态,病灶原发于肾上腺概率更高。生存曲线进一步证实,PAM3和PAM4患儿生存率显著低于PAM1和PAM2。对4个亚型分别进行差异表达蛋白筛选以及GSEA功能富集分析,各亚型特征如下:①PAM1-基质亚型,显著富集细胞外基质组装、胶原合成及细胞粘附相关蛋白,提示该亚型具有较高的间质组分。②PAM2-剪切亚型,核心特征为RNA剪接、核糖体生物合成及mRNA加工通路高度激活。③PAM3-免疫亚型,表现出强烈的免疫响应信号,包括抗原提呈及淋巴细胞激活。④PAM4-代谢亚型,能量代谢极度活跃,显著富集氧化磷酸化、TCA循环以及脂肪酸代谢通路(NES>1.5, FDR < 0.05)。PAM4亚型预后最差,富集分析发现代谢通路显著激活,推测其生存高度依赖于特定的能量代谢途径。利用不同代谢通路抑制剂处理6株NB细胞系(表 2),结果显示阻断糖酵解(2-脱氧-D-葡萄糖,2-DG)或阻断谷氨酰胺分解时(Telaglenastat,CB839),NB细胞状态变化较小,加入脂肪酸氧化抑制剂Etomoxir后,细胞反应更强,肿瘤细胞存活率下降,线粒体解偶联剂(碳酰氰-4-三氟甲氧基苯腙,FCCP)实验证实该类细胞对线粒体电子传递链高度依赖,印证了蛋白质组学中氧化磷酸化通路激活的结果。
|
图 3 150例神经母细胞瘤样本的非监督聚类分析热图 Fig.3 Unsupervised clustering heatmap of 150 neuroblastoma samples |
| 表 2 不同代谢通路抑制剂处理神经母细胞瘤细胞株药物IC50 Table 2 IC50 values of the drug in neuroblastoma cell lines treated with different metabolic pathway inhibitors |
|
|
NB临床特征存在较高异质性,病程可从自发性消退延伸至快速进展的不同阶段,传统临床分层可指导治疗方案选择,相关作用已有明确共识[4]。但其在揭示肿瘤深层生物学差异和寻找新型代谢靶点方面存在局限。本研究收集150例NB患儿肿瘤组织样本,进行蛋白质组学深度测序分析,系统描绘了NB的蛋白质组学景观。研究结果验证了传统风险分层的分子基础,发现了原发部位肿瘤的生物学差异,在分子分型方面提出了创新性见解。
本研究发现,蛋白质表达谱(K1~K3簇)能够精确复现现有的风险分层体系。在高危/预后差的样本中,观察到E2F靶点和DNA修复通路的显著激活,这与Pugh等[5]关于高危NB基因组不稳定性的研究结果相互印证。相比之下,低危组表现出更强的上皮-间质转化,这可能反映了肿瘤分化程度较高、恶性程度较低的生物学状态。
通过对肾上腺来源和非肾上腺来源的肿瘤标本分析发现,肾上腺来源肿瘤表现出更强的胚胎发育特征和更差的预后。肾上腺来源肿瘤不仅富集了MYC信号和氧化磷酸化通路,还显著表达与神经发育障碍相关的胚胎性蛋白。通路分析结果提示,肾上腺来源的肿瘤可能保留了更多的胚胎发育特征。根据Dong等[6]的单细胞发育图谱研究,NB可能起源于发育早期的交感神经前体细胞,而肾上腺环境可能进一步诱导其去分化状态,这种去分化状态与不良预后的关联,尚需结合发育生物学谱系追踪技术进行进一步的验证。
在对组织样本的无监督聚类分析中,笔者进一步通过分子表达谱对NB进行了蛋白质组亚型模型的构建,这一模型较传统的临床分级更精细地刻画了肿瘤的生物学特征。PAM1富集细胞外基质蛋白,预后极佳。这验证了Blavier等[7]的观点,即肿瘤基质成分在抑制神经母细胞恶性转化中起到了关键的物理支撑和生化诱导作用。PAM3免疫分型尽管具有明显的淋巴细胞浸润,但仍存在较高的死亡风险。这可能归因于NB的典型免疫逃逸机制,如Brady等[8]所描述的MHC-Ⅰ类分子表达缺失,导致T细胞虽有浸润但无法发挥有效的杀伤作用。这与Wienke等[9]关于NB免疫景观的分析相吻合。最具有临床意义的是PAM4(代谢型)亚型。该亚型预后最差,其蛋白质谱显示出极度活跃的氧化磷酸化和脂肪酸代谢特征。实验证实此类NB细胞株对脂肪酸氧化抑制剂Etomoxir表现出特异性敏感。对于部分极高危患者,针对线粒体能量代谢的靶向策略(如抑制线粒体转运或脂肪酸氧化)可能较传统的细胞毒性化疗更具潜力。Arif等[10]、龙俊汕[11]曾指出VDAC1是线粒体代谢和凋亡的关键闸门,是极具潜力的肿瘤治疗靶点。实验证实,抑制脂肪酸氧化(Etomoxir)能显著抑制NB细胞活力。这与Bansal等[12]的观点一致,高危NB可能通过代谢重编程来维持高氧化应激下的生存。
本研究尚存在一定的局限性。首先,虽然本研究通过Etomoxir和FCCP处理验证了NB细胞株对脂肪酸氧化及线粒体功能的依赖,但所有验证实验均在体外细胞系中完成,缺乏体内动物模型(如PDX模型)的药效学数据。其次,虽然蛋白质组学揭示了潜在靶点,但具体的分子调控机制仍需进一步解析。未来的研究将致力于构建高危NB动物模型,以评估代谢靶向治疗在体内的安全性与有效性。
综上所述,本研究证明了蛋白质组学在NB风险分层和亚型鉴定中的巨大价值。通过整合临床特征和蛋白质表达谱,本研究从原发部位的胚胎特征以及高危亚型的线粒体代谢依赖,为NB的精准诊断和个性化治疗提供了丰富的理论资源。未来的研究应进一步探讨关键蛋白(如TIMM10)在体内环境下的功能,并验证评估相关代谢抑制剂在临床转化中的可能性。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 陈凯负责文献检索、研究设计、数据收集、实验操作、研究结果分析与讨论、论文撰写;武志祥负责研究指导、数据审核;吴晔明负责研究指导、全文知识性内容的审读与修正
| [1] |
张梅慧, 姜大朋. 先天性神经母细胞瘤发病机制与临床特点的研究进展[J]. 临床小儿外科杂志, 2022, 21(2): 141-145. Zhang MH, Jiang DP. Pathogenesis and clinical characteristics of congenital neuroblastoma[J]. J Clin Ped Sur, 2022, 21(2): 141-145. DOI:10.3760/cma.j.cn101785-202105045-008 |
| [2] |
Maris JM. Recent advances in neuroblastoma[J]. N Engl J Med, 2010, 362(23): 2202-2211. DOI:10.1056/NEJMra0804577 |
| [3] |
Khelifa L, Hu YB, Tall J, et al. Diagnostic technologies for neuroblastoma[J]. Lab Chip, 2025, 25(15): 3630-3664. DOI:10.1039/d4lc00005f |
| [4] |
Cohn SL, Pearson ADJ, London WB, et al. The International Neuroblastoma Risk Group (INRG) classification system: an INRG task force report[J]. J Clin Oncol, 2009, 27(2): 289-297. DOI:10.1200/JCO.2008.16.6785 |
| [5] |
Pugh TJ, Morozova O, Attiyeh EF, et al. The genetic landscape of high-risk neuroblastoma[J]. Nat Genet, 2013, 45(3): 279-284. DOI:10.1038/ng.2529 |
| [6] |
Dong R, Yang R, Zhan Y, et al. Single-cell characterization of malignant phenotypes and developmental trajectories of adrenal neuroblastoma[J]. Cancer Cell, 2020, 38(5): 716-733. e6. DOI:10.1016/j.ccell.2020.08.014 |
| [7] |
Blavier L, Yang RM, DeClerck YA. The tumor microenvironment in neuroblastoma: new players, new mechanisms of interaction and new perspectives[J]. Cancers (Basel), 2020, 12(10): 2912. DOI:10.3390/cancers12102912 |
| [8] |
Brady SW, Liu YL, Ma XT, et al. Pan-neuroblastoma analysis reveals age-and signature-associated driver alterations[J]. Nat Commun, 2020, 11(1): 5183. DOI:10.1038/s41467-020-18987-4 |
| [9] |
Wienke J, Dierselhuis MP, Tytgat GAM, et al. The immune landscape of neuroblastoma: challenges and opportunities for novel therapeutic strategies in pediatric oncology[J]. Eur J Cancer, 2021, 144: 123-150. DOI:10.1016/j.ejca.2020.11.014 |
| [10] |
Arif T, Shteinfer-Kuzmine A, Shoshan-Barmatz V. Decoding cancer through silencing the mitochondrial gatekeeper VDAC1[J]. Biomolecules, 2024, 14(10): 1304. DOI:10.3390/biom14101304 |
| [11] |
龙俊汕, 张京, 苏小霞, 等. 儿童神经母细胞瘤靶向治疗的研究进展[J]. 临床小儿外科杂志, 2023, 22(7): 619-624. Long JS, Zhang J, Su XX, et al. Research advances of targeted therapy for neuroblastoma in children[J]. J Clin Ped Sur, 2023, 22(7): 619-624. DOI:10.3760/cma.j.cn101785-202303039-004 |
| [12] |
Bansal M, Gupta A, Ding HF. MYCN and metabolic reprogramming in neuroblastoma[J]. Cancers (Basel), 2022, 14(17): 4113. DOI:10.3390/cancers14174113 |
 2026, Vol. 25
2026, Vol. 25


