2. 河北省儿童医院科研处, 石家庄 050031
2. Research Office, Hebei Provincial Children's Hospital, Shijiazhuang 050031, China
畸胎瘤通常发生于骶尾、纵隔、腹膜后及性腺,肾脏是畸胎瘤罕见的起源部位之一,肾脏未成熟畸胎瘤更为罕见[1-2]。肾脏未成畸胎瘤由于临床罕见,术前误诊率高。本文报道河北省儿童医院1例新生儿左侧肾脏未成熟畸胎瘤,结合文献复习此病病理学特点、临床表现、诊疗及预后情况,提高小儿外科医师对此病的认识和诊治水平。
患儿女,25日龄,因“发现腹部肿物1天”于2020年9月9日入院。其母孕期定期常规产检,彩超等结果无异常,生后母乳喂养。患儿因腹胀、面色苍白于当地医院就诊,腹部平扫CT提示左肾巨大肿块,考虑肾母细胞瘤可能性大,血常规:血红蛋白:71 g/L。体格检查:体温37℃、心率188次/min、呼吸52次/min、血压68/42 mmHg(1 mmHg=0.133 kPa)、血氧饱和度98%、体重2.83 kg。神志清楚,精神、反应较差。全身皮肤苍白,无黄染及出血点。心肺查体未见异常。专科查体:腹部明显膨隆,无胃肠型及蠕动波,可见腹壁静脉扩张,高度腹胀,腹部无明显压痛,无反跳痛及肌紧张,肝脾触诊不清,左腹可触及大小约11.0 cm×8.0 cm×7.0 cm肿物,质地较硬,边界欠规则,叩诊鼓音,肠鸣音正常。入院诊断:①腹部巨大肿物;②新生儿贫血(重度)。实验室检查:白细胞18.0×109/L、中性粒细胞百分比70.1%、血红蛋白85 g/L、C反应蛋白122.57 mg/L;甲胎蛋白10 327 ng/mL。腹部彩超:左中上腹部巨大肿物,考虑:占位性病变,腹腔积液(透声差);腹部CT平扫及强化:左上腹巨大占位性病变,考虑来源于左肾恶性肿瘤,透明细胞肉瘤可能,横纹肌肉瘤不除外,肾母细胞瘤不除外(图 1);患儿胸部CT、头颅CT等检查无远处转移表现。

|
图 1 肾脏未成熟畸胎瘤术前腹部平扫、强化CT Fig.1 Preoperative abdominal scan and enhanced CT image 注 A:平扫CT可见左上腹部巨大占位性病变,内可见散在高密度影;B.强化CT可见肿物包膜完整,左肾实质及左肾动静脉未见显示;C.强化CT冠状位显示病变上缘达胃下缘,下缘达脐水平,内缘跨越中线达右肾门、肝门水平,左肾正常形态显示不清 |
患儿于超声引导下行肿瘤穿刺,选择左侧腋后线与脐水平线交叉点上方2 cm,3 cm为进针点,分别穿刺3针,共取到浅白色组织6条。肿瘤穿刺病理结果:大部出血、坏死,结构消失,炎细胞漫润,见少量鳞状上皮、附属器及间叶组织,穿刺组织局限且大部坏死,考虑畸胎性肿瘤(图 2A)。患儿月龄小,体重轻,肿瘤巨大,组织全院专家行MDT多学科讨论后,拟行左侧肾脏肿瘤切除术。术前静点哌拉西林钠他唑巴坦钠、美罗培南、替考拉宁抗感染,输注悬浮红细胞纠正贫血、血浆输入、静点止血药物、营养支持等治疗。
|
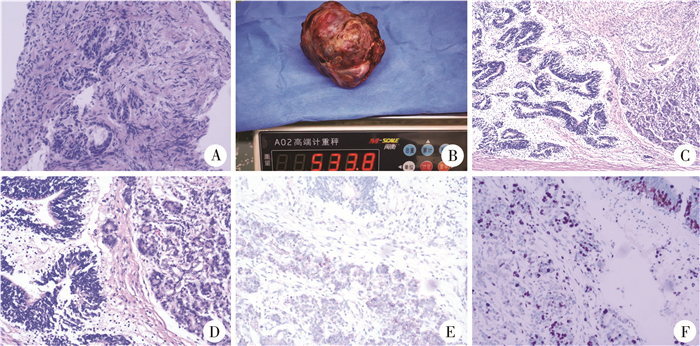
图 2 肾脏未成熟畸胎瘤手术标本及病理形态学检查 Fig.2 Surgical Specimen and Pathomorphological Examination of Renal Immature Teratoma 注 A:肿瘤穿刺组织:可见鳞状上皮、附属器及间叶组织(HE,×100);B:手术标本:肿瘤大小约11.0 cm×8.0 cm×7.0 cm,重量533.8 g,包膜较完整;C:手术标本:肿瘤边缘可见少量发育幼稚的肾小球及肾小管结构(HE,×100);D:手术标本:镜下可见原始神经管,部分间质分化欠成熟(HE,×400);E:免疫组化:AFP阴性(×100);F:免疫组化:Ki-67热区40%+(×100)。 |
完善术前准备后于全身麻醉下行左侧肾脏肿瘤切除术,术中关键细节如下:①手术入路:取上腹部横切口长约14 cm,切口跨越中线;因肿瘤巨大导致暴露困难,遂于中线处向上纵行切开至剑突下,肿瘤位于左侧腹膜后,越过中线,主体位于左侧,大小约11.0 cm×8.0 cm×7.0 cm;触摸右肾未见异常,判断未受肿瘤侵犯。取左侧结肠旁沟入路,切开左侧结肠外侧的侧后腹膜,将结肠、脾脏及胰腺向内侧牵拉;②主要粘连处理:肿瘤左下方与结肠系膜粘连紧密,分离中致部分系膜破损,确认横结肠、降结肠血运正常;③脾脏血供处理:脾脏动静脉受压变细无弹性;结合侧支供血存在、脾动脉供血减少且与肿瘤边界不清,于脾门处离断结扎脾动静脉,术后观察脾脏下极血供差而上极尚可;④肾蒂血管确认:分离肿瘤内侧离断供应血管,解剖追踪显示动脉源自腹主动脉、静脉汇入下腔静脉,位置与正常肾动静脉一致,确认为肿瘤供血肾蒂血管;⑤肿瘤完整切除:裸化肠系膜上动脉、腹主动脉,游离肿瘤与腰大肌粘连后完整切除肿瘤(图 2B)。
术后常规予预防感染、营养支持、白蛋白静点、补液等治疗。术后第3天发热,最高体温为39℃,双份血培养为屎肠球菌,给予应用替考拉宁抗感染治疗,感染逐渐控制。术后第7天查腹部胃肠道彩超示:脾脏下极实质回声减低不均匀、未见明显血流显示,脾静脉内径细;腹腔内未见明显积液。术后第8天,给予拔除腹腔引流管。术后第18天,无发热,吃奶好,无腹胀,顺利出院。术后病理学和免疫组织化学报告:肿瘤镜下见肾小球、肾小管、鳞状上皮、皮肤附属器、柱状上皮、胰腺、脉络丛上皮、肌肉、脂肪、骨、软骨、脑组织及室管膜上皮,部分含色素等,可见原始神经管,部分间质分化欠成熟,肿瘤内10%为片状坏死,未见其他恶性生殖细胞肿瘤成份(图 2C、2D)。病理学诊断:(左肾)囊实性未成熟畸胎瘤(2级);输尿管断端未见肿瘤。免疫组化:S-100(+)、Myognein(+)、PAX-8(+)、AFP(-)(图 2E)、WT-1(+)、CK(+)、GFAP(+)、CD99(+)、CD56(+)、Ki-67 40%(+)(图 2F)、Desmin(+)、PAX-8(+)、WT-1(+)、SALL-4(-)。术后5年随访期间,未见肿瘤复发或远处转移,脾脏结构逐步恢复正常,预后良好。
讨论 畸胎瘤起源于潜在多功能的原始胚细胞,肿瘤内含有三个胚层组织(内胚层、中胚层、外胚层)[3]。畸胎瘤发生位置与年龄相关,大龄儿童畸胎瘤常发生在性腺组织;婴幼儿以性腺外畸胎瘤多见,多见于骶尾部、纵隔、腹膜后、性腺部位,较少发生于舌部,极少发生于肾脏[4-6]。原始生殖细胞从卵黄囊向生殖嵴迁移的停止可导致出现不同解剖部位的畸胎瘤。由于原始生殖嵴接近肾原基,故生殖细胞可转移至肾脏,可部分解释肾脏畸胎瘤的发生,但具体发病机制尚未明确[7]。1934年,首次报道了肾脏畸胎瘤病例,为一7周龄的婴儿。肾脏畸胎瘤可分为成熟畸胎瘤和未成熟畸胎瘤,文献中记载的肾脏畸胎瘤病例不足60例,其中肾脏未成熟畸胎瘤尤为罕见,国内外文献至今仅报道了8例[6, 8-11]。本文通过检索PubMed、Medline、Embase、Web of Science以及中国知网、万方、维普网等中外文数据库,系统性地搜集相关资料,进一步补充了肾脏未成熟畸胎瘤的临床数据,为深入研究该疾病提供了重要参考(表 1)。
| 表 1 文献报道的8例肾脏未成熟畸胎瘤患者临床资料 Table 1 Clinical characteristics and pathologic features of renal immature teratoma (n=8) |
|
|
肾脏未成熟畸胎瘤术前诊断非常困难,最终诊断依赖切除标本的病理结果[12]。细针穿刺活检在术前虽可尝试获取少量组织样本,但受限于组织量较少,往往难以满足分子检测对样本量的要求,部分复杂病例中甚至无法明确诊断;因此在临床实践中,需结合患儿具体病情综合评估其适用性及局限性,谨慎选择。若肿瘤穿刺病理切片观察到鳞状细胞、柱状细胞和间充质成分,需怀疑畸胎瘤的诊断。本例符合Beckwith[13]提出的肾脏畸胎瘤诊断标准:①肿瘤位于肾脏被膜内,无肾脏外转移瘤证据;②镜下可见肾小管、肾小球残迹,且形成皮肤、神经上皮等肾脏外组织结构。结合患儿CT提示左肾占位、肿瘤包膜完整、Norris 2级无侵袭性生长特征等,肾脏畸胎瘤诊断明确。术后病理结果提示皮肤和神经上皮等未成熟成分,故诊断为肾脏未成熟畸胎瘤。儿童肾脏未成熟畸胎瘤术前应与神经母细胞瘤、肾母细胞瘤、肾囊肿、肾积水等肾脏区占位鉴别,尤其需区分畸胎瘤样肾母细胞瘤,以避免不必要的术前化疗[14-15]。
肾脏未成熟畸胎瘤一旦确诊,需早期手术切除[16]。本例患儿术前存在低体重,贫血,术前评估患儿一般情况差,给予输血等治疗,经治疗后患儿除体重较轻外,心肺功能无明显手术禁忌症,且患儿肿瘤性质尚不能完全明确,肿瘤压迫症状明显,患儿饮食受限,体重增长不佳,综合考虑尽早手术利大于弊。本例患儿术中离断脾脏动静脉主要有2点原因:①由于肿瘤巨大,脾脏血管受压明显,血流明显减少,加上手术过程牵拉,脾动脉基本无供血;②由于肿瘤大,脾脏血管不予结扎,严重影响操作。术后有对脾脏进行彩超随访,结果显示:术后1个月复查彩超:脾下极实质回声减低不均匀,未见明显血流显示;4个月后复查彩超:脾下极包膜欠光滑;术后10个月复查彩超:脾脏大小正常,实质回声尚均匀;且术后10个月复查CT:脾脏形态正常,大小正常,边缘清楚光整,密度均匀。对于小年龄患儿,脾脏完全切除可能发生术后爆发性感染,故尽可能保留脾脏,即使已经结扎脾脏动脉,也可以保留脾脏,避免脾脏全切或者部分切除。
关于外科术后的后继治疗仍缺乏相关数据,对于病理分级为Ⅰ级患者术后建议观察;Ⅲ级患者术后建议化疗[17]。对于病理结果回报为Norris 2级的未成熟畸胎瘤患儿术后化疗与否尚无明确结论,一般需综合考虑,可根据肿瘤分期、部位、影像学、AFP、Ki-67、手术切除等情况进行选择性化疗。本例患儿术后病理结果回报为Norris 2级,虽然本患者Ki-67指数40%+,且肿瘤体积较大,越过中线生长,并与周围组织脏器形成挤压粘连,都是可能对预后产生不利影响的因素,但考虑患者年龄体重小,化疗耐受差,手术切除肿瘤标本包膜完整,手术前后AFP均为生理性增高,故未给予化疗。目前常用化疗方案为PEB。COG方案推荐PEB(博来霉素+依托泊苷+顺铂),对于难治者可选择5-Fu、CTX、ADM、TPT等药物进行化疗药[18]。术后常规辅助化疗3~6个疗程。本例患儿术后未给予化疗,主要原因:①本患儿Norris病理分级为2级属低度恶性潜能,且术前术后甲胎蛋白均正常;②肿瘤局限于肾被膜内,无远处转移、邻近器官浸润;③患儿年龄小,体重低,营养状态差,化疗风险高。
预后评估及长期规范随访是肾脏未成熟畸胎瘤诊疗的重要环节,其预后与病理分级、肿瘤切除完整性密切相关,NorrisⅠ~Ⅱ级患者若实现完整切除,术后复发风险显著降低[17]。本例患儿为Norris 2级且术后未行化疗,参照临床常规制定个体化随访计划:术后1~3个月每月复查血常规、肝肾功能、甲胎蛋白及腹部彩超(评估脾脏恢复与腹腔占位);术后4~12个月每3个月复查1次,追加腹部CT明确手术区域及腹膜后情况;1年后调整为每年复查1次,一般建议随访至少5年。本例患儿术后5年随访期间未见复发或远处转移。术后5年随访期间,患儿各项实验室指标均正常,AFP水平保持稳定;腹部影像学检查显示脾脏形态和功能恢复良好,左肾手术区域无积液粘连,腹膜后及腹腔未见肿瘤复发或肿大淋巴结,饮食及体重增长正常,无手术相关并发症,整体预后良好。但由于该肿瘤临床病例稀少,远期复发风险尚不明确,后续仍需持续随访。
综上,儿童肾脏未成熟畸胎瘤临床极为罕见,术前缺乏特异性诊断依据,诊断难度较高,因此在儿童肾区占位性病变的鉴别诊断中需重点纳入,需与神经母细胞瘤、肾母细胞瘤等其他腹膜后实体肿瘤明确区分并针对性诊疗,以精准制定个体化治疗策略;同时,术后长期规范随访是评估患儿预后、早期发现肿瘤复发的关键环节。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 祁艳卫、孙会媛负责论文起草;张文辉、董政负责临床资料收集;仲智勇负责对文章知识性内容进行审阅。全体作者均参与本研究的选题与设计讨论,对研究数据的真实性、完整性及分析解释承担相应责任,并同意本文发表且对研究工作的诚信问题共同负责
| [1] |
Guntiboina VA, Islam N, Banerjee S, et al. Post therapy Wilms tumour or ectopic immature renal tissue: a pathologist's diagnostic dilemma[J]. Indian J Pathol Microbiol, 2019, 62(2): 266-269. DOI:10.4103/IJPM.IJPM_112_18 |
| [2] |
Chu H, Deng QF, Liu X, et al. Kidney teratoma: a case report and literature review[J]. Urol Case Rep, 2018, 20: 83-84. DOI:10.1016/j.eucr.2018.07.012 |
| [3] |
Albany C, Einhorn LH. Extragonadal germ cell tumors: clinical presentation and management[J]. Curr Opin Oncol, 2013, 25(3): 261-265. DOI:10.1097/CCO.0b013e32835f085d |
| [4] |
Bokemeyer C, Nichols CR, Droz JP, et al. Extragonadal germ cell tumors of the mediastinum and retroperitoneum: results from an international analysis[J]. J Clin Oncol, 2002, 20(7): 1864-1873. DOI:10.1200/JCO.2002.07.062 |
| [5] |
Motzer RJ, Amsterdam A, Prieto V, et al. Teratoma with malignant transformation: diverse malignant histologies arising in men with germ cell tumors[J]. J Urol, 1998, 159(1): 133-138. DOI:10.1016/s0022-5347(01)64035-7 |
| [6] |
张崔建, 杨新宇, 李学松, 等. 肾脏非成熟囊性畸胎瘤一例报道及文献回顾[J]. 中华临床医师杂志(电子版), 2010, 4(12): 2563-2566. Zhang CJ, Yang XY, Li XS, et al. Report of a case of immature cystic teratoma of the kidney and review of the literature[J]. Chin J Clin (Electronic Edition), 2010, 4(12): 2563-2566. DOI:10.3877/cma.j.issn.1674-0785.2010.12.042 |
| [7] |
Sigumonrong YH, Putra AA. Renal immature teratoma in infant: a rare case report[J]. Urol Case Rep, 2025, 59: 102967. DOI:10.1016/j.eucr.2025.102967 |
| [8] |
Liu YC, Wang JS, Chen CJ, et al. Intrarenal mixed germ cell tumor[J]. J Urol, 2000, 164(6): 2020-2021. DOI:10.1097/00005392-200012000-00039 |
| [9] |
康子明, 王城, 张彪, 等. 成人肾盂畸胎瘤1例[J]. 临床泌尿外科杂志, 2025, 40(4): 382-386. Kang ZM, Wang C, Zhang B, et al. One case report of renal pelvic teratoma in adult[J]. J Clin Urol, 2025, 40(4): 382-386. DOI:10.13201/j.issn.1001-1420.2025.04.018 |
| [10] |
李俊龙, 章小龙, 徐刚, 等. 原发性肾非成熟性畸胎瘤1例报告[J]. 中华泌尿外科杂志, 2022, 43(3): 219-220. Li JL, Zhang XL, Xu G, et al. Primary renal immature teratoma: one case report[J]. Chin J Urol, 2022, 43(3): 219-220. DOI:10.3760/cma.j.cn112330-20210126-00049 |
| [11] |
Al Sharqi A, Mouaffak S, Al Rahbi F, et al. Primary immature renal teratoma in a neonate[J]. Oman Med J, 2023, 38(5): e558. DOI:10.5001/omj.2023.49 |
| [12] |
Ronchi A, Cozzolino I, Montella M, et al. Extragonadal germ cell tumors: not just a matter of location.A review about clinical, molecular and pathological features[J]. Cancer Med, 2019, 8(16): 6832-6840. DOI:10.1002/cam4.2195 |
| [13] |
Beckwith JB. Wilms' tumor and other renal tumors of childhood: a selective review from the National Wilms' Tumor Study Pathology Center[J]. Hum Pathol, 1983, 14(6): 481-492. DOI:10.1016/s0046-8177(83)80003-3 |
| [14] |
Idrissi-Serhrouchni K, El-Fatemi H, El madi A, et al. Primary renal teratoma: a rare entity[J]. Diagn Pathol, 2013, 8: 107. DOI:10.1186/1746-1596-8-107 |
| [15] |
Geethamani V, Kusuma V, Gowda KMS, et al. Adult Wilms' tumour: a case report with review of literature[J]. Diagn Pathol, 2006, 1: 46. DOI:10.1186/1746-1596-1-46 |
| [16] |
Hamidi H, Foladi N. Intrarenal teratoma within a horseshoe kidney-a case report[J]. Radiol Case Rep, 2020, 15(10): 1743-1746. DOI:10.1016/j.radcr.2020.07.013 |
| [17] |
杨婷, 王珊, 胡显良. 32例小儿未成熟畸胎瘤临床诊疗特点回顾分析[J]. 中国小儿血液与肿瘤杂志, 2015, 20(5): 245-250. Yang T, Wang S, Hu XL. Retrospective study of clinical features of immature teratoma in young children: a report of 32 cases[J]. J China Pediatr Blood Cancer, 2015, 20(5): 245-250. DOI:10.3969/j.issn.1673-5323.2015.05.006 |
| [18] |
姚强华, 汤静燕, 潘慈, 等. 儿童Ⅳ期颅外恶性生殖细胞肿瘤疗效观察[J]. 临床儿科杂志, 2017, 35(5): 321-324. Yao QH, Tang JY, Pan C, et al. Study on the clinical outcomes of children with stage Ⅳ malignant extracranial germ cell tumors[J]. J Clin Pediatr, 2017, 35(5): 321-324. DOI:10.3969/j.issn.1000-3606.2017.05.001 |
 2026, Vol. 25
2026, Vol. 25


