2. 曲靖市妇幼保健院 昆明理工大学附属曲靖市妇幼保健院影像科, 曲靖 655099
2. Department of Radiology, Qujing Maternal and Children's Healthcare Hospital, Kunming University of Science and Technology, Qujing 655099, China
儿童腮腺病变的疾病谱与成人存在显著差异,儿童腮腺区病损以先天性疾病和脉管性肿物(如血管瘤、鳃裂囊肿、腮腺淋巴管畸形等)最为常见,仅有不到5%的腮腺肿瘤发生于儿童群体[1-2]。目前,国内外学者对儿童腮腺少见肿瘤的临床特征及影像学表现缺乏深入系统的研究,相关报道多为个案[3]。本研究通过回顾性分析儿童腮腺少见肿瘤的临床特点及CT、MRI表现,总结其影像学特征,以期提高儿童腮腺病变术前诊断的准确性。
资料与方法 一、临床资料本研究为回顾性病例系列研究,收集2014年1月至2025年5月上海市儿童医院收治的13例腮腺少见肿瘤患儿的临床资料,所有患儿均经手术及病理检查确诊。其中男8例、女5例,年龄3岁2个月至15岁4个月,中位年龄10岁2个月。病理类型包括多形性腺瘤7例、肌上皮瘤1例、淋巴瘤2例、横纹肌肉瘤1例、分泌性癌1例、NTRK重排梭形细胞肿瘤1例。本研究已通过上海市儿童医院医学伦理委员会审核批准(2025R177 — E01),免除患儿及家属知情同意。
二、检查方法13例患儿术前均行腮腺CT平扫+增强检查,10例行MRI平扫检查,6例行MRI增强检查。重点分析病灶的部位、形态与边界、密度/信号特征(含出血、坏死、钙化及囊变等情况)、强化方式、周围血管变化及邻近解剖结构改变等指标。
三、治疗方式5例仅行腮腺肿物切除术;6例行腮腺肿物+腮腺浅叶切除术;1例行腮腺肿物+腮腺全切除术;2例术中发现肿大淋巴结,同时行淋巴结清扫术;2例因肿物与面神经总干及分支黏连明显,术中同步进行面神经解剖减压术,解剖并保护面神经各分支;1例横纹肌肉瘤患儿行腮腺肿块活检术后进一步予以放化疗治疗。
结果13例患儿的临床表现均无特异性,主要表现为耳前区、耳垂下或腮腺后下极区肿块,部分肿块呈缓慢增大趋势。所有患儿术后定期门诊随访2~97个月,目前无复发、转移病例,亦无面神经受损情况。13例腮腺肿瘤患儿的临床特征及病理类型详见表 1。
| 表 1 13例腮腺肿瘤患儿的临床特征及病理类型 Table 1 Clinical characteristics and pathological types of 13 children with parotid gland tumors |
|
|
13例患儿术前血常规及肝肾功能电解质均未见明显异常,1例患儿神经元特异性烯醇化酶(neuron-specific enolase,NSE)轻度升高。13例病灶均为单侧单发,其中11例位于右侧,2例位于左侧(1例多形性腺瘤、1例横纹肌肉瘤);6例仅位于浅叶(5例多形性腺瘤、1例肌上皮瘤),7例同时累及浅叶和深叶。分泌性癌及横纹肌肉瘤形态欠规则,略呈分叶状;其余病灶均呈圆形或类圆形,边界清晰。横纹肌肉瘤及NTRK重排梭形细胞肿瘤最大径>3 cm,其余病灶最大径均<3 cm。不同病理类型腮腺肿瘤的影像学特点详见表 2及图 1—图 6。
| 表 2 不同病理类型腮腺肿瘤的强化及弥散特点 Table 2 The enhancement and diffusion characteristics of different pathological types |
|
|
|
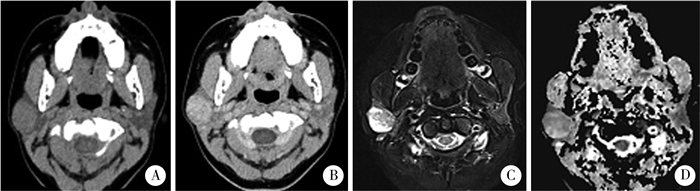
图 1 多形性腺瘤患儿的CT及MRI表现 Fig.1 CT and MRI findings of a child with pleomorphic adenoma of parotid gland 注 女,11岁8个月,发现右侧耳下肿物2月余。A-B: CT平扫+增强扫描图像:右侧腮腺浅叶稍低密度肿块, 延迟期明显强化; C-D:MRI图像: T2WI-FS等高混杂信号,ADC图等高混杂信号 |

|
图 2 腮腺肌上皮瘤患儿的CT及MRI表现 Fig.2 CT and MRI findings of a child with parotid myoepithelioma 注 男,11岁4个月,发现右侧颊部肿物半年余。A-C: CT平扫+增强动静脉期图像,右侧腮腺浅叶咬肌旁稍低密度肿块,动脉期边缘明显强化,静脉期强化幅度增加并向中心进一步充填;D:MRI图像: T2WI稍高信号伴边缘低信号环,内见微囊样高信号 |

|
图 3 腮腺经典型霍奇金淋巴瘤患儿的CT及MRI表现 Fig.3 CT and MRI findings of a child with Classic Hodgkin lymphoma of the parotid gland 注 男,7岁11个月,发现右侧耳垂下肿物5月余。A-B:CT平扫+增强扫描图像,右侧腮腺稍高密度肿块,静脉期中度强化;C-D:MRI图像,T2WI-FS均匀稍高信号,ADC图显示明显弥散受限 |

|
图 4 腮腺横纹肌肉瘤患儿的CT及MRI表现 Fig.4 CT and MRI findings of a child with parotid rhabdomyosarcoma 注 女,3岁2个月,发现左侧耳后肿物1月余。A-B:CT平扫+增强扫描图像,左侧腮腺分叶状稍低密度肿块,静脉期明显强化,周边强化为主,内见未强化区;C-D:MRI图像,T2WI-FS等高混杂信号,DWI序列呈高信号 |
|
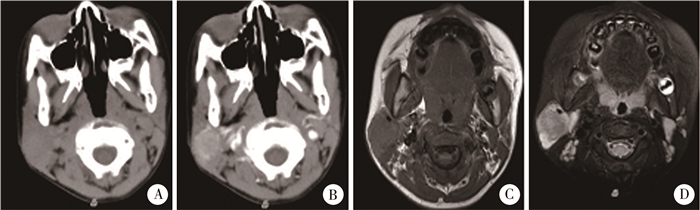
图 5 腮腺分泌性患儿的CT及MRI表现 Fig.5 CT and MRI findings of a child with parotid secretory carcinoma 注 男,4岁11个月,发现右侧腮腺区肿物7月余。A-B:CT平扫+增强扫描图像,右侧腮腺不规则形等密度肿块,动脉期明显强化,周边见供血血管;C-D:MRI图像,T1WI稍高信号,T2WI-FS呈等低信号为主,边缘淋巴结呈稍高信号 |

|
图 6 腮腺NTRK重排梭形细胞肿瘤患儿的CT及MRI表现 Fig.6 CT and MRI findings of a child with parotid NTRK rearranged spindle cell neoplasm 注 男,5岁7个月,发现右侧面部肿块3月余。A-B:CT平扫+增强扫描图像,右侧腮腺稍低密度肿块,静脉期明显强化;C-D: MRI图像,T1WI均匀等信号, T2WI-FS高信号, 内见低信号的面神经分支 |
术前正确诊断7例,诊断准确率为53.8%;误诊或诊断不明确6例,占比46.2%。其中2例多形性腺瘤和1例淋巴瘤因未行MRI检查误诊为肿大淋巴结;2例分别因对肌上皮瘤、分泌性癌认识不足误诊为脉管源性肿瘤;1例仅诊断为间叶来源良性肿瘤,未明确具体病理类型。
讨论儿童腮腺最常见的病变为血管瘤、鳃裂囊肿及腮腺淋巴管畸形等。腮腺多形性腺瘤、肌上皮瘤、分泌性癌等疾病好发于成人,10岁以下儿童罕见;淋巴瘤虽好发于儿童头颈部,但原发于腮腺者十分罕见,仅占腮腺肿瘤的1.5%左右[4];横纹肌肉瘤好发于儿童头颈部的鼻腔、鼻窦及眼眶等部位,发生于腮腺者较少见[5]。
儿童腮腺少见肿瘤的临床表现缺乏特异性,良性肿瘤与恶性肿瘤初期均可表现为单侧腮腺区局限性无痛性缓慢生长的肿块,且多为单侧单发;横纹肌肉瘤因进展迅速,可能出现局部疼痛症状;炎性包块也可表现为快速增长伴疼痛,因此仅依靠临床症状和体征难以做出准确诊断。不同病理类型肿瘤的治疗方案存在差异,术前准确定性对于指导临床制定个性化治疗方案具有重要意义[6]。CT及MRI检查是诊断腮腺病变的重要手段,可清晰显示肿瘤的位置、累及范围及与周围组织的关系;结合病灶的边界特征(清晰或不规则)、T2WI信号强度(高信号或低信号)、动态增强强化特点、弥散受限程度及ADC值大小等指标,可鉴别常见的腮腺良恶性肿块,且对预测肿瘤病理类型具有较高的诊断价值[7-8]。
多形性腺瘤在组织学上由肿瘤性上皮组织与黏液样或黏液软骨样间质混合构成,因其细胞形态和结构具有特征性多样性,导致其密度及信号表现多样[9]。CT上多呈等或低密度,T2WI信号多不均匀;动态增强表现为轻中度持续性渐进性强化及延迟强化,TIC曲线为A型渐进性强化型,这可能与肿瘤富含黏液基质、上皮成分较少、血管分布稀疏,导致造影剂渗漏及廓清缓慢有关[8-9];DWI及ADC图示轻度弥散受限,文献报道其ADC值为(1.47±0.16)×10-3mm2/s[10],高于腮腺其他良性肿瘤,主要因其富含黏液样及软骨样组织,细胞排列不紧密、细胞外间隙大,水分子弥散受限不明显[7]。本组7例多形性腺瘤的实性成分均表现出渐进性强化的典型特征。该肿瘤的治疗首选外科手术完整切除瘤体,由于其存在复发及恶变风险,临床常采用腮腺全切除术或部分切除术以彻底清除病灶[6]。
肌上皮瘤的增强表现多为早期明显强化,并持续向心性强化,这主要与肿瘤内含有丰富的毛细血管及静脉有关;MRI上T1WI呈稍低信号、T2WI呈稍高信号,囊变区呈明显高信号,实性部分弥散成像示轻度受限。由于肌上皮瘤血供丰富,其强化程度高于多形性腺瘤;且因细胞成分较密集,不含黏液样及软骨样成分,其弥散受限程度较多形性腺瘤高。临床治疗以手术根治切除为主,若切除不完全则易复发,多次复发可能发生恶变。
原发性腮腺淋巴瘤十分罕见,多为非霍奇金淋巴瘤,好发于学龄期男童;霍奇金淋巴瘤也可发生于腮腺内淋巴结,好发于10岁以上儿童,影像学检查无法区分这两种淋巴瘤。CT上多表现为类圆形、密度均匀的软组织肿块,因血流灌注较低,呈轻中度强化,部分可见包膜强化;MRI上多为信号均匀的实性肿块,由于肿瘤细胞排列密集、核浆比高且核异型性明显,扩散加权成像呈明显高信号是其特征性表现;ADC值极低,约为0.5×10-3mm2/s,通过最小ADC值可将其与多形性腺瘤及其他恶性肿瘤相鉴别。病理检查是淋巴瘤确诊及分型的金标准,通常选择病变淋巴结或结外病灶进行切除活检。霍奇金淋巴瘤的治疗一般采用化疗联合放疗的综合治疗及个体化治疗原则,总体疗效及预后较好。目前,儿童滤泡性淋巴瘤的治疗缺乏明确的治疗指南或专家共识,最主流的治疗选择为观察- 等待方案,其总体预后较好[11]。
横纹肌肉瘤具有侵袭性强、进展迅速的特点,因此发现时肿块体积一般较大,形态不规则,内部多因坏死导致密度及信号不均匀。CT上多呈等或稍低于肌肉的密度,这与肿瘤细胞富含黏液基质有关;增强表现为明显不均匀渐进性强化[12],由于肿瘤具有绕血管生长的特点,内部可见条状血管影,即围血管现象[5],周边环状强化或葡萄状强化是其特征性影像学表现[12],这可能与肿块中央为黏液基质、边缘为肿瘤细胞有关;MRI上表现为实性为主的肿块,T1WI呈等或稍低信号,T2WI呈等或稍高信号,其恶性程度高,细胞增殖迅速、排列紧密,扩散加权成像显示明显高信号[13],ADC值明显降低,但一般高于淋巴瘤,约为0.7×10-3mm2/s[14];TIC曲线呈速升平台型,坏死区和黏液成分无强化[5, 12-14]。组织病理学检查是诊断横纹肌肉瘤的金标准,结合免疫组化可提高诊断率。治疗多采用手术、放疗及化疗相结合的综合治疗方式,预后与年龄、病变部位、肿瘤大小及临床分期等多种因素相关。
涎腺分泌性癌是一种少见的低度恶性肿瘤,多同时累及腮腺浅叶及深叶,可表现为实性、囊实性或囊性为主。CT上呈类圆形或浅分叶状肿物,增强表现为“快进缓出”的特点;MRI上实性成分T1WI呈等高信号,因常伴有含铁血黄素沉积的出血,T2WI表现为特征性低信号,增强扫描实性部分TIC曲线呈速升- 速降型。该肿瘤虽为低度恶性,但肿瘤细胞以实性结构为主,细胞密度高、组织间隙小,DWI示扩散受限,ADC值较低。ETV6-NTRK3基因融合是其诊断金标准。治疗首选手术切除,可辅助放化疗,其临床生物学行为多为惰性,预后良好。
NTRK重排梭形细胞肿瘤是一种以NTRK重排为分子特征的软组织肿瘤,儿童多见,好发于头颈、四肢、躯干的浅表或深部软组织,患儿多因无痛性肿块或压迫症状就诊[15-16]。影像学上具有富血供及易于局灶性侵犯周围组织(尤其是脂肪组织)的特点[17],MRI扫描与骨骼肌相比,T1WI呈等信号或略高信号,T2WI呈高信号;增强扫描示明显强化,部分病例表现为肿瘤周边强化。本组病例为实性肿块,包绕面神经生长,呈明显均匀渐进性强化,静脉期强化程度最高,与以往报道相符[17]。术前仅依靠影像学检查难以做出正确诊断,弥散受限程度仅可提示其良恶性。该肿瘤组织学差异较大,仅靠镜下观察也难以确诊,分子水平确认NTRK基因存在重排是诊断的金标准[18]。治疗首选手术完整切除瘤体,部分报道显示其具有局部侵袭性,复发率为25% ~40%,罕见转移,对于复发、转移或无法完整切除的病例,建议采用靶向药物治疗[16]。
综上所述,儿童腮腺少见肿瘤的病理类型多样,其影像学表现具有各自的特异性特征,结合增强表现及弥散受限程度,可初步预测肿瘤的恶性程度及病理类型,为临床术前制定治疗方案提供重要参考依据。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 蔡雪梅负责临床资料的搜集、归纳和起草文案;袁文赢负责病例影像资料和临床资料的收集;徐化凤负责研究的设计、实施和起草、修改文案,并对文章知识性内容进行审阅
| [1] |
徐宏鸣, 郑阳阳, 陈芳, 等. 儿童腮腺区病损的诊疗特点[J]. 临床耳鼻咽喉头颈外科杂志, 2020, 34(10): 941-944. Xu HM, Zheng YY, Chen F, et al. Diagnosis and characteristics of parotid region lesions in children[J]. J Clin Otorhinolaryngol Head Neck Surg, 2020, 34(10): 941-944. DOI:10.13201/j.issn.2096-7993.2020.10.017 |
| [2] |
Ord RA, Carlson ER. Pediatric salivary gland malignancies[J]. Oral Maxillofac Surg Clin North Am, 2016, 28(1): 83-89. DOI:10.1016/j.coms.2015.07.007 |
| [3] |
赵娜, 裴广华. 1例儿童腮腺分泌性癌超声表现[J]. 中国医学影像技术, 2023, 39(12): 1897. Zhao N, Pei GH. Ultrasonic manifestations of parotid secretory carcinoma in a child: case report[J]. Chin J Med Imaging Technol, 2023, 39(12): 1897. DOI:10.13929/j.issn.1003-3289.2023.12.035 |
| [4] |
El-Naggar AK, Chan JKC, Grandis JR, et al. WHO classification of head and neck tumours[M]. 4th ed. Lyon: International Agency for Research on Cancer, 2017: 276-280.
|
| [5] |
Jawad N, McHugh K. The clinical and radiologic features of paediatric rhabdomyosarcoma[J]. Pediatr Radiol, 2019, 49(11): 1516-1523. DOI:10.1007/s00247-019-04386-5 |
| [6] |
Hellquist H, Paiva-Correia A, Vander Poorten V, et al. Analysis of the clinical relevance of histological classification of benign epithelial salivary gland tumours[J]. Adv Ther, 2019, 36(8): 1950-1974. DOI:10.1007/s12325-019-01007-3 |
| [7] |
Kato H, Kawaguchi M, Ando T, et al. Current status of diffusion-weighted imaging in differentiating parotid tumors[J]. Auris Nasus Larynx, 2023, 50(2): 187-195. DOI:10.1016/j.anl.2022.07.002 |
| [8] |
Pâris P, Fath L, Schultz P, et al. Diffusion-weighted and gadolinium-enhanced dynamic MRI in parotid gland tumors[J]. Eur Arch Otorhinolaryngol, 2023, 280(1): 391-398. DOI:10.1007/s00405-022-07590-6 |
| [9] |
Bianchini C, Brugali M, Migliorelli A, et al. Basal cell adenoma and pleomorphic adenoma of the parotid gland: a single center experience[J]. Minerva Surg, 2023, 78(6): 626-632. DOI:10.23736/S2724-5691.23.09876-3 |
| [10] |
文宝红, 程敬亮, 张会霞, 等. 磁共振高清扩散加权成像鉴别腮腺良恶性上皮性肿瘤的价值[J]. 中华医学杂志, 2018, 98(17): 1347-1351. Wen BH, Cheng JL, Zhang HX, et al. Value of high-resolution diffusion weighted imaging in differentiating benign and malignant epithelial tumors of parotid gland[J]. Natl Med J China, 2018, 98(17): 1347-1351. DOI:10.3760/cma.j.issn.0376-2491.2018.17.013 |
| [11] |
Choi J, Choi HJ, Yim K, et al. Pediatric follicular lymphoma of the parotid gland[J]. Arch Craniofac Surg, 2018, 19(4): 279-282. DOI:10.7181/acfs.2018.02075 |
| [12] |
Gennaro N, Marrari A, Renne SL, et al. Multimodality imaging of adult rhabdomyosarcoma: the added value of hybrid imaging[J]. Br J Radiol, 2020, 93(1112): 20200250. DOI:10.1259/bjr.20200250 |
| [13] |
Inarejos Clemente EJ, Navallas M, Barber Martínez de la Torre I, et al. MRI of rhabdomyosarcoma and other soft-tissue sarcomas in children[J]. Radiographics, 2020, 40(3): 791-814. DOI:10.1148/rg.2020190119 |
| [14] |
Wang XY, Song LY, Chong V, et al. Multiparametric MRI findings of sinonasal rhabdomyosarcoma in adults with comparison to carcinoma[J]. J Magn Reson Imaging, 2017, 45(4): 998-1004. DOI:10.1002/jmri.25484 |
| [15] |
WHO Classification of Tumours Editorial Board. Soft tissue and bone tumours[M]. 5th ed. Lyon: International Agency for Research on Cancer, 2020.
|
| [16] |
Marchetti A, Ferro B, Pasciuto MP, et al. NTRK gene fusions in solid tumors: agnostic relevance, prevalence and diagnostic strategies[J]. Pathologica, 2022, 114(3): 199-216. DOI:10.32074/1591-951X-787 |
| [17] |
Kobayashi H, Teramura Y, Yamashita K, et al. Imaging findings of NTRK?rearranged spindle cell neoplasms: a case series[J]. Mol Clin Oncol, 2023, 18(3): 14. DOI:10.3892/mco.2023.2610 |
| [18] |
韦笑, 吴鸿雁, 濮晓红, 等. NTRK重排梭形细胞肿瘤1例[J]. 中华病理学杂志, 2023, 52(12): 1278-1280. Wei X, Wu HY, Pu XH, et al. NTRK-rearranged spindle cell neoplasm: report of a case[J]. Chin J Pathol, 2023, 52(12): 1278-1280. DOI:10.3760/cma.j.cn112151-20230831-00113 |
 2026, Vol. 25
2026, Vol. 25


