儿童脾良性病变临床较为少见,发病率仅为全身肿瘤的0.1%,以脾囊肿与脉管源性肿瘤为主要类型,外科手术切除是其主要治疗方法。随着微创技术的发展,以及临床对脾脏免疫功能和全脾切除术后并发症认识的不断深入,腹腔镜脾切除尤其是腹腔镜脾部分切除逐渐受到临床重视。但目前儿童脾脏肿瘤相关报道仍较少,儿童腹腔镜脾部分切除术因操作难度较高,其安全性与有效性仍需更多循证医学证据支持。本文通过回顾性分析脾良性病变患儿的临床资料,旨在为儿童脾良性病变的临床治疗提供参考,现报道如下。
资料与方法 一、一般资料本研究为回顾性队列研究。2015年6月至2024年7月,浙江大学医学院附属儿童医院共对23例脾良性病变患儿实施脾部分切除手术,其中男12例、女11例,年龄10.50(8.00, 12.08)岁。2例患儿伴间歇性腹痛;4例脾囊肿合并感染,其中1例先行囊肿外引流术,延期3个月行脾部分切除;其余17例均无临床症状,为门诊B超检查偶然发现。病变直径<5 cm者予门诊定期随访,6个月~2年观察期间病变逐渐增大至5 cm以上者,行手术切除;1例脾囊肿曾于外院行超声定位下囊肿穿刺无水酒精注射治疗2次,因囊肿缩小不明显改行手术治疗。本研究经浙江大学医学院附属儿童医院伦理委员会审核通过(2024-IRB-0300-P-01),所有患儿法定监护人均签署知情同意书。
二、术前影像学检查23例均行腹部B超检查,19例行腹部增强CT扫描,15例行腹部MRI检查。影像学检查初步诊断脾囊肿10例、血管瘤8例、淋巴管瘤2例、错构瘤1例、肿瘤性质不明2例;脉管瘤的术前影像诊断与术后病理诊断符合率仅为30.77%(4/13)。超声检查示病变单个最大径5.85(5.30, 8.00)cm,位于上极/中上极9例、下极/中下极14例。
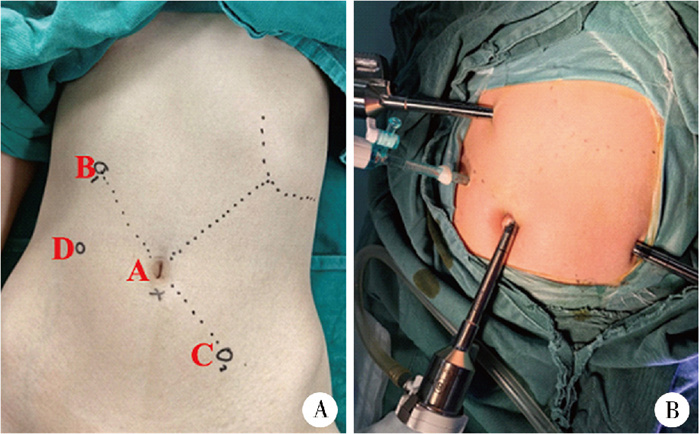
三、手术方法患儿取右倾头高体位,脐正中布置主视镜,右上腹及左锁骨中线髂前上棘水平布置操作孔,分别放置马里兰钳、电凝钩/持针器/超声刀,右中腹布置辅助孔(图 1)。打开小网膜囊,缝制胃牵引线,在脾门处解剖脾血管,先结扎拟切除的脾极的动脉,分离出该脾极静脉后等待5~10 min,待结扎后脾极缺血分界线明显,脾血回流后再结扎脾静脉,离断脾周围韧带,保护预留脾极的韧带和血管,超声刀沿脾脏表面的缺血线一侧0.5~1 cm离断脾脏,断面双极电凝止血后3 - 0可吸收线间断缝合止血(图 2)。对于跨越脾上下极的病变,可进一步解剖脾血管分支,直至拟切除脾组织缺血(超选择性脾血管结扎, 图 3)。对于病变巨大,只能保留上、下极部分脾组织者,可结扎脾动脉主干,保留胃短血管与脾膈韧带及不经脾门而直接进入脾上、下极的脾极血管(图 4)。切除之脾脏组织装入标本袋后适当扩大脐部切口,剪碎脾组织后取出。术后常规脾窝处留置腹腔引流。
|
图 1 机器人脾部分切除手术Troca布孔图 Fig.1 Trocar placement during robot-assisted partial splenectomy 注 A:脐部正中布置镜头孔;B、C:右上腹及左下腹分别布置操作孔;D:右中腹布置辅助孔 |
|
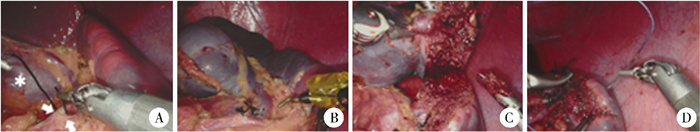
图 2 机器人辅助规则脾上极切除手术图片 Fig.2 Intraoperative images of robot-assisted anatomical resection of the upper pole of the spleen 注 A:脾上极血管结扎(*为脾上极病变,→为脾上、下极动脉);B: 脾上极动脉结扎后脾脏表面形成分解清楚的缺血线;C:超声刀沿缺血线离断脾实质;D:脾断面3-0可吸收线间断缝合止血 |
|
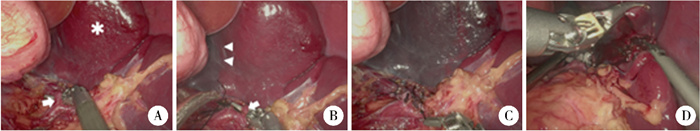
图 3 机器人辅助超选择性脾血管结扎的脾部分切除手术图片 Fig.3 Intraoperative images of robot-assisted partial splenectomy with super-selective splenic vessel ligation 注 A:病变位于脾中上极,游离出上极血管(*为脾上极病变,→为脾上极动脉);B:脾上极动脉结扎后,部分脾实质缺血,部分肿瘤组织仍未缺血,继续解剖脾下极血管分支(→);C:脾下极血管分支结扎后,包含肿瘤组织的脾组织已缺血;D:超声刀沿缺血线离断脾实质 |
|
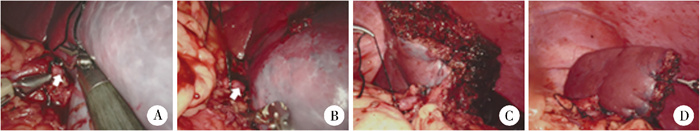
图 4 机器人辅助脾动脉主干结扎的脾大部分切除手术图片 Fig.4 Intraoperative images of robot-assisted subtotal splenectomy with ligation of the main trunk of the splenic artery 注 A:脾巨大病变位于脾中下极,结扎脾下极血管(→);B:结扎脾下极血管后部分病变组织仍未缺血,结扎脾动脉主干(→);C:脾实质离断,残脾血运良好;D:保留胃短血管和脾膈韧带的脾大部分切除 |
所有切除标本均常规行组织病理HE染色,必要时加做免疫组织化学染色。根据病理检查结果明确病变类型,其中4例患儿经免疫组织化学染色最终确诊。
五、术后处理与随访术后12~24 h指导患儿进食;腹腔引流液<20 mL/d时拔除引流管。术后监测血小板水平,血小板>600×109/L时口服双嘧达莫,血小板>800×109/L时加用阿司匹林。本研究中8例患儿术后服用双嘧达莫(腹腔镜组2例、机器人组6例),仅机器人手术组2例患儿术后加用阿司匹林。患儿出院后予门诊定期随访,监测血小板水平变化,定期复查脾脏超声,评估残脾血运、体积及病变复发情况。
六、统计学处理采用SPSS 22.0进行统计学分析。对非正态分布的计量资料采用M(Q1,Q3)描述,采用秩和检验进行组间比较。P < 0.05为差异有统计学意义。
结果23例患儿均顺利完成手术,无中转开腹病例;其中5例行腹腔镜脾部分切除术,18例行机器人辅助腹腔镜脾部分切除术。17例行规则的脾上极/脾下极切除术,3例行超选择性脾血管结扎脾大部分切除术,3例行脾动脉主干结扎脾大部分切除术。
腹腔镜组与机器人组患儿的年龄、病变最大径比较,差异均无统计学意义(P>0.05);机器人组手术时间、术中出血量均显著少于腹腔镜组,差异均有统计学意义(P<0.05);两组术后住院时间比较,差异无统计学意义(P>0.05)。见表 1。
| 表 1 机器人辅助与传统腹腔镜脾部分切除对比分析[M(Q1,Q3)] Table 1 Comparison between robot-assisted and conventional laparoscopic partial splenectomy [M (Q1, Q3)] |
|
|
术后病理诊断:脾上皮源性囊肿10例、淋巴管瘤6例、脾错构瘤4例,脾血管瘤、硬化性血管瘤样结节性转化、窦岸细胞血管瘤各1例。
所有患儿术后均无出血、膈下脓肿、血管栓塞、胰腺炎、胰瘘、残脾缺血、肠粘连梗阻等并发症发生;随访1个月至4年,无爆发性感染发生,未见病变复发;超声检查示残脾血运良好,无萎缩,且残脾体积逐渐增大。
讨论小儿脾良性病变以脾囊肿及脉管源性肿瘤为主,各类脉管源性肿瘤在影像学表现上高度相似,导致术前难以精准诊断病变类型[1-3]。本研究中13例脉管源性肿瘤患儿,术前影像诊断与术后病理诊断符合率仅30.77%,甚至3例淋巴管瘤术前被误诊为血管瘤;而脾囊肿多表现为单房性囊性包块,部分可见纤维分隔或囊内液体絮状物/分层,术前影像学可明确诊断,与临床报道一致。
目前儿童脾良性肿瘤尚无统一的最佳治疗策略,临床治疗方式包括穿刺注射、射频消融、介入栓塞及手术切除等,其中手术切除为最彻底的治疗方法。临床共识认为,直径<5 cm的无症状脾良性肿瘤可门诊定期随访,若随访期间肿瘤增大或出现临床症状,需及时干预,避免感染、出血、破溃等并发症发生[4-5]。穿刺注射治疗虽有临床应用,但疗效不一,且部分病例需麻醉下反复操作,复发率较高[6];本研究中1例脾囊肿患儿经2次超声引导下无水酒精注射治疗后效果不佳,改行脾部分切除术后痊愈。囊肿开窗术虽操作简单、可保留脾脏免疫功能,但文献报道其复发率高达60% ~80%[7];同时脾脉管源性肿瘤存在恶变可能,因此手术切除仍是目前脾脉管源性肿瘤的主要治疗方法。
全脾切除虽能彻底切除病变,但可导致儿童获得性免疫缺失、血浆免疫因子水平下降,显著增加爆发性感染的风险,且年龄越小感染风险越高[8]。研究证实,保留25%以上的脾脏组织即可维持儿童正常B细胞水平,有效预防感染[9];且脾部分切除患者术后T、B淋巴细胞水平均高于全脾切除者。因儿童免疫功能尚未发育完善,保留脾脏的治疗方式更适合用于儿童脾良性病变的治疗。
脾部分切除术既切除病灶,又保留部分脾实质,可最大程度保存脾脏免疫功能,是治疗脾脏局灶性病变的理想方法;而腹腔镜技术的应用进一步降低了手术创伤[10-11],成为临床首选术式之一。但腹腔镜脾部分切除术操作难度较高,脾脏断面出血、术后残脾缺血/扭转是其主要并发症。临床研究发现,沿血管结扎后脾脏表面的缺血线分离脾组织,可显著减少术中出血[12];同时,捆扎悬吊技术、脾断面间断缝合、带血管蒂大网膜覆盖、生物胶喷洒等措施,可进一步降低术后出血风险[13-14]。对于特殊病变,本研究提出针对性手术策略:①病变跨越脾上下极者,行超选择性脾血管结扎,可保留约1/3脾实质;②病变巨大无法行规则脾部分切除者,行脾动脉主干离断+保留胃短血管及脾膈韧带,可保留约1/4脾实质,且术后残脾血运良好、体积逐渐增大。此外,术中不宜过度游离拟保留的脾极组织,尽量保留其韧带与血管,必要时将残脾缝合固定于脾窝,可有效预防残脾缺血及扭转。
近年来,机器人手术系统在外科领域的应用,进一步提升了腹腔镜手术的微创性与精准性。本研究结果显示,与传统腹腔镜相比,机器人辅助腹腔镜脾部分切除具有以下优势:①机器人手术系统的灵活关节活动与高倍三维立体视野,使脾门解剖、脾二级血管游离及超选择性脾血管结扎操作更精准,减少脾血管损伤,显著降低术中出血量;②对于脾上极病变,机器人系统可在膈下狭窄空间内轻松完成脾胃韧带、脾膈韧带离断,无需过度游离脾周韧带,降低残脾扭转风险;③可提高脾部分切除成功率,实现对脾上极/跨越脾上下极病变的微创切除,而传统腹腔镜下此类病变多需开腹或行全脾切除。本研究中机器人手术组手术时间、术中出血量均显著少于腹腔镜组,且无严重并发症发生,与Berelavichus等[15]的研究结论一致。但机器人手术也存在费用较高、腹壁切口相对偏大、缺乏触觉反馈等缺点,临床可通过积累手术经验、视觉弥补等方式克服触觉反馈的不足。
综上,机器人辅助腹腔镜脾部分切除术治疗儿童脾良性病变安全、有效,在缩短手术时间、减少术中出血、提高手术成功率及保留正常脾组织等方面均优于传统腹腔镜手术,可在儿童患者中推广应用。对于脾脉管源性肿瘤,因自行消退可能性小且缺乏其他有效治疗手段,确诊后建议及时行脾部分切除术,避免病变增大增加手术难度及脾组织损失。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 宣笑笑、陈青江负责研究的设计、实施和起草文稿;罗文娟、黄宗伟、陈肯、金益、王林燕进行数据收集与分析;高志刚、熊启星、陈青江负责数据质量监管,并对文章知识性内容进行审阅
| [1] |
Wang ZM, Peng CH, Wu DY, et al. Surgical treatment of benign splenic lesions in pediatric patients: a case series of 30 cases from a single center[J]. BMC Surg, 2022, 22(1): 295. DOI:10.1186/s12893-022-01745-2 |
| [2] |
Boehnke MW, Watterson CT, Connolly SA, et al. Imaging features of pathologically proven pediatric splenic masses[J]. Pediatr Radiol, 2020, 50(9): 1284-1292. DOI:10.1007/s00247-020-04692-3 |
| [3] |
Milickovic M, Rasic P, Cvejic S, et al. Splenic hamartomas in children[J]. World J Clin Cases, 2024, 12(11): 1909-1917. DOI:10.12998/wjcc.v12.i11.1909 |
| [4] |
Chen QJ, Wang LY, Chen XL, et al. Laparoscopic management of benign splenic tumors in children[J]. World J Pediatr Surg, 2022, 5(4): e000419. DOI:10.1136/wjps-2022-000419 |
| [5] |
Lee SH, Lee JS, Yoon YC, et al. Role of laparoscopic partial splenectomy for tumorous lesions of the spleen[J]. J Gastrointest Surg, 2015, 19(6): 1052-1058. DOI:10.1007/s11605-015-2812-5 |
| [6] |
Accinni A, Bertocchini A, Madafferi S, et al. Ultrasound-guided percutaneous sclerosis of congenital splenic cysts using ethyl alcohol 96% and minocycline hydrochloride 10%: a pediatric series[J]. J Pediatr Surg, 2016, 51(9): 1480-1484. DOI:10.1016/j.jpedsurg.2016.05.005 |
| [7] |
Schier F, Waag KL, Ure B. Laparoscopic unroofing of splenic cysts results in a high rate of recurrences[J]. J Pediatr Surg, 2007, 42(11): 1860-1863. DOI:10.1016/j.jpedsurg.2007.07.012 |
| [8] |
Madenci AL, Armstrong LB, Kwon NK, et al. Incidence and risk factors for sepsis after childhood splenectomy[J]. J Pediatr Surg, 2019, 54(7): 1445-1448. DOI:10.1016/j.jpedsurg.2018.06.024 |
| [9] |
Buesing KL, Tracy ET, Kiernan C, et al. Partial splenectomy for hereditary spherocytosis: a multi-institutional review[J]. J Pediatr Surg, 2011, 46(1): 178-183. DOI:10.1016/j.jpedsurg.2010.09.090 |
| [10] |
Makansi M, Hutter M, Theilen TM, et al. Comparison of perioperative outcomes between laparoscopic and open partial splenectomy in children and adolescents[J]. World J Gastrointest Surg, 2021, 13(9): 979-987. DOI:10.4240/wjgs.v13.i9.979 |
| [11] |
Liu GS, Fan Y. Feasibility and safety of laparoscopic partial splenectomy: a systematic review[J]. World J Surg, 2019, 43(6): 1505-1518. DOI:10.1007/s00268-019-04946-8 |
| [12] |
Redmond HP, Redmond JM, Rooney BP, et al. Surgical anatomy of the human spleen[J]. Br J Surg, 1989, 76(2): 198-201. DOI:10.1002/bjs.1800760230 |
| [13] |
闫学强, 朱真闯, 匡后芳, 等. 悬吊技术在儿童腹腔镜脾部分切除术中的应用[J]. 中华小儿外科杂志, 2025, 46(3): 232-236. Yan XQ, Zhu ZC, Kuang HF, et al. Application of suspension technique in the treatment of laparoscopic partial splenectomy in children[J]. Chin J Pediatr Surg, 2025, 46(3): 232-236. DOI:10.3760/cma.j.cn421158-20240328-00141 |
| [14] |
刘立国, 谭海东, 黄笳, 等. 腹腔镜脾部分切除术治疗脾脏实性肿瘤的临床分析[J]. 中华普通外科杂志, 2018, 33(5): 398-400. Liu LG, Tan HD, Huang J, et al. Laparoscopic partial splenectomy for splenic solid lesions[J]. Chin J Gen Surg, 2018, 33(5): 398-400. DOI:10.3760/cma.j.issn.1007-631X.2018.05.010 |
| [15] |
Berelavichus SV, Smirnov AV, Ionkin DA, et al. Robot-assisted and laparoscopic partial splenectomy for nonparasitic cysts[J]. Khirurgiia (Mosk), 2015, 7: 41-48. DOI:10.17116/hirurgia2015741-48 |
 2026, Vol. 25
2026, Vol. 25


