2. 河北省人民医院麻醉科, 石家庄 050000
2. Department of Anesthesiology, Hebei Provincial People's Hospital, Shijiazhuang 050000, China
神经母细胞瘤(neuroblastoma, NB)是儿童最常见的颅外实体瘤,约占所有儿童癌症的8% ~10%[1]。由于其高度侵袭性,近半数患儿确诊时已发生转移,导致该疾病占儿童癌症死亡病例的15%左右[2]。神经母细胞瘤具有显著的临床异质性,根据INRG风险分层系统可分为不同危险组别,其中低中危患儿预后良好,而高危患儿长期生存率仍低于50%[3-4]。
当前多模式治疗虽可改善高危患儿预后,但常伴随生长障碍、继发性癌症等严重并发症[5]。因此,建立快速、准确的风险分层指标对实现个体化治疗至关重要。系统免疫炎症指数(systemic immune-inflammation index, SII)作为一种基于外周血细胞计数的炎症标志物,已在多种成人及部分儿童实体瘤中证实其预后价值[6-8]。然而,SII与传统国际神经母细胞瘤风险小组(International Neuroblastoma Risk Group, INRG)分层联合应用于神经母细胞瘤预后的研究尚属空白。本研究旨在探讨SII联合INRG危险分层在神经母细胞瘤患儿预后评估中的价值。
资料与方法 一、研究对象本研究为回顾性研究,以2013年1月至2024年11月于河北省儿童医院确诊为神经母细胞瘤并住院接受手术的166例患儿为研究对象。病例纳入标准:①依据组织病理学诊断、骨髓细胞学涂片检查及活检诊断确诊的神经母细胞瘤;②接受肿瘤根治切除术;③具备完整的术前1周血液成分检测结果。排除标准:①严重感染或免疫缺陷;②合并其他恶性肿瘤;③随访资料不完整。本研究经河北儿童医院医学研究伦理委员会批准(202430)。
二、数据收集对患儿的性别、年龄、组织病理类型、危险度分级、影像学特征(肿瘤位置、大小、有无转移)、化疗情况和实验室指标(血常规、LDH)进行了回顾性收集。考虑到新辅助化疗的影响,于术前1周内的抽取患儿空腹静脉血进行血清学指标测定,抽取时所有患儿均未出现发热症状(腋下温度不高于37.28℃)或任何形式的活动性感染、慢性炎症。从测定结果中提取中性粒细胞(×109/L)、淋巴细胞(×109/L)和血小板计数(×109/L)水平。SII计算方法如下:SII=外周血小板×中性粒细胞/淋巴细胞计数。将SII和INRG危险度分级联合,拟合的新的预后指标:“SII+INRG分级”,其具体判定标准如下:“低SII+非高危INRG分级”判定为低危,“低SII+高危INRG分级”或“高SII+非高危INRG分级”判定为中危,“高SII+高危INRG分级”判定为高危。
三、术后随访所有患儿在术后的前3年内,每3个月随访1次,随后6个月1次。随访期间根据《NCCN肿瘤学临床实践指南》采集临床病史、进行体格检查、测量外周肿瘤生物标记物水平,并进行腹部和盆腔计算机断层扫描或超声检查。总生存期(overall survival rate,OS)是指从初次治疗到患儿死亡之间的时间。无事件生存期(event-free survival,EFS)是指从初次治疗起至首次出现疾病进展、复发之间的时间。
四、统计学处理所有统计分析均使用GraphPad Prism 9.5.1.733 for Windows进行。连续变量以x±s或M(Q1, Q3)表示,分类变量以频率和百分比表示,并使用卡方检验进行比较。建立SII的ROC曲线来评估其与复发和死亡关系,通过约登指数(Youden index)值来定义最佳的SII截断值。约登指数是指ROC曲线中的灵敏度+特异度-1。使用Kaplan-Meier生存曲线估计OS和EFS,Log-rank检验用于比较组间差异。采用单因素和多因素Cox回归分析估计SII、INRG分级、SII+INRG分级对OS的影响(单因素分析中P < 0.05的变量被纳入多因素分析)。P < 0.05为差异有统计学意义。
结果 一、患儿基本特征本研究共纳入166例NB患儿,其中存活组144例,死亡组22例。对比两组基线特征发现,存活组在较小的肿瘤直径(χ2=7.551, P=0.006)、高危INRG危险分级(χ2=42.024, P < 0.001)、无远处转移(χ2=16.000, P < 0.001)、未接受化疗(χ2=7.331, P=0.007)以及较低SII水平(χ2=41.854, P < 0.001)方面显著优于死亡组,见表 1。
| 表 1 存活组和死亡组神经母细胞瘤患儿基线资料比较 Table 1 Comparison of baseline profiles between survivors and non-survivors with NB |
|
|
在NB患儿中,根据INRG分级,高危组与非高危组的SII的分布情况具有差异性。高危组患儿的SII值[549.29(219.04, 1234.80)]普遍高于非高危组[247.42(143.47, 364.68)],且两组之间的差异具有统计学意义(P < 0.01)。高SII与低SII患儿在不同生存状态组的分布亦具有差异性,其中高SII患儿在死亡组中占比90.91%;在存活组中占比22.22%;在疾病进展组中占70.37%;在未进展组中占12.95%。
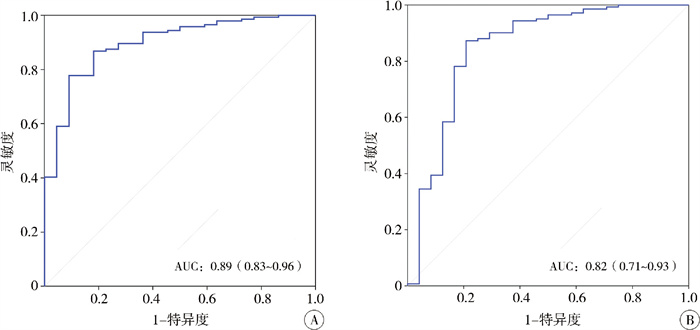
三、SII对总生存和无事件生存结局的预测针对死亡和疾病进展,绘制了SII的ROC曲线,具体见图 1A、1B,SII预测死亡结局的曲线下面积AUC值为0.89(95%CI:0.83~0.96),其临界值为428.74;预测疾病进展结局的曲线下面积AUC值为0.82(95%CI:0.71~0.93),其临界值为582.52。SII在死亡和疾病进展的预测中均显示出较高的AUC值。根据约登指数确定的截断值,将SII分为高SII和低SII组。
|
图 1 基于SII预测死亡(A)和疾病进展(B)的ROC曲线 Fig.1 ROC curves for predicting death (A) and disease progression (B) based upon SII |
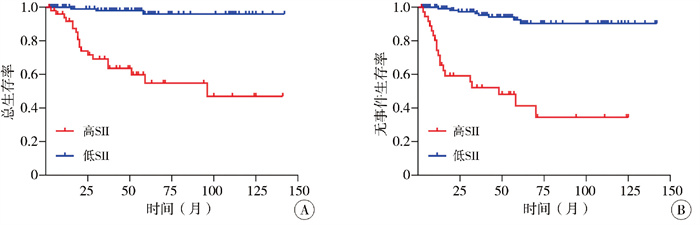
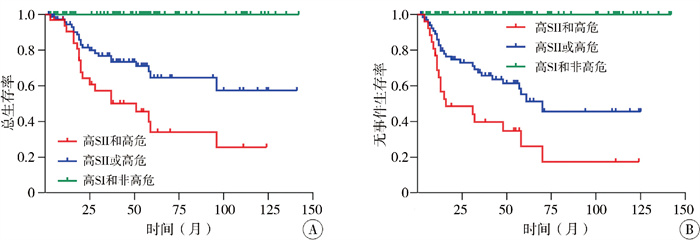
利用三种炎症指标的截断值,绘制了Kaplan-Meier生存曲线(图 2)。分析结果显示,高SII组与低SII组相比,患儿的5年OS显著降低(54.91%比95.31%,P < 0.001);EFS显著降低(41.32%比90.37%,P < 0.001)。将SII与NB的INRG危险分级联合进一步分析,结果表明SII与NB的INRG危险分级联合使用,能更有效地预测OS和EFS(图 3)。高SII且合并高危等级的患儿,其OS和EFS明显降低。
|
图 2 NB患儿Kaplan-Meier生存曲线:基于SII的OS(A)和EFS(B) Fig.2 Kaplan-Meier survival curves in NB children: OS (A) and EFS (B) by SII levels |
|
图 3 NB患儿Kaplan-Meier生存分析:基于SII及INRG危险分级的OS与EFS比较 Fig.3 Kaplan-Meier survival analysis in NB children: Comparison of OS and EFS based upon SII and INRG risk stratification 注 A: OS与SII及INRG危险分级的关系; B: EFS与SII及INRG危险分级的关系 |
我们采用单因素及多因素Cox回归评估SII+INRG分级的预后价值(表 2)。将SII与INRG分级整合,构建“SII+INRG分级”模型,定义为:低SII+非高危为低危,低SII+高危或高SII+非高危为中危,高SII+高危为高危。多因素分析中,高SII(HR=19.70, 95%CI: 3.98~97.61, P < 0.001)、高LDH(HR=4.74, 95%CI: 1.34~16.75, P < 0.05)及高危INRG(HR=14.11, 95%CI: 1.84~108.25, P < 0.05)为总生存结局的独立危险因素。而“SII+INRG分级”高危组在OS(HR=36.19, 95%CI: 10.50~124.75, P < 0.001)中表现出最高的风险比,提示其联合模型具有更强的预后预测能力。
| 表 2 SII+INRG危险分级对于总生存结局的单因素和多因素Cox回归分析 Table 2 Univariate and multivariate Cox regression analysis of SII+INRG for overall survival |
|
|
NB是儿童最常见的实体瘤之一,尤其在2岁以下儿童中发病率较高(占所有儿童癌症的8% ~10%)[1, 9]。尽管现代治疗方法已显著提高了低危和中危NB的生存率,但对于高危NB患儿,特别是在晚期阶段,预后依然较差[10-11]。本研究中,166名患儿中高风险组占34.34%,其中约16%发生复发,13.25%的患儿死亡,提示高危NB的预后仍不容乐观。预后评估的精准性对于制定个性化治疗方案至关重要[5]。炎症与肿瘤的发生和进展密切相关,近年研究发现,炎症标志物在多种成人及儿童肿瘤中具有重要的预后意义[7, 12]。在本研究中,我们系统地评估了SII联合INRG分级对NB患儿预后的影响。
我们的数据表明,SII在死亡和疾病进展的预测中具有较高的ROC曲线下面积,分别为0.89和0.82,提示它们在预测NB患儿的预后方面具有较强的效能。根据Kaplan-Meier生存曲线分析,高SII的患儿在五年OS和EFS上显著低于低SII的患儿。这一发现符合先前的研究,高水平SII与肿瘤的不良预后密切相关,这在多种肿瘤的研究中得到证明[13-14]。值得注意的是,SII在神经母细胞瘤中与INRG危险度分级的结合,能够更好地预测患儿的生存和复发风险,目前尚未有相关方面的研究。我们的数据表明,高SII与高危患儿的低生存率和高疾病进展风险显著相关,这提示这些炎症指标可以作为有效的临床工具与INRG危险分级联合,用于帮助患儿在治疗前进行风险分层。
我们通过多因素Cox回归分析验证了SII在NB预后中的独立价值。尽管INRG危险度分级和高LDH水平已被广泛认可为NB预后不良的标志,但SII与INRG危险度分级的联合分析进一步揭示了其在预后判断中的独特作用。通过构建“SII+INRG分级”的新预后指标,我们发现SII与INRG危险度分级的联合能够显著提高预后分层的准确性,尤其是在总生存结局分析中,SII+INRG分级高危组的HR值远高于单独的SII或INRG分级。
炎症反应在肿瘤的发生、发展及转移过程中起着至关重要的作用。大量研究表明,炎症可通过多种途径促进肿瘤细胞的增殖、存活、血管生成及免疫逃逸,进而加速肿瘤的进展[15]。在肿瘤微环境中,持续的炎症反应不仅改变了免疫细胞的功能,还促进了肿瘤相关细胞因子和趋化因子的分泌,这些分子不仅支持肿瘤细胞的生长,还能抑制宿主的免疫监视功能[16]。
炎症通过改变肿瘤微环境中的细胞成分,尤其是免疫细胞的功能,进一步影响肿瘤的进展和预后。在神经母细胞瘤中,肿瘤相关巨噬细胞(tumor-associated macrophages,TAM)和髓系来源的抑制性细胞(Myeloid-derived suppressor cells,MDSCs)在肿瘤中大量存在[17],肿瘤相关巨噬细胞的高水平存在不仅促使肿瘤的生长和血管生成,还能通过分泌促炎症因子,如TNF-α、IL-1β等,进一步增强局部炎症反应,抑制抗肿瘤免疫反应,从而促进肿瘤的侵袭性和转移[18]。肿瘤免疫逃逸是炎症在肿瘤进展中的关键作用之一。炎症微环境不仅为肿瘤提供了免疫逃逸的机会,还通过调节免疫细胞的功能,削弱了宿主的抗肿瘤免疫反应。肿瘤相关的免疫抑制性细胞(如MDSCs)通过分泌抑制性因子(如IL-10和TGF-β),抑制CD8+T细胞的抗肿瘤活性,从而增强肿瘤的免疫逃逸能力[19]。
通过将SII与INRG危险度分级结合,我们不仅增强了预后判断的准确性,还为临床实践提供了一个更实用的评估工具。“SII+INRG分级”在NB的预后评估中具有重要的临床应用价值。通过这一新的预后指标,临床医生可以更精准地识别高危患儿,并为其制定更个性化的治疗方案。此外,SII作为一种基于血液标志物的指标,具有无创、易获取的特点,能够为临床预后评估提供更便捷的手段。在基层医疗机构中,SII的低成本和易获取性使其成为一种理想的预后评估工具。基层医院通常缺乏先进的检测设备和技术人员,而SII的检测仅需常规的血液检查即可完成,这大大降低了对医疗资源的需求。此外,SII的无创性避免了对患儿的额外伤害,进一步提高了其在临床实践中的适用性未来的研究可以进一步探讨SII在不同临床亚组中的表现,并验证其与其他已知预后因素(如MYCN扩增、肿瘤分期等)的联合应用效果。此外,随着技术的不断进步,新的炎症相关标志物和评分系统可能进一步提高预后评估的精确性和敏感性。
尽管本研究为神经母细胞瘤的炎症标志物提供了重要的预后数据,但仍存在一些局限性。首先本研究为单中心回顾性研究,且样本量较小,结果应谨慎解释。其次,本研究中SII的临界值是在我们的队列中通过约登指数确定的,需要进一步的分析来确定以这种方式是否适用于其他队列。此外,SII的具体生物学机制尚未完全明确,未来研究可以进一步探索其在神经母细胞瘤中的作用机制,以及与其他预后标志物的联合应用潜力。未来的大规模前瞻性研究可进一步验证这些结果的普适性,并探讨炎症标志物在不同治疗模式中的作用。
综上所述,本研究验证了SII在NB患儿预后评估中的潜在价值。SII作为系统性炎症指标,能够有效地预测NB患儿的死亡和疾病进展风险,并可与患儿的INRG危险分级联合使用,以提高预后评估的精度。基于炎症反应的评估方法,具有快捷、简便和经济的优势,可为NB的临床治疗提供有力支持。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 文献检索为张成龙、王晓宇;研究设计为张成龙、耿建磊;数据分析为张成龙、王晓宇;初稿撰写为张成龙、耿建磊;稿件审阅与修改为牛会忠、张鹏举
| [1] |
Castleberry RP. Neuroblastoma[J]. Eur J Cancer, 1997, 33(9): 1430-1437. DOI:10.1016/s0959-8049(97)00308-0 |
| [2] |
Cohn SL, Pearson ADJ, London WB, et al. The International Neuroblastoma Risk Group (INRG) classification system: an INRG Task Force report[J]. J Clin Oncol, 2009, 27(2): 289-297. DOI:10.1200/JCO.2008.16.6785 |
| [3] |
Maris JM. Recent advances in neuroblastoma[J]. N Engl J Med, 2010, 362(23): 2202-2211. DOI:10.1056/NEJMra0804577 |
| [4] |
Wienke J, Dierselhuis MP, Tytgat GAM, et al. The immune landscape of neuroblastoma: challenges and opportunities for novel therapeutic strategies in pediatric oncology[J]. Eur J Cancer, 2021, 144: 123-150. DOI:10.1016/j.ejca.2020.11.014 |
| [5] |
Tolbert VP, Matthay KK. Neuroblastoma: clinical and biological approach to risk stratification and treatment[J]. Cell Tissue Res, 2018, 372(2): 195-209. DOI:10.1007/s00441-018-2821-2 |
| [6] |
Terasaki F, Sugiura T, Okamura Y, et al. Systemic immune-inflammation index as a prognostic marker for distal cholangiocarcinoma[J]. Surg Today, 2021, 51(10): 1602-1609. DOI:10.1007/s00595-021-02312-7 |
| [7] |
Nayak A, McDowell DT, Kellie SJ, et al. Elevated preoperative neutrophil-lymphocyte ratio is predictive of a poorer prognosis for pediatric patients with solid tumors[J]. Ann Surg Oncol, 2017, 24(11): 3456-3462. DOI:10.1245/s10434-017-6006-0 |
| [8] |
Kunc M, Gabrych A, Dulak D, et al. Systemic inflammatory markers and serum lactate dehydrogenase predict survival in patients with Wilms tumour[J]. Arch Med Sci, 2022, 18(5): 1253-1261. DOI:10.5114/aoms/125543 |
| [9] |
Swift CC, Eklund MJ, Kraveka JM, et al. Updates in diagnosis, management, and treatment of neuroblastoma[J]. Radiographics, 2018, 38(2): 566-580. DOI:10.1148/rg.2018170132 |
| [10] |
Maris JM, Hogarty MD, Bagatell R, et al. Neuroblastoma[J]. Lancet, 2007, 369(9579): 2106-2120. DOI:10.1016/S0140-6736(07)60983-0 |
| [11] |
王鹏程, 董瑞. 神经母细胞瘤4S期预后不良相关因素的研究进展[J]. 临床小儿外科杂志, 2022, 21(4): 394-398. Wang PC, Dong R. Research advances on poor prognostic factors of children with stage 4S neuroblastoma[J]. J Clin Ped Sur, 2022, 21(4): 394-398. DOI:10.3760/cma.j.cn101785-202108053-019 |
| [12] |
Diakos CI, Charles KA, McMillan DC, et al. Cancer-related inflammation and treatment effectiveness[J]. Lancet Oncol, 2014, 15(11): e493-e503. DOI:10.1016/S1470-2045(14)70263-3 |
| [13] |
Jomrich G, Paireder M, Kristo I, et al. High systemic immune-inflammation index is an adverse prognostic factor for patients with gastroesophageal adenocarcinoma[J]. Ann Surg, 2021, 273(3): 532-541. DOI:10.1097/SLA.0000000000003370 |
| [14] |
Toyoda J, Sahara K, Maithel SK, et al. Prognostic utility of systemic immune-inflammation index after resection of extrahepatic cholangiocarcinoma: results from the U.S.Extrahepatic Biliary Malignancy Consortium[J]. Ann Surg Oncol, 2022, 29(12): 7605-7614. DOI:10.1245/s10434-022-12058-2 |
| [15] |
Greten FR, Grivennikov SI. Inflammation and cancer: triggers, mechanisms, and consequences[J]. Immunity, 2019, 51(1): 27-41. DOI:10.1016/j.immuni.2019.06.025 |
| [16] |
Zhao HK, Wu L, Yan GF, et al. Inflammation and tumor progression: signaling pathways and targeted intervention[J]. Signal Transduct Target Ther, 2021, 6(1): 263. DOI:10.1038/s41392-021-00658-5 |
| [17] |
Yang L, Lin PC. Mechanisms that drive inflammatory tumor microenvironment, tumor heterogeneity, and metastatic progression[J]. Semin Cancer Biol, 2017, 47: 185-195. DOI:10.1016/j.semcancer.2017.08.001 |
| [18] |
Wang MN, Chen SY, He XM, et al. Targeting inflammation as cancer therapy[J]. J Hematol Oncol, 2024, 17(1): 13. DOI:10.1186/s13045-024-01528-7 |
| [19] |
Decock J, Comito G, Zaravinos A. Editorial: tumor microenvironment, inflammation, and resistance to immunotherapies[J]. Front Oncol, 2023, 13: 1215332. DOI:10.3389/fonc.2023.1215332 |
 2026, Vol. 25
2026, Vol. 25


