2. 中南大学湘雅医学院附属儿童医院(湖南省儿童医院)康复中心, 长沙 410007
2. Rehabilitation Center, Affiliated Children's Hospital, Xiangya School of Medicine, Central South University (Hunan Children's Hospital), Changsha 410007, China
儿童脑积水是神经外科常见疾病,多由脑脊液循环障碍引发脑室系统扩大,常需手术干预以缓解颅内压增高、改善神经功能[1-2]。目前临床主流术式为脑室- 腹腔分流术(ventriculoperitoneal shunt, VPS)与内镜下第三脑室造瘘术(endoscopic third ventriculostomy, ETV),虽能有效控制病情,但术后30天内仍面临分流管梗阻、感染等治疗失败风险,不仅延长患儿住院时间,还可能加重神经损伤,影响预后[3-6]。既往研究报道,儿童脑积水术后30天内治疗失败率达15% ~25%,但缺乏可靠的临床预测工具辅助风险分层[7-10]。本研究回顾性分析儿童脑积水患者的临床资料,筛选术后30天内治疗失败的独立危险因素,构建列线图预测模型,为临床医师提供量化风险评估工具,助力制定针对性诊疗策略。
资料与方法 一、研究对象本研究为病例对照研究,以2016年7月至2025年9月于湖南省儿童医院神经外科接受手术治疗的儿童脑积水患者为研究对象。病例纳入标准:①年龄≤18岁;②符合《中国儿童脑积水外科治疗及并发症处理专家共识(2022)》中脑积水诊断标准[11],且经头颅MRI/CT证实;③首次接受脑积水手术治疗(VPS或ETV);④临床资料完整(含人口学特征、病因、影像学资料、手术记录、术后30天随访数据)。排除标准:①合并严重心、肝、肾等多器官功能衰竭;②合并恶性肿瘤终末期或严重遗传代谢性疾病;③术后30天内失访或因非治疗失败相关原因死亡(如严重感染性休克、多器官功能障碍综合征);④既往接受过脑积水手术治疗(如分流管置换、再次造瘘);⑤医源性技术性失败所致的失败事件(如导管定位/长度选择不当、固定/隧道失败、造瘘口未达解剖位点、术中异物操作等)。所有患儿术前均签署知情同意书,手术指征和方案由经验丰富的神经外科主任医师确定。本研究经湖南省儿童医院伦理委员会批准(HCHLL-2025-368),因回顾性研究豁免患儿及家属知情同意。
二、变量定义因变量:术后30天内治疗失败参考《中国儿童脑积水外科治疗及并发症处理专家共识(2022)》[11]定义,包括以下任一情况:①症状性分流管梗阻:术后出现头痛、呕吐、烦躁、意识障碍等颅内压增高症状,头颅CT/MRI提示脑室较术前扩大,需手术干预;②术后感染:术后出现发热(体温≥38.5℃),脑脊液检查提示白细胞计数>10×106/L、糖定量 < 2.2 mmol/L或蛋白定量>0.45 g/L,且脑脊液培养阳性,或临床高度怀疑感染(如脑膜刺激征阳性)并经抗感染治疗后症状缓解;③严重并发症:如分流管移位/断裂、颅内出血(出血量≥10 mL)、腹腔端并发症(如脏器损伤、肠梗阻),需二次手术处理。
自变量:①人口学特征:年龄(< 1岁、1~3岁、>3岁)、性别(男、女)、胎龄(早产儿:胎龄 < 37周,足月儿:胎龄≥37周);②疾病特征:病因(出血相关:新生儿颅内出血、脑外伤后出血继发脑积水;发育/先天畸形:中脑导水管狭窄、Dandy-Walker畸形等;感染相关:化脓性脑膜炎、结核性脑膜炎后脑积水;囊肿:蛛网膜囊肿、脉络丛囊肿继发脑积水;外伤:脑外伤后蛛网膜下腔粘连所致脑积水;肿瘤相关:脑肿瘤(如髓母细胞瘤、室管膜瘤)压迫或阻塞脑室系统所致脑积水)、脑积水类型(交通性、非交通性、混合性)、术前临时引流(是/否)、手术方式(VPS/ETV);③影像学指标:额- 枕角比(fronto-occipital horn ratio, FOHR):术前行头颅MRI/CT检查,于脑室水平轴位双侧Monro孔层面,测量双侧侧脑室额角内侧壁间距(F)、枕角内侧壁间距(O)及同层面最大颅骨内径(BPD),FOHR计算公式为:
采用SPSS 26.0及R 4.5进行统计分析。列线图构建采用“rms”包,受试者操作特征(receiver operating characteristic, ROC)曲线分析采用“pROC”包,决策曲线分析(decision curve analysis,DCA)采用“rmda”包。服从正态分布的计量资料以x±s表示,组间比较采用两独立样本t检验;不服从正态分布的计量资料以M(Q1,Q3)表示,组间比较采用Mann-Whitney U检验;计数资料以例(%)表示,组间比较采用χ2检验。险因素筛选与模型构建:逐一分析各自变量与术后30天内失败的关联:分类变量采用χ2检验,连续变量(如年龄、胎龄)先分组后分析,筛选P < 0.05的变量进入多因素分析;采用逐步回归法(前进法,α入=0.05,α出=0.10),以术后30天内失败为因变量(赋值:失败=1,成功=0),纳入单因素分析P < 0.05的变量为自变量,分析独立危险因素;同时引入“手术方式×病因”交互项,检验其交互效应;基于多因素Logistic回归的独立危险因素,采用“rms”包构建列线图,通过累加各因素评分得到总评分,进而对应术后30天内失败的预测概率。模型效能评估:①判别效能:绘制ROC曲线,计算曲线下面积(area under curve, AUC);②校准度:绘制校准曲线,采用Hosmer-Lemeshow检验(将患者按预测概率分为10组),P>0.05提示模型预测概率与实际概率拟合良好;③临床适用性:绘制DCA曲线,计算不同阈值概率下模型的净获益,模型曲线位于“全部治疗”或“全部不治疗”曲线之上提示临床适用性良好;④内部验证:采用Bootstrap重采样法(1 000次)评估模型稳定性与泛化能力。P < 0.05为差异有统计学意义。
结果共纳入326例儿童脑积水患者,其中男189例(58.0%),女137例(42.0%);年龄中位数为1.5(0.3,5.0)岁,其中 < 1岁128例(39.3%)、1~3岁105例(32.2%)、>3岁93例(28.5%);胎龄:早产儿68例(20.9%),足月儿258例(79.1%);病因:出血相关72例(22.1%)、发育/先天畸形98例(30.1%)、感染相关65例(19.9%)、囊肿32例(9.8%)、外伤28例(8.6%)、肿瘤相关31例(9.5%);脑积水类型:交通性142例(43.6%)、非交通性158例(48.5%)、混合性26例(8.0%);术前临时引流:是89例(27.3%),否237例(72.7%);手术方式:VPS 203例(62.3%),ETV 123例(37.7%);FOHR:轻- 中度225例(69.0%),重度101例(31.0%)。术后30天内治疗失败68例(失败率20.86%),其中分流管梗阻29例(42.6%)、术后感染21例(30.9%)、严重并发症18例(26.5%);治疗成功258例(79.14%)。
单因素分析结果显示,病因(出血相关、感染相关)、手术方式(ETV)、FOHR(重度)与术后30天内失败相关(P < 0.05);年龄、性别、胎龄、脑积水类型、术前临时引流及其他病因(发育/先天畸形、囊肿、外伤、肿瘤相关)与术后30天内失败无显著关联(P>0.05)。见表 1。
| 表 1 儿童脑积水术后30天内治疗失败的单因素分析[例(%)] Table 1 Univariate analysis of failure within 30 days postoperative for pediatric hydrocephalus surgery[n(%)] |
|
|
多因素Logistic回归分析结果显示:额- 枕角比≥60%(OR=3.826,95%CI:2.154~6.798)、感染相关病因(OR=3.215,95%CI:1.732~5.976)、出血相关病因(OR=2.783,95%CI:1.462~5.297)及手术方式为内镜下第三脑室造瘘术(相对于脑室- 腹腔分流术)(OR=2.517,95%CI:1.389~4.558)为脑积水术后30天内治疗失败的独立危险因素。见表 2。
| 表 2 儿童脑积水术后30天内治疗失败的多因素Logistic回归分析 Table 2 Multivariate Logistic regression analysis of failure within 30 days post-operation for pediatric hydrocephalus |
|
|
进一步引入“手术方式×病因”交互项分析,结果显示两者存在显著交互作用(P=0.013):①出血相关病因患者中,ETV术后失败风险是VPS的2.399倍(OR=2.399,95%CI:1.062~5.408,P=0.033);②感染相关病因患者中,ETV术后失败风险是VPS的2.491倍(OR=2.491,95%CI:1.078~5.756,P=0.030);③发育/先天畸形、囊肿、外伤、肿瘤相关病因患者中,两种术式失败风险差异无统计学意义(OR=1.240,95%CI:0.618~2.488,P=0.576)。见表 3。
| 表 3 儿童脑积水术后30天内治疗失败手术方式与病因的交互效应分析 Table 3 Interaction analysis between surgical approach and etiology |
|
|
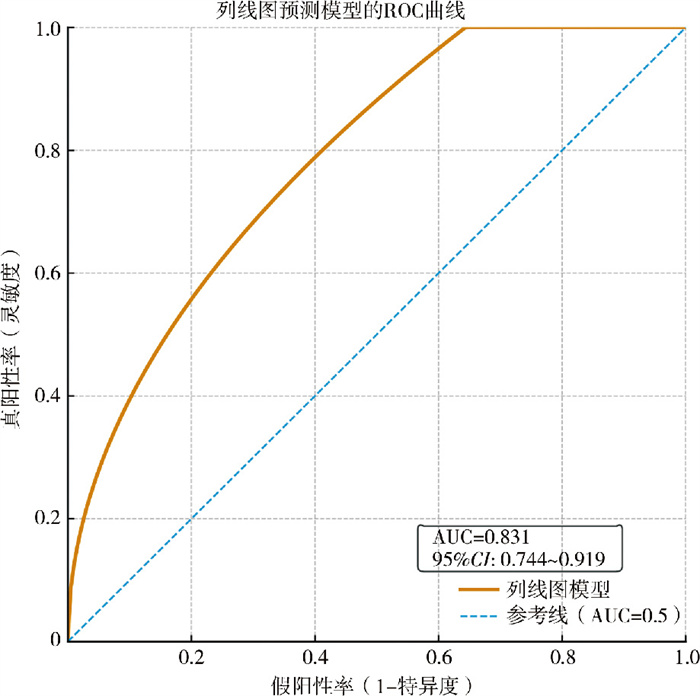
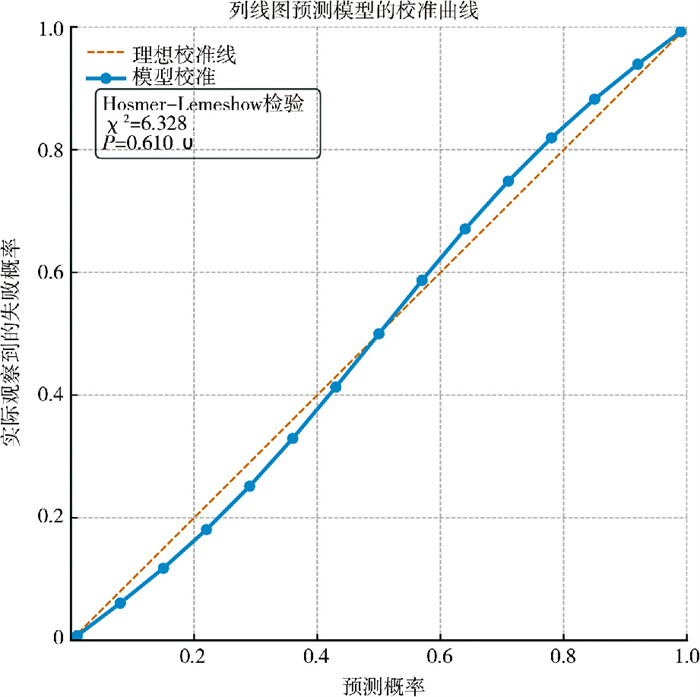
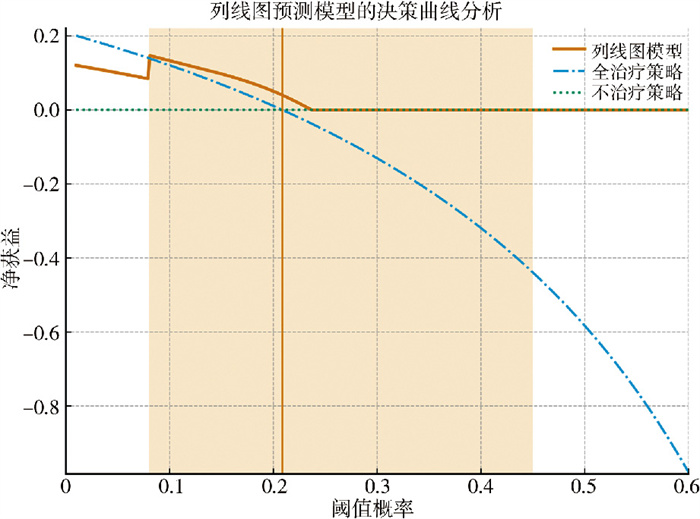
基于多因素Logistic回归分析确定的独立危险因素(病因、手术方式、FOHR),构建列线图模型;采用ROC曲线评估列线图模型的判别效能,结果显示AUC为0.831(95%CI:0.744~0.919),提示模型具有中等判别效能(图 1)。通过校准曲线及Hosmer-Lemeshow检验评估模型校准度。校准曲线显示,列线图预测的失败概率与患者实际失败概率贴合紧密,预测值与实际值基本分布在对角线附近(图 2);Hosmer-Lemeshow检验结果为χ2=6.328、P=0.610,提示模型校准度优良,预测概率与实际发生概率无显著差异。DCA曲线分析显示(图 3):当临床阈值概率在8% ~45%范围内时,列线图模型对应的净获益曲线显著高于“全部治疗”策略(假设所有患者均会失败并采取干预措施)和“全部不治疗”策略(假设所有患者均不会失败且不采取干预措施);当阈值概率 < 8%时,“全部不治疗”策略净获益更高;当阈值概率>45%时,“全部治疗”策略净获益更高。结合儿童脑积水术后30天失败率(20.86%),提示该模型在临床常用阈值范围内(8% ~45%) 具有良好的临床适用性,可帮助临床医师筛选高风险患者并制定干预策略。
|
图 1 儿童脑积水术后30天内治疗失败预测列线图的ROC曲线 Fig.1 ROC Curve for predictive cut-off line chart of treatment failure within 30 days post-operation for pediatric hydrocephalus |
|
图 2 儿童脑积水术后30天内治疗失败预测列线图的校准曲线 Fig.2 Calibration curve for predictive regression model of treatment failure within 30 days post-operation for pediatric hydrocephalus |
|
图 3 儿童脑积水术后30天内治疗失败列线图模型临床适用性的决策曲线分析 Fig.3 Decision curve analysis of clinical applicability of a line chart model for treatment failure within 30 days post-operation for pediatric hydrocephalus |
本研究基于326例儿童脑积水患者的临床资料,系统分析术后30天内治疗失败的相关因素并构建风险预测列线图模型,结果表明:脑积水病因、术式选择及术前脑室扩张程度是影响术后短期失败的关键因素,基于上述独立危险因素建立的列线图模型具有较好的区分度和校准度,可为个体患儿术后30天内失败概率的预测提供参考。
本研究显示,感染与出血相关病因可显著升高术后30天失败风险,符合脑积水的病理生理特点:①感染相关脑积水(如化脓性/结核性脑膜炎后)常因蛛网膜颗粒功能受损、黏连广泛,术后易出现分流阻塞或感染;炎症可导致脑脊液蛋白与细胞成分升高,易沉积堵管并降低ETV造瘘口通畅率[8, 12]。国内文献提示,重度颅内感染可致脑室纤维化与炎细胞浸润,增加引流困难及失败风险[13-14]。②出血相关脑积水(如早产儿IVH)因血液降解产物滞留,易引发分流管阻塞与脑膜黏连,既往研究指出儿童初次分流早期失效与脑室内出血独立相关,30天失败风险约增4倍[8]。此外,本研究证实FOHR≥0.60(重度脑室扩张)是术后短期失败的独立危险因素。重度脑积水反映病程更长、脑室壁顺应性下降及循环障碍更复杂,分流后易发生过度引流、硬膜下并发症而需再手术;且重度脑积水多伴慢性过程与膜性重塑,术后难以迅速恢复正常动力学[15],故无论分流或造瘘均更易早期失败,临床需高度重视。本研究还发现,出血/感染病因下ETV短期失败率显著高于VPS,交互分析显示该亚组ETV失败风险约为VPS的2.4倍;而先天发育异常、囊肿、肿瘤等梗阻性病因中,两术式差异无显著。这与ETV的临床应用特点相符:年龄较大且纯梗阻性脑积水患儿行ETV的成功率较高,而小婴儿及感染、出血继发脑积水患儿的成功率较低[12]。部分中心报告[12],感染/出血所致脑积水中ETV成功率接近0%,主要因脑脊液吸收通路广泛受损;而VPS通过直接引流脑脊液,在此类脑脊液循环障碍中更具优势,但植入异物也可能增加感染风险。因此,感染或出血相关病因患儿宜优先选择VPS以降低早期失败风险;梗阻性且年龄较大的患儿,ETV作为无植入方案具有感染风险低等优势,短期疗效不亚于VPS。
本研究关于感染、出血相关脑积水短期失败率更高的结论,与Orrego-Gonzáalez等[8]、Hauptman等[16]的研究结果一致:Orrego-Gonzáalez等[8]在83例初次分流患儿中发现1个月内失效率达25.3%,其中新生儿脑室出血相关风险最高;Hauptman等[16]多中心前瞻性研究提示,病因为快速失效的关键因素(P=0.005),感染后与出血后脑积水更易出现≤30天失败。巫瑞[17]系统综述认为ETV与VPS总体成功率接近,但并发症构成不同:ETV可降低植入相关感染,而VPS在复杂脑积水中不可替代。本研究进一步证实病因与术式的交互作用,即感染/出血相关人群中分流术短期效果优于造瘘,而先天畸形、肿瘤等梗阻性病因中两术式短期成功率无显著差异,符合梗阻性脑积水患儿可选择ETV以避免植入异物的临床共识。但本研究未观察到年龄对失败率的独立影响;术前临时引流也未显示独立关联,而Orrego-Gonzáalez等[8]提示其可能增加早期失败。推测差异与中心管理策略(如感染控制、择期手术时机)及混杂因素控制有关,提示临床决策应综合病因与影像指标,而非依赖单一因素。此外,本研究将FOHR纳入分析并证实其预后价值,与Tatoshvili等[15]的研究结果一致, Tatoshvili等[15]发现FOHR越小(≤0.56),ETV后维持无分流状态的概率越高,且FOHR独立于年龄与解剖学指标。传统ETV成功率评分未纳入脑室大小,本研究的创新在于用FOHR完善风险评估,解释了慢性高张力脑积水术后仍易出现硬膜下积液、需多次调整的现象。临床上应结合FOHR与解剖生理特征(如第三脑室底形态、导水管狭窄)综合判定[18-19]。
本研究构建的列线图模型聚焦术后30天内失败概率的预测,弥补了既有模型多聚焦长期分流存活或特定场景的不足。Zhou等[20]针对髓母细胞瘤术后脑积水发生构建列线图(AUC=0.85),但其应用场景为预测脑积水发生,而本研究面向已接受手术的患儿,评估短期再次失败风险,更契合围手术期决策需求。本模型AUC达0.831,校准良好,DCA显示在8%~45%阈值概率范围内具有净获益,提示该模型可有效辅助临床决策:①术前评估:输入患儿病因类别、FOHR值等信息,即可得到术后30天失败概率估计,高风险患儿(如失败率远高于20%且病因为感染/出血)可优先选择VPS并采取抗感染预防措施,术后加强监测;低风险患儿(如病因为肿瘤阻塞且FOHR适中)可首次尝试ETV以避免植入分流。②医患沟通:借助列线图可直观向家属解释患儿风险水平,提高家属依从性并配合围术期管理[21]。
本研究为单中心回顾性研究,病例来源、地区及医疗水平差异可能导致选择偏倚,模型外推性需谨慎;仅行内部验证,缺乏跨中心外部验证,不同医院术式偏好与围术期管理可能影响模型适用性;结局限定为术后30天早期失败,未能反映远期疗效与迟发性风险。未来应开展多中心、前瞻性研究,在不同地区与医院层级进行外部验证与参数校准;同时引入更丰富的变量与新技术(如影像组学、脑脊液生化标志物、手术学指标等),尝试机器学习以提升预测性能与识别潜在风险因子;临床应用上可开发手机或网页版计算工具,基于真实世界反馈迭代更新。
综上,本研究构建的列线图预测模型在儿童脑积水围手术期管理中具有潜在应用价值,可辅助术式选择、围术期干预及随访计划制定,对提高整体治疗效果、减少重复手术具有积极意义。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 张津维负责文献检索;张津维、苏君负责论文调查设计,张津维、袁丽平负责数据收集与统计学分析;张津维负责论文结果撰写;张津维、苏君、袁丽平、吴水华负责论文讨论分析;张津维、苏君、吴水华负责对文章知识性内容进行审阅
| [1] |
Whitehead WE, Weiner HL. Infantile and childhood hydrocephalus[J]. N Engl J Med, 2022, 387(22): 2067-2073. DOI:10.1056/NEJMra2116504 |
| [2] |
Bauer DF, Baird LC, Klimo P, et al. Congress of neurological surgeons systematic review and evidence-based guidelines on the treatment of pediatric hydrocephalus: update of the 2014 guidelines[J]. Neurosurgery, 2020, 87(6): 1071-1075. DOI:10.1093/neuros/nyaa434 |
| [3] |
Hanak BW, Bonow RH, Harris CA, et al. Cerebrospinal fluid shunting complications in children[J]. Pediatr Neurosurg, 2017, 52(6): 381-400. DOI:10.1159/000452840 |
| [4] |
Alvi MA, Bhandarkar AR, Daniels DJ, et al. Factors associated with early shunt revision within 30 days: analyses from the National Surgical Quality Improvement Program[J]. J Neurosurg Pediatr, 2022, 29(1): 21-30. DOI:10.3171/2021.7.PEDS21222 |
| [5] |
Kulkarni AV, Riva-Cambrin J, Holubkov R, et al. Endoscopic third ventriculostomy in children: prospective, multicenter results from the Hydrocephalus Clinical Research Network[J]. J Neurosurg Pediatr, 2016, 18(4): 423-429. DOI:10.3171/2016.4.PEDS163 |
| [6] |
Adebayo BO, Kanu OO, Bankole OB, et al. Early outcome of endoscopic third ventriculostomy with choroid plexus cauterization versus ventriculoperitoneal shunt as primary treatment of hydrocephalus in children with myelomeningocele: a prospective cohort study[J]. Oper Neurosurg (Hagerstown), 2021, 21(6): 461-466. DOI:10.1093/ons/opab314 |
| [7] |
Al-Tamimi YZ, Sinha P, Chumas PD, et al. Ventriculoperitoneal shunt 30-day failure rate: a retrospective international cohort study[J]. Neurosurgery, 2014, 74(1): 29-34. DOI:10.1227/NEU.0000000000000196 |
| [8] |
Orrego-González E, Enriquez-Marulanda A, Ravindran K, et al. Factors associated with ventriculoperitoneal shunt failures in the first 30 postoperative days in pediatric patients[J]. World Neurosurg, 2019, 124: e517-e526. DOI:10.1016/j.wneu.2018.12.125 |
| [9] |
Shahrestani S, Shlobin N, Gendreau JL, et al. Developing predictive models to anticipate shunt complications in 33, 248 pediatric patients with shunted hydrocephalus utilizing machine learning[J]. Pediatr Neurosurg, 2023, 58(4): 206-214. DOI:10.1159/000531754 |
| [10] |
Pahwa B, Bali O, Goyal S, et al. Applications of machine learning in pediatric hydrocephalus: a systematic review[J]. Neurol India, 2021, 69(Supplement): S380-S389. DOI:10.4103/0028-3886.332287 |
| [11] |
中华医学会神经外科分会小儿神经外科学组. 中国儿童脑积水外科治疗及并发症处理专家共识(2022)[J]. 中华小儿外科杂志, 2023, 44(10): 869-873. Group of Pediatric Neurosurgery, Committee of Neurosurgery, Chinese Medical Association. Chinese expert consensus on surgery and complication management of hydrocephalus in children (2022)[J]. Chin J Pediatr Surg, 2023, 44(10): 869-873. DOI:10.3760/cma.j.cn421158-20220429-00317 |
| [12] |
Ang J, Chua FHZ, Devi S, et al. Evaluation of the endoscopic third ventriculostomy success score for pediatric hydrocephalus: experience from a Singapore Children's Hospital[J]. Pediatr Neurosurg, 2025, 60(3): 64-73. DOI:10.1159/000546994 |
| [13] |
徐华中, 黄保胜. 自发性脑室出血后脑积水的危险因素分析[J]. 中国实用神经疾病杂志, 2020, 23(16): 1381-1385. Xu HZ, Huang BS. Risk factors for hydrocephalus in patients with spontaneous intraventricular hemorrhage[J]. Chin J Pract Nerv Dis, 2020, 23(16): 1381-1385. DOI:10.12083/SYSJ.2020.16.011 |
| [14] |
张毅, 沈淳, 薛萍, 等. 产前检查及手术策略对新生儿脑积水分流障碍的影响研究[J]. 临床小儿外科杂志, 2022, 21(9): 815-819. Zhang Y, Shen C, Xue P, et al. Effect of prenatal examination and surgical strategy for shunt outcome in neonatal hydrocephalus[J]. J Clin Ped Sur, 2022, 21(9): 815-819. DOI:10.3760/cma.j.cn101785-202204092-004 |
| [15] |
Tatoshvili D, Schaumann A, Tietze A, et al. Clinical and radiologic criteria to predict endoscopic third ventriculostomy success in non-communicating pediatric hydrocephalus[J]. Childs Nerv Syst, 2024, 41(1): 57. DOI:10.1007/s00381-024-06704-1 |
| [16] |
Hauptman JS, Kestle J, Riva-Cambrin J, et al. Predictors of fast and ultrafast shunt failure in pediatric hydrocephalus: a Hydrocephalus Clinical Research Network study[J]. J Neurosurg Pediatr, 2021, 27(3): 277-286. DOI:10.3171/2020.7.PEDS20111 |
| [17] |
巫瑞. 内镜下第三脑室造瘘术与脑室腹腔分流术治疗脑积水的疗效比较: 系统回顾和荟萃分析[D]. 重庆: 重庆医科大学, 2023. DOI: 10.27674/d.cnki.gcyku.2023.001855. Wu R. Effectives of endoscopic third ventriculostomy in hydrocephalus versus vebtriculoperitioneal shunt: systematic review and meta-analysis[D]. Chongqing: Chongqing Medical University, 2023. DOI: 10.27674/d.cnki.gcyku.2023.001855. |
| [18] |
Ragan DK, Cerqua J, Nash T, et al. The accuracy of linear indices of ventricular volume in pediatric hydrocephalus: technical note[J]. J Neurosurg Pediatr, 2015, 15(6): 547-551. DOI:10.3171/2014.10.PEDS14209 |
| [19] |
Foroughi M, Wong A, Steinbok P, et al. Third ventricular shape: a predictor of endoscopic third ventriculostomy success in pediatric patients[J]. J Neurosurg Pediatr, 2011, 7(4): 389-396. DOI:10.3171/2011.1.PEDS10461 |
| [20] |
Zhou WT, Zhang H, An X, et al. A nomogram for predicting post-operative hydrocephalus in children with medulloblastoma[J]. Neurosurg Rev, 2023, 46(1): 246. DOI:10.1007/s10143-023-02156-4 |
| [21] |
Stacey D, Lewis KB, Smith M, et al. Decision aids for people facing health treatment or screening decisions[J]. Cochrane Database Syst Rev, 2024, 1(1): CD001431. DOI:10.1002/14651858.CD001431.pub6 |
 2026, Vol. 25
2026, Vol. 25


