2. 南方医科大学珠江医院小儿外科, 广州 510285
2. Department of Pediatric Surgery, Zhujiang Hospital of Southern Medical University, Guangzhou 510285, China
胆道闭锁(biliary atresia, BA)是婴儿期严重的胆汁淤积性疾病,若未及时干预,可快速进展为胆汁性肝硬化及肝衰竭,威胁患儿生命[1-2]。Kasai手术是目前BA的首选治疗方式,但即便手术成功,仍有60% ~70%的患儿最终需接受肝移植[3]。早诊断、早治疗是改善BA患儿自体肝生存率的关键[4]。γ-谷氨酰转肽酶(γ-glutamyl transferase, γ-GGT)是谷胱甘肽代谢的关键酶,主要表达于肝细胞及胆管细胞膜,其血清水平升高常提示胆道梗阻或肝细胞损伤,在BA的早期识别中具有重要价值,可用于鉴别BA与其他肝脏疾病[5]。临床中BA患儿γ-GGT水平多会出现显著升高,300 IU/L被公认为最佳诊断临界值,具有较高的灵敏度和特异度[6-7]。然而,部分确诊为BA的患儿术前γ-GGT水平低于300 IU/L,相关研究表明,此类患儿Kasai手术预后不良,但具体影响因素尚未完全明确[6, 8-9]。本研究通过对比低水平与高水平γ-GGT BA患儿的术后预后差异,探讨低水平γ-GGT BA患儿预后的关键影响因素,为该特殊高危亚群的识别及预后评估提供理论依据。
资料与方法 一、研究对象本研究为回顾性队列研究,选取2016年6月至2023年10月在广州医科大学附属妇女儿童医疗中心确诊为Ⅲ型BA并接受Kasai手术的患儿,筛选术前γ-GGT<300 IU/L的51例患儿作为低水平γ-GGT组(LG组);同期选取术前γ-GGT≥300 IU/L的BA患儿124例作为高水平γ-GGT组(HG组)进行对照分析。纳入标准:①经手术探查及临床病理活检确诊为Ⅲ型BA;②病历资料完整,包含术前检查、手术记录及术后随访信息。排除标准:①Ⅰ、Ⅱ型BA;②失访或随访资料不全。
二、研究方法 (一) 临床数据收集收集患儿性别、手术日龄、体重、身体质量指数(body mass index, BMI),术前丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase, AST)、总胆红素(total bilirubin, TBIL)、直接胆红素(direct bilirubin, DBIL)、总胆汁酸(total bile acid, TBA)、白蛋白(albumin, ALB)等指标,记录术后胆管炎发生情况及早期胆汁引流(early bile drainage, EBD)效果。通过门诊复诊、电话随访,随访终点为患儿接受肝移植或死亡,计算Kasai术后自体肝生存时间(以月为单位),随访截至2024年10月。
(二) 分组依据按术前γ-GGT水平分组:LG组(γ-GGT<300 IU/L)、HG组(γ-GGT≥300 IU/L)。LG组按术后结局分组:自体肝生存组(Low γ-glutamyl transferase with native liver survival group,LG-G组)定义为随访期内维持自体肝功能,未行肝移植且未死亡;肝移植/死亡组(Low γ-glutamyl transferase with liver transplantation/mortality group,LG-P组)定义为随访期内接受肝移植或因BA相关并发症及肝移植相关原因死亡。按手术日龄60天分层分组:≤60天LG组(Younger-age low γ-glutamyl transferase group,Y-LG组)、≤60天HG组(Younger-age high γ-glutamyl transferase group, Y-HG组)、>60天LG组(Older-age low γ-glutamyl transferase group, O-LG组)、>60天HG组(Older-age high γ-glutamyl transferase group, O-HG组)。O-LG组按术后结局分组:自体肝生存组(Older-age Low γ-glutamyl transferase with native liver survival, O-LG-G组)、肝移植/死亡组(Older-age Low γ-glutamyl transferase with liver transplantation/mortality, O-LG-P组)。
(三) 诊断标准早期胆汁引流:Kasai术后1个月内大便颜色变黄,皮肤巩膜黄染明显消退,血清胆红素水平较术前下降1/3,定义为早期胆汁引流良好(early bile drainage-good, EBD-G);反之则为引流不良(early bile drainage-poor, EBD-P)[10]。
胆管炎:①全身炎症反应(发热或中性粒细胞、C反应蛋白等炎症标志物升高);②胆汁淤积表现(黄疸复发或加重、陶土样便、TBIL≥34 μmol/L且DBIL升高为主、转氨酶>1.5倍正常值、影像学提示胆汁湖形成)。疑似诊断需符合①和②中任意2项,确诊需符合①中1项及②中2项,或疑似病例合并血培养阳性[11]。
三、统计学处理采用SPSS 25.0及GraphPad Prism 9.5.1进行数据整理与分析。计数资料以频数、构成比表示,组间比较采用χ2检验或Fisher精确概率法;服从正态分布的计量资料以x±s表示,组间比较采用两独立样本t检验;不服从正态分布的计量资料以M(Q1, Q3)表示,组间比较采用Mann-Whitney U检验;以Kaplan-Meier法绘制生存曲线。P<0.05为差异有统计学意义。
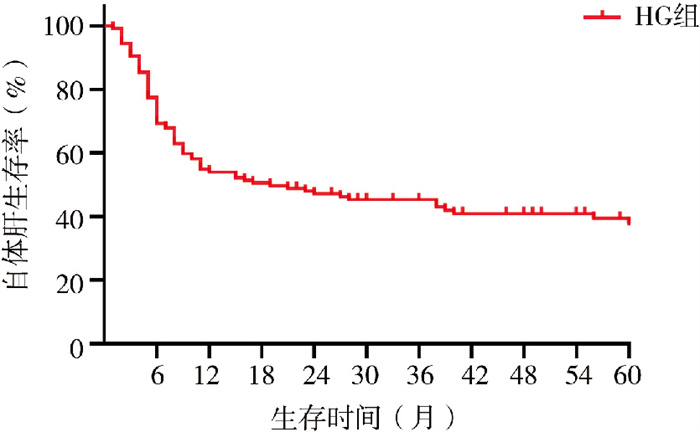
结果LG组共51例(男24例,女27例),术后6个月、1年、3年及5年SNL分别为62.7%、41.2%、28.2%、28.2%(图 1);HG组共124例(男65例,女59例),术后6个月、1年、3年及5年SNL分别为69.4%、54.0%、45.2%、37.8%(图 2)。两组总体生存曲线比较,差异无统计学意义(Log-rank χ2=1.86,P>0.05)。

|
图 1 LG组胆道闭锁患儿自体肝生存曲线 Fig.1 Native Liver Survival Curve in BA infants with LG group 注 LG组: 低水平γ-GGT(<300 IU/L)组 |
|
图 2 HG组胆道闭锁患儿自体肝生存曲线 Fig.2 Native liver survival curve in BA infants with HG group 注 HG组: 高水平γ-GGT(≥300 IU/L)组 |
LG-G组(15例)手术日龄显著低于LG-P组(36例)[(55.80±12.35)d比(71.28±15.36)d],差异有统计学意义(P<0.05);LG-G组早期胆汁引流良好率显著高于LG-P组(9/15比2/36),差异有统计学意义(P<0.001);两组在性别、体重、BMI、术前肝功能指标(ALT、AST、TBIL等)及胆管炎发生情况方面,差异均无统计学意义(P>0.05)。见表 1。
| 表 1 LG-G组与LG-P组胆道闭锁患儿基本资料及围术期指标比较 Table 1 Comparison of basic profiles and perioperative parameters between LG-G and LG-P groups |
|
|
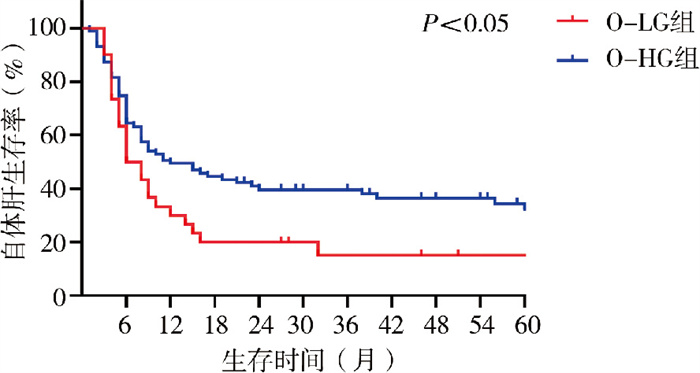
不同手术日龄亚组预后比较:①手术日龄≤60天亚组:Y-LG组(21例),Y-HG组(37例),两组自体肝生存率比较,差异无统计学意义(P>0.05);②手术日龄>60天亚组:O-LG组30例,O-HG组87例,O-LG组5年SNL(15%)显著低于O-HG组(32.3%),差异有统计学意义(Log-rank χ2=4.12,P<0.05)。见图 3。
|
图 3 O-LG组与O-HG组胆道闭锁患儿自体肝生存率比较 Fig.3 Comparison of Native Liver Survival Rates in Infants with Biliary Atresia between O-LG and O-HG groups 注 O-LG组: 手术日龄>60天的低水平γ-GGT组;O-HG组: 手术日龄>60的高水平γ-GGT组 |
O-LG-G组(5例)早期胆汁引流良好率显著高于O-LG-P组(25例)(4/5比1/25),差异有统计学意义(P<0.001);两组在性别、手术日龄、体重、BMI、术前肝功能指标及胆管炎发生情况方面,差异均无统计学意义(P>0.05)。见表 2。
| 表 2 O-LG-G组与O-LG-P组胆道闭锁患儿两组基本资料及围术期指标比较 Table 2 Comparison of basic profiles and perioperative parameters between O-LG-G and O-LG-P groups |
|
|
γ-GGT显著升高是BA筛查与诊断的重要生化指标[12],但临床中部分BA患儿术前γ-GGT水平低于300 IU/L,此类患儿预后相对较差[8]。本研究结果显示,低水平γ-GGT BA患儿Kasai术后5年SNL仅28.2%,低于高水平γ-GGT组的37.8%,虽总体差异无统计学意义(可能与样本量较小有关),但亚组分析提示手术日龄>60天的低水平γ-GGT患儿预后显著更差,且早期胆汁引流效果是影响其预后的关键因素。
γ-GGT参与谷胱甘肽代谢,对维持细胞氧化还原平衡、抵御氧化应激损伤具有重要作用[5]。在梗阻性胆汁淤积(如BA)中,胆道压力增高破坏胆- 血屏障,促使γ-GGT从胆管细胞膜脱落并反流入血,致其血清水平显著升高,这实质上是胆道梗阻及其引发的胆管细胞损伤的生化标志[13-14]。然而,若患儿胆管细胞γ-GGT表达低下,或存在胆汁酸组成异常、胆汁酸转运相关基因(如ABCB11或ATP8B1)杂合变异,则即使存在胆道梗阻,血清γ-GGT也可能不会显著升高,常提示更复杂的肝内代谢缺陷,并可能伴随更严重的肝细胞损伤[6, 8]。低水平γ-GGT可能意味着肝细胞及胆管细胞抗氧化应激能力不足,谷胱甘肽循环效能低,难以抵御胆汁淤积引发的氧化攻击,导致肝纤维化进程加速[15]。Luo等[15]研究也发现,长期自体肝生存的BA患儿其调控谷胱甘肽代谢的基因表达上调,提示抗氧化能力在疾病进展中的保护作用。此外,低γ-GGT水平可能使患儿被误判为非梗阻性肝病,延误最佳手术时机[6]。本研究结果显示,手术日龄是决定低水平γ-GGT BA患儿预后的关键因素之一。LG-G组手术日龄显著低于LG-P组,且手术日龄>60天的O-LG组5年SNL(15%)显著低于O-HG组(32.3%),提示手术时机对低水平γ-GGT BA患儿预后至关重要。韩一江等[16]也强调了早期手术对改善BA预后的意义。对于可能存在抗氧化能力不足和胆汁酸代谢紊乱的低γ-GGT BA患儿,早期手术可及时解除胆道梗阻,减少胆汁淤积对肝脏的持续损伤,而手术延迟会使氧化应激损伤不断累积,突破肝细胞防御阈值,导致不可逆肝损害。结合临床实践,这类患儿更应被视为需要尽早诊断、尽早手术干预的高危群体。
早期胆汁引流效果是评估BA患儿术后黄疸清除及肝功能恢复的重要指标[17-18]。本研究显示,在低水平γ-GGT患儿中,自体肝生存组(LG-G组及O-LG-G组)早期胆汁引流良好率分别显著高于肝移植/死亡组(LG-P组及O-LG-P组),成功的早期胆汁引流不仅意味着机械性梗阻的解除,更深层次的作用在于快速降低肝内胆汁酸浓度,减轻其对肝细胞及胆管细胞的直接毒性;改善肝内微循环与氧化还原状态,缓解因胆汁淤积引发的持续氧化应激;并可能延缓甚至部分逆转早期肝纤维化进程。葛亮等[17]的研究亦表明,术后黄疸的快速清除有助于减缓肝纤维化,从而延长自体肝生存时间。对于抗氧化应激能力不足的低水平γ-GGT患儿,建立有效的胆汁引流通路更是关键的保护措施。
本研究存在一定局限性:样本量较小且为单中心回顾性分析,可能存在选择偏倚;未纳入术后γ-GGT动态变化、胆汁酸分析等更深入的指标。未来需通过多中心大样本研究进一步验证结论,并探索靶向抗氧化治疗等改善低水平γ-GGT BA患儿预后的新策略。
综上所述,低水平γ-GGT BA患儿手术日龄超过60天者预后差于高水平γ-GGT患儿,早期胆汁引流成功是改善其预后的重要因素。临床中对胆汁淤积患儿,无论γ-GGT水平如何,均应尽早开展BA鉴别诊断,把握60天内的最佳手术时机,以提高患儿自体肝生存率。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 文献检索为郭烁烁、刘斐;论文设计为郭烁烁、刘斐;数据收据收集与分析为郭烁烁、陶波圆、叶志华、兰梦龙、张红、李斯锦;论文结果撰写为郭烁烁、刘斐、曾纪晓、徐晓钢;论文讨论分析为郭烁烁、曾纪晓、徐晓钢、刘斐
| [1] |
Zhu JJ, Yang YF, Dong R, et al. Biliatresone: progress in biliary atresia study[J]. World J Pediatr, 2023, 19(5): 417-424. DOI:10.1007/s12519-022-00619-0 |
| [2] |
Davenport M, Kronfli R, Makin E. Advances in understanding of biliary atresia pathogenesis and progression-a riddle wrapped in a mystery inside an enigma[J]. Expert Rev Gastroenterol Hepatol, 2023, 17(4): 343-352. DOI:10.1080/17474124.2023.2191188 |
| [3] |
Zheng LL, Wu YB, Gong ZH, et al. The composition of the gut microbiota is altered in biliary atresia with cholangitis[J]. Front Surg, 2022, 9: 990101. DOI:10.3389/fsurg.2022.990101 |
| [4] |
Tam PKH, Wells RG, Tang CSM, et al. Biliary atresia[J]. Nat Rev Dis Primers, 2024, 10(1): 47. DOI:10.1038/s41572-024-00533-x |
| [5] |
黄子寒, 郑珊. γ-谷氨酰转肽酶在胆道闭锁诊断和预后评价中的研究进展[J]. 临床小儿外科杂志, 2021, 20(2): 140-144, 160. Huang ZH, Zheng S. Research advances of gamma-glutamyltransferase in the diagnosis and prognosis of biliary atresia[J]. J Clin Ped Sur, 2021, 20(2): 140-144, 160. DOI:10.12260/lcxewkzz.2021.02.007 |
| [6] |
Sun S, Zheng S, Shen C, et al. Low gamma-glutamyl transpeptidase levels at presentation are associated with severity of liver illness and poor outcome in biliary atresia[J]. Front Pediatr, 2022, 10: 956732. DOI:10.3389/fped.2022.956732 |
| [7] |
李明明, 潘永康, 卢朝祥, 等. γ-谷氨酰转肽酶 <300 U/L的胆汁淤积患儿胆道闭锁风险的列线图预测模型[J]. 中华小儿外科杂志, 2023, 44(2): 125-131. Li MM, Pan YK, Lu CX, et al. A histogram model for predicting the risks of biliary atresia in cholestatic infants with GGT <300 U/L[J]. Chin J Pediatr Surg, 2023, 44(2): 125-131. DOI:10.3760/cma.j.cn421158-20210909-00440 |
| [8] |
Shankar S, Bolia RS, Foo HW, et al. Normal gamma glutamyl transferase levels at presentation predict poor outcome in biliary atresia[J]. J Pediatr Gastroenterol Nutr, 2020, 70(3): 350-355. DOI:10.1097/MPG.0000000000002563 |
| [9] |
张书豪, 陈功, 郑珊, 等. 低谷氨酰转肽酶水平胆道闭锁患儿的临床特点[J]. 中华小儿外科杂志, 2019, 40(1): 23-27. Zhang SH, Chen G, Zheng S, et al. Clinical features of low level serum gamma-glutamyl transferase in infants with biliary atresia[J]. Chin J Pediatr Surg, 2019, 40(1): 23-27. DOI:10.3760/cma.j.issn.0253-3006.2019.01.005 |
| [10] |
李斯锦, 曾纪晓, 徐晓钢, 等. 胆道闭锁Kasai手术后未发生胆管炎患儿的近中期疗效及影响因素分析[J]. 临床小儿外科杂志, 2025, 20(1): 30-34. Li SJ, Zeng JX, Xu XG, et al. Analysis of short/medium-term effectiveness and influencing factors after Kasai surgery in patients with biliary atresia without cholangitis[J]. J Clin Ped Sur, 2025, 20(1): 30-34. DOI:10.3760/cma.j.cn101785-202405016-006 |
| [11] |
中华医学会小儿外科学分会肝胆外科学组. 胆道闭锁Kasai术后胆管炎诊疗专家共识(2022版)[J]. 中华小儿外科杂志, 2022, 43(9): 769-774. Section of Hepatobiliary Surgery, Branch of Pediatric Surgery, Chinese Medical Association. Expert consensus on diagnosing and treating cholangitis after Kasai operation for biliary atresia (2022 edition)[J]. Chin J Pediatr Surg, 2022, 43(9): 769-774. DOI:10.3760/cma.j.cn421158-20220427-00308 |
| [12] |
Kong FY, Dong R, Chen G, et al. Progress in biomarkers related to biliary atresia[J]. J Clin Transl Hepatol, 2024, 12(3): 305-315. DOI:10.14218/JCTH.2023.00260 |
| [13] |
Ye CX, Gao W. Predictors of outcome among children with biliary atresia: a single centre trial[J]. PeerJ, 2025, 13: e19001. DOI:10.7717/peerj.19001 |
| [14] |
Kohlmaier B, Tichy H, Blatterer J, et al. Extrahepatic biliary atresia and normal-range serum gamma-glutamyltranspeptidase activity: a case report[J]. JPGN Rep, 2024, 5(4): 533-537. DOI:10.1002/jpr3.12131 |
| [15] |
Luo ZH, Shivakumar P, Mourya R, et al. Gene expression signatures associated with survival times of pediatric patients with biliary atresia identify potential therapeutic agents[J]. Gastroenterology, 2019, 157(4): 1138-1152. DOI:10.1053/j.gastro.2019.06.017 |
| [16] |
韩一江, 吴昊, 季浩森, 等. 胆道闭锁Kasai手术日龄与早期预后的关联性分析[J]. 临床小儿外科杂志, 2023, 22(3): 225-231. Han YJ, Wu H, Ji HS, et al. Correlation between age of Kasai portoenterostomy and early prognosis for biliary atresia[J]. J Clin Ped Sur, 2023, 22(3): 225-231. DOI:10.3760/cma.j.cn101785-202210044-005 |
| [17] |
葛亮, 詹江华. 胆道闭锁肝纤维化与自体肝生存关系的研究进展[J]. 临床小儿外科杂志, 2020, 19(2): 171-175. Ge L, Zhan JH. Relationship between liver fibrosis and native liver survival in infants with biliary atresia[J]. J Clin Ped Sur, 2020, 19(2): 171-175. DOI:10.3969/j.issn.1671-6353.2020.02.016 |
| [18] |
Liu F, Xu XG, Liang ZJ, et al. Early bile drainage improves native liver survival in biliary atresia without cholangitis[J]. Front Pediatr, 2023, 11: 1189792. DOI:10.3389/fped.2023.1189792 |
 2026, Vol. 25
2026, Vol. 25


