左侧门静脉高压(left-sided portal hypertension, LSPH),又名区域性门静脉高压(sinistral portal hypertension, SPH),最常见病因是脾静脉梗阻引发脾静脉血流不畅,最终导致食管胃底静脉曲张、出血,是一种少见的上消化道出血疾病。当前文献报道大多为成人患者,儿童病例报道较少。本文报道3例LSPH患儿诊治经过,并结合文献复习探讨其诊治经验。
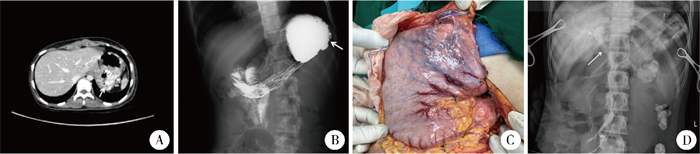
患儿1,女,14岁,因“反复不明原因贫血2年”就诊,门诊以门静脉高压收入院。患儿曾因食管胃底静脉出血予止血治疗。体格检查:脾肋下3 cm,未扪及包块。辅助检查:肝功能正常;血常规:白细胞1.55×109/L,血红蛋白40 g/L,血小板145×109/L;超声检查:脾脏弥漫性增大,脾门静脉呈细的迂曲状,肝内及肝门部门静脉形态良好,胃短静脉扩张,胃底静脉曲张;CT检查:胃底脾门周围见多发迂曲血管影,脾脏体积增大(图 1A);上消化道造影:胃底出现充盈缺损(图 1B)。初步诊断为LSPH,并行手术探查。术中见脾门处脾静脉明显狭窄,胃底静脉曲张明显(图 1C),测得脾胃区门静脉压力为15 cm H2O(1 cm H2O=0.098 kPa),造影显示肝内门静脉显影良好(图 1D),胃底静脉曲张明显。确诊为LSPH,行脾切除术和胃底静脉结扎术。术后CT提示胃底静脉曲张消失,血红蛋白逐渐上升(64 g/L),白细胞恢复正常(4.61×109/L)。术后1个月复查患儿恢复良好。
|
图 1 1例14岁女性左侧门静脉高压患儿检查组图 Fig.1 A panel of diagnostic images for left-sided portal hypertension in Case No.1 注 A:术前腹部增强CT显示胃底周围明显迂曲强化血管影;B:上消化道造影出现胃底充盈缺损;C:术中见胃底静脉明显曲张;D:门静脉造影结果正常 |
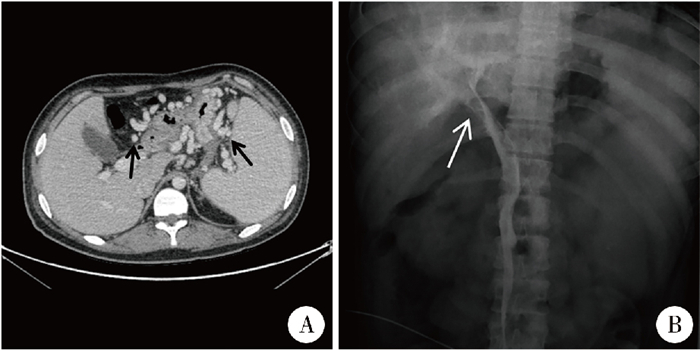
患儿2,男,16岁,因“腹痛、呕吐”就诊,查血清淀粉酶、脂肪酶及尿淀粉酶升高,2年前曾有急性胰腺炎病史,2年内多次复发胰腺炎。腹部检查触及脾肿大,入院后完善血液学检查,白细胞4×109/L,血红蛋白76 g/L,血小板84×109/L。急诊超声见胰腺回声粗糙,胰周出现不规则低回声片影,脾脏弥漫性肿大,有脾静脉血栓征象,脾周、胃周见多发迂曲走行的侧支血管,门静脉形态正常。CT显示胰腺周围脂肪间隙模糊,脾大,脾门及胃体周围有迂曲血管影(图 2A)。考虑区域性门静脉高压行手术探查,术中测得门静脉压力(12 cm H2O)正常,门静脉造影显示正常(图 2B),探查见脾脏增大,胃底静脉明显曲张,胰腺缩小硬化,确诊为LSPH。因反复胰腺炎导致脾门粘连严重,最终选择脾完全切除,并结扎曲张的胃底静脉。术后CT见迂曲血管较前明显改善,白细胞、血小板及血红蛋白逐渐恢复正常。
|
图 2 1例16岁男性左侧门静脉高压患儿检查组图 Fig.2 A panel of diagnostic images for left-sided portal hypertension in Case No.2 注 A:增强CT见脾门及胃体周围多个迂曲血管影;B:门静脉造影显示正常 |
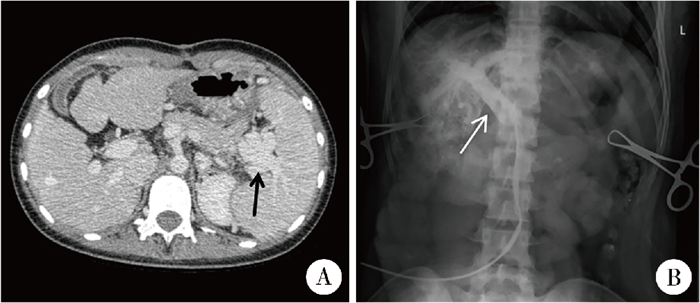
患儿3,女,14岁,2年前确诊肝纤维化型门静脉高压,行脾静脉-肾静脉分流术及胃底静脉结扎术,术后间断出现消化道出血,行保守治疗,此次因“不明原因黑便、呕血”入院。体格检查:皮肤及黏膜稍苍白。辅助检查:超声下脾肾分流血管腔结构不清晰,左肾静脉增粗,胃周及脾门静脉迂曲扩张;CT提示肝内多发血管畸形,食管、胃底静脉曲张,脾门多发血管曲张,脾静脉明显增粗(图 3A);血常规:血红蛋白88 g/L,红细胞2.34×109/L,谷草转氨酶(asparate aminotransferase, AST)39.3 U/L,谷丙转氨酶(alanine aminotransferase, ALT)41.2 U/L。行手术探查,经肠系膜上静脉分支血管置入中心静脉导管,测量门静脉主干压力正常(16 cm H2O),门静脉造影显示肝内外门静脉正常(图 3B),探查见脾脏增大,胃底静脉曲张明显,原脾肾分流血管闭锁。鉴于患儿门静脉压力正常,脾大伴胃底静脉曲张明显,考虑诊断为LSPH,选择脾切除术和胃底静脉结扎术。术后影像学检查见曲张静脉血管消失,红细胞、血小板逐渐正常,患儿恢复良好出院。
|
图 3 1例14岁女性左侧门静脉高压患儿检查组图 Fig.3 A panel of diagnostic images for left-sided portal hypertension in Case No.3 注 A:增强CT见脾门多发血管曲张,脾静脉增粗;B:门静脉造影显示门静脉正常 |
LSPH的概念由Greenwald等[1]于1939年首次提出,是肝外门静脉高压的一种,在肝外型门静脉高压中占比不超过5%,在全部门静脉高压中占比为0.25%~0.5%。尽管该病在临床表现上与传统的门静脉高压有相似之处,但二者致病原因不同。传统门静脉高压系各种原因(包括门静脉海绵样变、肝硬化和布加综合征等)引发的门静脉压力升高,进而导致脾大和食管胃底静脉曲张破裂出血。
LSPH的主要致病原因是脾静脉血栓形成或闭塞,导致脾脏及胃底静脉血流不畅,进而出现脾大。最常见原因是胰腺原发疾病对脾静脉的影响,包括急慢性胰腺炎、胰腺假性囊肿和胰腺肿瘤。Madsen等[2]报道了209例LSPH,其中胰腺炎占65%,17% 为其他疾病所致。唐亮等[3]检索分析了1980年1月至2019年6月相关文献,共报道3 576例患者,主要病因分别是胰腺肿瘤(34.40%)、慢性胰腺炎(29.67%)、急性胰腺炎(7.27%),以胰腺炎为病因者占36.94%。其他原因包括医源性脾静脉结扎、先天性解剖畸形、副脾、脾肾静脉远端分流术后吻合口血栓形成、外伤等,为罕见病因,较少报道。本组病例1经术中探查发现病因为先天性脾静脉狭窄,导致脾静脉易梗阻;病例2曾有胰腺炎病史,此次就诊以胰腺炎为首要表现,胰腺组织肿大压迫以及炎症因子使脾周出现血液高凝状态、炎症直接侵蚀脾静脉使血管内膜受损等,都是胰腺炎导致脾静脉血栓形成的可能原因;病例3有脾肾远端分流手术史,术中探查发现因脾肾分流血管闭锁,使原本流入脾静脉的血液逆流入胃周、胃底静脉,引起静脉曲张,极易破裂出血。
目前,国内外尚未建立统一的LSPH诊断标准,诊断主要基于临床表现及CT、胃镜等辅助检查,主要特征包括: ①影像学检查发现侧支血管或内镜下检查存在胃底静脉曲张;②排除门静脉高压的其他原因,包括特发性门静脉高压或肝硬化;③伴或不伴脾大或脾功能亢进[4-5]。临床表现主要为脾肿大(68.47%)、上消化道出血(54.92%)、上腹部不适或腹痛(38.56%)、孤立性静脉曲张(71.44%)等,多数患者以上消化道出血为首诊表现[3]。实验室检查可见脾功能亢进征象,包括白细胞、血小板减少,但肝功能正常(ALT、AST正常)。影像学检查是确诊LSPH的主要手段,包括超声、CT、经皮穿刺脾静脉造影等,其中穿刺造影为金标准,但因其为有创检查,临床上并不作为首选。超声和CT是目前首选检查方法,本组3例术前实验室检查均发现脾功能亢进且肝功能正常,超声和CT检查发现脾脏增大和胃底静脉曲张,考虑为门静脉高压,术中观察肝脏形态正常,进一步完善门静脉造影和测压,确定门静脉压力正常,排除引起系统性门静脉高压的病因,最终诊断为LSPH。
上消化道出血是LSPH的严重并发症,出血量大时有引发休克的风险,可危及患者生命,因此及时处理LSPH非常重要。内镜治疗的优势在于治疗和检查可以同时进行,包括内镜下血管套扎术(endoscopic variceal ligation, EVL)和内镜下硬化剂注射(endoscopic injection sclerotherapy, EIS),EVL和EIS可以起到暂时止血的作用,但止血治疗仅能暂时保持病情稳定,并不能解决区域内高压,因而病情复发不可避免,因此内镜治疗主要用于LSPH出现急性上消化道出血的抢救治疗[6]。当患儿生命体征平稳后,还需针对区域性门静脉高压的根本原因进行治疗。脾切除术可以解除LSPH的致病原因,降低侧支曲张静脉的压力,解除脾静脉回流障碍,是当前治疗LSPH最常用和最有效治疗方法。Liu等[7]在一项荟萃研究中得出结论,脾切除术在降低上消化道出血发生率和病死率方面较其他治疗方式更有效。介入下血管内微创治疗也被认为是可行的治疗手段,包括脾动脉栓塞术(splenic artery embolism, SAE)和脾静脉支架植入术(splenic vein stenting, SVS)[8-9]。SAE的原理与脾切除术相同,可以通过减少从脾到侧支静脉的血流来防止出血,从而减轻相关静脉曲张的压力。与脾切除术相比,SAE最重要的优点是其微创性且保留了脾功能[4]。但SAE存在不能有效把握脾脏栓塞面积、栓剂外流引发异位栓塞和术后复发率高的风险。Liu等[10]和Wang等[11]提出使用两步完全SAE治疗LSPH,可减少单纯SAE治疗的并发症,但长期疗效仍需更多证据支持。另有研究人员认为,在脾切除术前行脾动脉栓塞可有效减少手术时间和术中失血量,且不会增加各种并发症的发生率[9, 12]。因此,SAE适合作为高风险患儿脾切除术前的辅助治疗手段。SVS因具备微创及术后并发症少等优势,在血管外科领域受到关注。然而,将其应用于处持续生长发育的儿童患者时,其固定管径的机械特性可能因无法匹配血管的自然生长而演变为医源性狭窄。此外,所有植入性血管支架均普遍面临血管内膜增生致远期再狭窄的风险。目前,针对儿童群体的SVS临床应用报道极为有限,其长期安全性及疗效证据尚属空白。因此,该术式用于儿童血管疾病治疗几乎不予常规考虑[8]。本研究中,3例患儿均采用脾切除术和胃底静脉结扎术治疗,术后随访1年恢复良好,患儿症状明显改善,后续将每年复查,长期随访。
总之,LSPH是一种少见的儿童门静脉高压,临床症状不典型,常难以诊断,需结合辅助检查、术中门静脉造影及测压来明确诊断,目前脾切除术是治疗该疾病的主要手段。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 辛丽媛负责文献检索、论文设计、数据收集、研究结果分析及论文撰写;张金山负责全文知识性内容的审读与修正
| [1] |
Greenwald HM, Wasch MG. The roentgenologic demonstration of esophageal varices as a diagnostic aid in chronic thrombosis of the splenic vein[J]. J Pediatr, 1939, 14(1): 57-65. DOI:10.1016/s0022-3476(39)80117-2 |
| [2] |
Madsen MS, Petersen TH, Sommer H. Segmental portal hypertension[J]. Ann Surg, 1986, 204(1): 72-77. DOI:10.1097/00000658-198607000-00010 |
| [3] |
唐亮, 邱秋, 徐福民, 等. 3576例区域性门脉高压症患者临床特征的系统分析[J]. 第三军医大学学报, 2019, 41(22): 2217-2222. Tang L, Qiu Q, Xu FM, et al. Clinical characteristics of regional portal hypertension: a systematic analysis of 3576 patients[J]. J Army Med Univ, 2019, 41(22): 2217-2222. DOI:10.16016/j.1000-5404.201908033 |
| [4] |
Miao Q, Zheng ZQ, Piao MY, et al. Case report: upper gastrointestinal bleeding associated with pancreatic segmental portal hypertension: six case reports and literature review[J]. Front Med (Lausanne), 2025, 12: 1522413. DOI:10.3389/fmed.2025.1522413 |
| [5] |
Ru N, He CH, Ren XL, et al. Risk factors for sinistral portal hypertension and related variceal bleeding in patients with chronic pancreatitis[J]. J Dig Dis, 2020, 21(8): 468-474. DOI:10.1111/1751-2980.12916 |
| [6] |
Pancreas Study Group, Chinese Society of Gastroenterology, Chinese Medical Association. Practice guidance for diagnosis and treatment of pancreatitis-related splanchnic vein thrombosis (Shenyang, 2020)[J]. J Dig Dis, 2021, 22(1): 2-8. DOI:10.1111/1751-2980.12962 |
| [7] |
Liu MH, Wei N, Song YH. Splenectomy versus non-splenectomy for gastrointestinal bleeding from left-sided portal hypertension: a systematic review and meta-analysis[J]. Therap Adv Gastroenterol, 2024, 17: 17562848241234501. DOI:10.1177/17562848241234501 |
| [8] |
Cakmak O, Parildar M, Oran I, et al. Sinistral portal hypertension; imaging findings and endovascular therapy[J]. Abdom Imaging, 2005, 30(2): 08-213. DOI:10.1007/s00261-004-0231-2 |
| [9] |
Wang ZH, Li M, Huang X, et al. Preoperative splenic artery embolism followed by splenectomy is safe and effective in patients with sinistral portal hypertension[J]. Langenbecks Arch Surg, 2022, 407(1): 313-319. DOI:10.1007/s00423-021-02329-z |
| [10] |
Liu JC, Meng J, Yang M, et al. Two-step complete splenic artery embolization for the management of symptomatic sinistral portal hypertension[J]. Scand J Gastroenterol, 2022, 57(1): 78-84. DOI:10.1080/00365521.2021.1983641 |
| [11] |
Wang Q, Xiong B, Zheng CS, et al. Splenic arterial embolization in the treatment of severe portal hypertension due to pancreatic diseases: the primary experience in 14 patients[J]. Cardiovasc Intervent Radiol, 2016, 39(3): 353-358. DOI:10.1007/s00270-015-1199-8 |
| [12] |
Covello B, Miller J, Fourzali R. Splenic vein stenting for recurrent chylous ascites in sinistral portal hypertension: a case report[J]. CVIR Endovasc, 2021, 4(1): 26. DOI:10.1186/s42155-021-00213-x |
 2026, Vol. 25
2026, Vol. 25


