生殖细胞肿瘤占儿童恶性肿瘤的3%,且多位于性腺组织[1]。腹膜后等性腺外的卵黄囊瘤较为少见,仅占2% ~5%,伴发肝转移则更为罕见[2]。本文报道福建省儿童医院收治的1例腹膜后卵黄囊瘤伴肝转移患儿,探讨腹膜后卵黄囊瘤伴肝转移的临床特点。
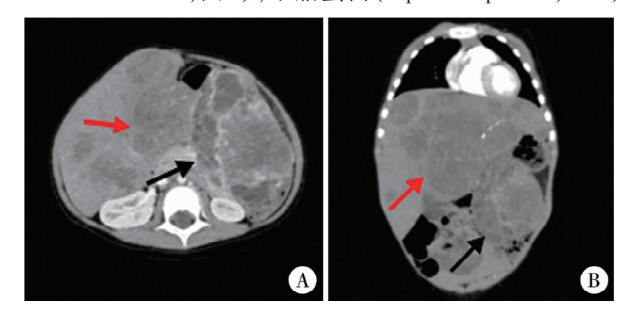
患儿,男,2岁10个月,因“发现腹部隆起4个月”于2022年2月10日就诊于福建省儿童医院普外科。本院查腹部增强CT示肝脏增大,见弥漫多发类圆形稍低密度灶,较大者位于左肝Ⅳ段,大部分突出肝轮廓之外,其内密度欠均匀,可见更低密度灶和小结节状高密度钙化影(约8.5 cm× 9.9 cm×12.1 cm,图 1),甲胎蛋白(alpha-fetoprotein, AFP)26 586.00 ng/mL。骨扫描、骨髓穿刺活检、胸部CT、颅脑MR均未见明显异常。
|
图 1 腹膜后卵黄囊瘤伴肝转移患儿治疗前腹部增强CT照片病灶 Fig.1 Abdominal contrast-enhanced CT images of a child of retroperitoneal yolk sac tumor with liver metastasis pre-treatment 注 A:肝内病灶(红色箭头)、肝轮廓外病灶(黑色箭头);B:冠状位 |
患儿初步诊断为“肝脏多发占位”,于2022年2月14日行“开腹肝脏肿物活检术+腹膜后肿物活检术”。肝脏见多发、大小不一肿物,肝脏包膜与腹膜部分粘连。左侧后腹膜明显隆起一肿物(约10.0 cm ×8.0 cm×8.0 cm),与肝脏分离,肿物向上压迫胰腺体尾部,左侧紧邻降结肠,右侧压迫门静脉及肠系膜上静脉,粘连紧密。切开肝脏肿物及腹膜后肿物包膜,见肿物呈鱼肉样外观,予行活检(图 2)。
|
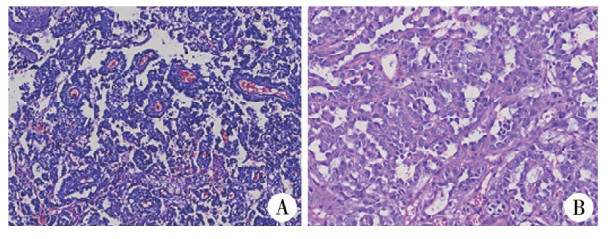
图 2 腹膜后卵黄囊瘤伴肝转移患儿病理检查结果图 Fig.2 Pathological examination results of a child of retroperitoneal yolk sac tumor with liver metastasis 注 A:腹膜后肿物可见散在S-D小体;B:肝肿物可见疏松网状结构,胞质AFP(+) |
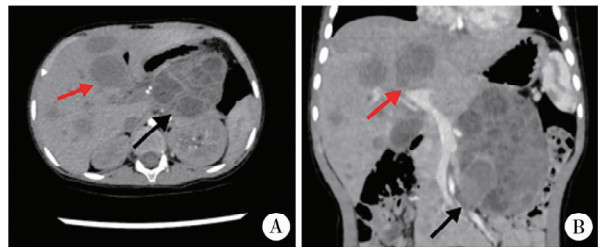
术后病理回报结合形态学及酶标符合生殖细胞肿瘤、卵黄囊瘤,最后病理为卵黄囊瘤,患儿术后分期按美国儿童肿瘤协作组(Children's Oncology Group, COG)归于腹膜后卵黄囊瘤Ⅳ期。于2022年2月21日起行4个周期化疗。予AVCP方案(多柔比星+环磷酰胺+顺铂+长春新碱)行第1疗程期间,患儿出现肝转移瘤破裂出血,予保守治疗后情况稳定;后予2疗程IEV方案(异环磷酰胺+依托泊苷+长春新碱)、1疗程BVCP方案(博来霉素+环磷酰胺+顺铂+长春新碱)序贯化疗。2022年5月12日复查腹部增强CT示“原左中上腹囊实性肿块较前略缩小,肝内多发结节肿块影较前略缩小”(图 3)。复查AFP降至8.12 ng/mL。
|
图 3 腹膜后卵黄囊瘤伴肝转移患儿辅助化疗后腹部增强CT照片 Fig.3 Abdominal contrast-enhanced CT images of a child of retroperitoneal yolk sac tumor with liver metastasis after adjuvant chemotherapy 注 A:肝转移病灶(红色箭头)、腹膜后病灶(黑色箭头);B:冠状位 |
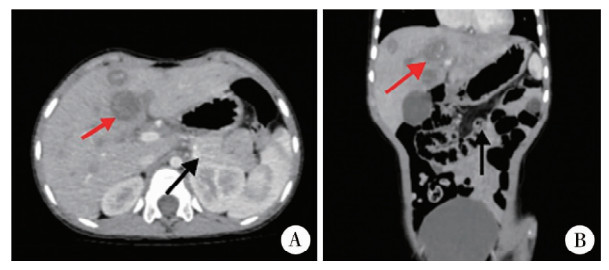
复查腹部增强CT见腹膜后病灶边界较前明显清晰,肝内转移灶缩小明显,肿瘤标志物AFP降至接近正常,故考虑存在手术切除指征,于2022年5月16日行“腹膜后卵黄囊瘤切除术、肝肿物活检术”。探查见后腹膜处可触及一肿物(约10 cm×8 cm×6 cm),质地中等,部分呈囊性。肿物后方与胰腺关系密切,内侧界与腹腔干、肠系膜上动脉粘连紧密,上界可见数根粗大的静脉引流至胃网膜左侧静脉。右肝Ⅵ段表面可及一肿物(约3 cm×3 cm),质地硬。行术中冰冻活检,回报肝肿物未见活性肿瘤成分,遂行腹膜后肿物切除术,术后病理同样证实肝肿物未见肿瘤组织。患儿出院后随访至术后4个月,复查腹部增强CT未见明显软组织影;肝内多发结节,考虑肿瘤转移,较前缩小、血供不明显(图 4),复查AFP 1.88 ng/mL。
|
图 4 腹膜后卵黄囊瘤伴肝转移患儿治疗后腹部增强CT照片病灶 Fig.4 Abdominal contrast-enhanced CT images of a child of retroperitoneal yolk sac tumor with liver metastasis post-treatment 注 A:肝转移病灶较前明显缩小(红色箭头)、原腹膜后病灶处未见复发(黑色病灶);B:冠状位 |
卵黄囊瘤(内胚窦瘤)是罕见的儿童生殖细胞肿瘤,好发于性腺、盆腔、骶尾部等部位,而原发于腹膜后的类型尤为罕见,仅占所有卵黄囊瘤的1.5%[3-4]。其发病机制与胚胎发育过程中原始生殖细胞迁移异常相关,迷失于腹膜后的原始生殖细胞异常转化形成肿瘤,且多沿人体中线分布[5]。腹膜后卵黄囊瘤因发病部位隐匿,早期诊断困难;首发症状多为腹部包块、腹围增大,常伴随腹痛、排便困难、恶心呕吐等消化道症状,确诊时肿瘤多已体积巨大,部分合并远处转移,其中肝转移属于高危情况。其临床表现缺乏特异性,辅助检查亦无特征性表现,增加诊断难度。
由于影像学表现和肿瘤标志物(如AFP升高)可能与多种疾病重叠,需与以下疾病重点鉴别:①肝母细胞瘤:原发于肝脏的恶性肿瘤,多为单发病灶,以腹胀、腹围增大为主要表现,部分肝外型病例影像学与腹膜后卵黄囊瘤相似[6],需通过病理检查确诊;②神经母细胞瘤:起源于交感神经系统,伴肝转移时可表现为直接浸润(边界不清)或血行转移(弥漫性增大或结节状病灶)[7-8],病理检查发现特征性神经母细胞瘤细胞可鉴别;③成熟性畸胎瘤:影像学以囊液性成分为主,常伴钙化,增强扫描多无强化,且AFP正常[9],可与本病区分;④结直肠癌肝转移:特征性影像学表现为“牛眼征”(门脉期肿瘤边缘强化、中心低密度)[10],结合病史可辅助鉴别。
腹膜后卵黄囊瘤的治疗以手术联合化疗为主,尤其对于伴肝转移的高危病例,该方案是改善预后的关键。文献回顾显示,大部分病例采用手术治疗,其中30例联合化疗;4例伴肝转移的病例中,2例接受手术联合化疗后预后理想,而仅行活检或活检联合化疗的2例患儿均死亡。生存率数据表明,无远处转移病例中,手术联合化疗组生存率显著高于其他治疗组;7例合并远处转移的病例中,5例死亡,仅2例手术联合化疗者存活。化疗药物的选择对疗效至关重要,铂类药物的应用显著提升了疗效[11]。宋君红等[12]研究显示,Ⅳ期高危组患儿采用VCP+IEV方案化疗,5年生存率88.73%。本例患儿术前接受4周期该方案化疗后,术中发现肝转移灶大片坏死,无存活肿瘤细胞;术后随访4个月,肝转移灶缩小,AFP降至正常。对于腹膜后卵黄囊瘤伴肝转移患儿,可先采用铂类药物辅助化疗,动态复查影像学及肿瘤指标;若肿瘤缩小、界限清晰,且未侵犯腹腔干、门静脉等重要血管及胰腺、肾脏等周围脏器,可行根治性手术切除原发病灶,肝转移灶条件许可时同步切除;若合并多发转移,术后继续辅助化疗,持续评估病灶变化。
综上,腹膜后卵黄囊瘤伴肝转移虽发生率低,但恶性程度高。通过“术前化疗+根治性手术+术后化疗”的综合治疗模式,尤其是铂类药物的合理应用,可显著改善患儿预后,总体疗效较以往明显提升。临床需重视早期鉴别诊断,及时采用规范的综合治疗方案,以提高患儿生存率。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 文献检索为黄雨珊,论文调查设计为林晟、白建喜,数据收集与分析为刘兰,论文结果撰写为林晟、白建喜,论文讨论分析为林晟、张炳、吴典明
| [1] |
苏雁, 洪慧敏, 赵倩, 等. 纵隔生殖细胞肿瘤并发恶性血液病3例并文献复习[J]. 中华实用儿科临床杂志, 2022, 37(5): 377-381. Su Y, Hong HM, Zhao Q, et al. Mediastinal germ cell tumors and concurrent hematologic malignancy: a report of 3 cases with a literature review[J]. Chin J Appl Clin Pediatr, 2022, 37(5): 377-381. DOI:10.3760/cma.j.cn101070-20201012-01606 |
| [2] |
Calaminus G, Joffe J. Germ cell tumors in adolescents and young adults[J]. Prog Tumor Res, 2016, 43: 115-127. DOI:10.1159/000447081 |
| [3] |
施全, 王凤华, 高秋, 等. 儿童及青少年卵黄囊瘤的临床病理分析[J]. 中国妇幼健康研究, 2019, 30(3): 342-346. Shi Q, Wang FH, Gao Q, et al. Clinicopathological analysis of yolk sac tumor in children and adolescents[J]. Chin J Woman Child Health Res, 2019, 30(3): 342-346. DOI:10.3969/j.issn.1673-5293.2019.03.019 |
| [4] |
许恬逸, 董瑞. 儿童卵黄囊瘤病因研究进展[J]. 临床小儿外科杂志, 2021, 20(12): 1194-1200. Xu TY, Dong R. Research advances in etiology of yolk sac tumor in children[J]. J Clin Ped Sur, 2021, 20(12): 1194-1200. DOI:10.12260/lcxewkzz.2021.12.018 |
| [5] |
De Felici M, Klinger FG, Campolo F, et al. To be or not to be a germ cell: the extragonadal germ cell tumor paradigm[J]. Int J Mol Sci, 2021, 22(11): 5982. DOI:10.3390/ijms22115982 |
| [6] |
陈吉, 易军, 孙斌, 等. 肝外型肝母细胞瘤一例[J]. 中华小儿外科杂志, 2016, 37(4): 302-303. Chen J, Yi J, Sun B, et al. Extrahepatic hepatoblastoma: one case report[J]. Chin J Pediatr Surg, 2016, 37(4): 302-303. DOI:10.3760/cma.j.issn.0253-3006.2016.04.014 |
| [7] |
朱帅, 张大伟, 苏雁, 等. 伴有肝脏受累的神经母细胞瘤患儿临床特点及预后分析——单中心10年诊治总结[J]. 中国小儿血液与肿瘤杂志, 2019, 24(4): 186-191. Zhu S, Zhang DW, Su Y, et al. Clinical characteristics and prognosis of neuroblastoma with liver involvement in children: 10-year diagnostic & therapeutic experiences at a single center[J]. J China Pediatr Blood Cancer, 2019, 24(4): 186-191. DOI:10.3969/j.issn.1673-5323.2019.04.004 |
| [8] |
杨双风, 高军, 李航, 等. 新生儿神经母细胞瘤的影像学表现[J]. 中国医学影像学杂志, 2021, 29(10): 1028-1034. Yang SF, Gao J, Li H, et al. Imaging features of neuroblastoma in neonates[J]. Chin J Med Imaging, 2021, 29(10): 1028-1034. DOI:10.3969/j.issn.1005-5185.2021.10.015 |
| [9] |
张继军, 王隽, 苏明, 等. 卵巢成熟囊性畸胎瘤误诊或漏诊CT表现分析[J]. 实用放射学杂志, 2017, 33(12): 1895-1897. Zhang JJ, Wang J, Su M, et al. Analysis of CT manifestations of misdiagnosed or missed ovarian cystic mature teratomas[J]. J Pract Radiol, 2017, 33(12): 1895-1897. DOI:10.3969/j.issn.1002-1671.2017.12.022 |
| [10] |
胡赢, 韦成江, 龚晗, 等. 结直肠癌肝转移灶的影像学特征与病理微形态学特点的关系[J]. 临床与实验病理学杂志, 2022, 38(9): 1109-1112. Hu Y, Wei CJ, Gong H, et al. Relationship between imaging features and pathological micromorphological characteristics of liver metastases in colorectal cancer[J]. Chin J Clin Exp Pathol, 2022, 38(9): 1109-1112. DOI:10.13315/j.cnki.cjcep.2022.09.018 |
| [11] |
International Germ Cell Consensus Classification: a prognostic factor-based staging system for metastatic germ cell cancers. International Germ Cell Cancer Collaborative Group[J]. J Clin Oncol, 1997, 15(2): 594-603. DOI:10.1200/JCO.1997.15.2.594 |
| [12] |
宋君红, 高怡瑾, 潘慈, 等. 138例儿童颅外恶性生殖细胞肿瘤临床研究[J]. 现代肿瘤医学, 2019, 27(3): 468-471. Song JH, Gao YJ, Pan C, et al. Clinical observation of 138 children with extracranial malignant germ cell tumors[J]. J Mod Oncol, 2019, 27(3): 468-471. DOI:10.3969/j.issn.1672-4992.2019.03.027 |
 2026, Vol. 25
2026, Vol. 25


