2. 武汉科技大学医学院襄阳市第一人民医院研究生联合培养基地外科,襄阳 441000
2. Department of Surgery, Base of Postgraduate Cooperative Training, Xiangyang No.1 People's Hospital, School of Medicine, Wuhan University of Science & Technology, Xiangyang 441000, China
目前多数研究者将短肠综合征(short bowel syndrome, SBS)定义为肠道的一种严重消化及吸收不良状态,需要长期(超过6周)依赖肠外营养(parenteral nutrition, PN)。对于长期依赖PN而无法实现肠道自主性(enteral autonomy, EA)的患儿,可考虑手术治疗。手术方式多种多样,如短段结肠间置、纵向离断延长术(longitudinal intestinal lengthening and tailoring, LILT)及连续横贯肠成形术(serial transverse enteroplasty, STEP)等。2024年7月湖北省妇幼保健院收治了1例SBS患儿,采用可吸收线缝合创面代替吻合器行STEP,现结合文献复习报道如下。
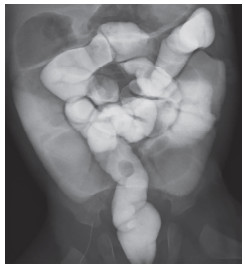
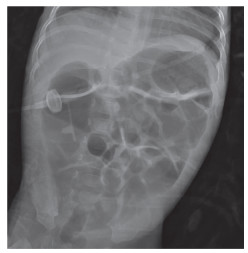
患儿女,2月5日龄,因“呕吐2天,发热1天”转至我院。患儿产前B型超声提示存在肠闭锁可能,于2024年5月9日顺产娩出,出生体重为2.37 kg。2024年5月10日在外院因多发性肠闭锁接受手术治疗,术后2个月患儿未能成功脱离PN,持续存在喂养不耐受的情况。在此期间,患儿反复出现重症感染,并且多次因血红蛋白降至84 g/L而接受输血治疗。既往外院血生化:白蛋白28.7 g/L。入院体格检查:体温38.2℃,体重2.2 kg,重度营养不良貌,皮下脂肪菲薄,腹部膨隆,可见肠型及腹壁静脉显露,右侧腹壁可见一长约4 cm的陈旧性手术疤痕,愈合良好,未触及明显腹部包块,肠鸣音稍亢进。初步诊断为营养不良、短肠综合征、先天性小肠闭锁术后。辅助检查:术前血红蛋白、白蛋白正常范围;血气检查提示:低磷、低镁、低氯;下消化道碘水造影提示结肠未见明显扩张及狭窄,左下腹肠管局限性狭窄,近端部分小肠扩张(图 1);腹部平片提示肠管充气扩张(图 2)。
|
图 1 本例SBS患儿术前下消化道碘水造影提示左下腹肠管狭窄,近端部分肠管扩张 Fig.1 Lower gastrointestinal tract iodine-water contrast examination of a SBS child hinted that intestinal stenosis was located in left lower quadrant with proximal intestinal tract dilation |
|
图 2 本例SBS患儿术前腹部平片提示肠管充气扩张 Fig.2 Preoperative abdominal radiograph of this SBS child revealed intestinal distension and intestinal gas distension |
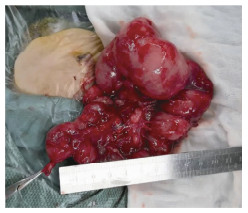
住院期间患儿反复出现呕吐、脓毒血症、体重增长不佳等状况,结合相关辅助检查,考虑为原小肠吻合口狭窄引起的肠梗阻合并短肠综合征,不排除近端肠管过度扩张后蠕动异常引起的狭窄可能。2024年9月9日行手术治疗,术中见肠管广泛粘连,原小肠吻合口粘连明显,仔细分离粘连后发现近端小肠约15 cm肠段扩张明显,直径约5 cm,扩张肠管全长约20 cm,经测量残存小肠全长约35 cm(图 3),探查可见回盲部、阑尾及结肠。切除原狭窄吻合口处肠管段约4 cm,用可吸收缝线缝合行肠管端端吻合。结合患儿临床表现及肠管扩张情况,决定实施STEP,用可吸收缝线缝合肠管切缘取代传统吻合器延长小肠。具体操作如下:选取距扩张段末端约3 cm处的肠管,在肠钳的辅助下垂直于小肠长轴方向进行横向裁剪,裁剪时保持肠系膜位于水平方向,在末端留下约2 cm肠管未裁剪,创面碘伏消毒后用5 - 0可吸收缝线连续横行缝合并6 - 0可吸收缝线间断行浆肌层缝合包埋。下一处裁剪距离此处约3 cm,按上述方式从对侧系膜缘处开始裁剪并缝合创面。重复上述步骤,裁剪时注意避开血管丰富区域,STEP后小肠长度约56 cm(延长约60%)。本例患儿手术顺利,术后16天转回当地医院指导过渡肠内营养(enteral nutrition, EN)并恢复经口喂养,深度水解配方奶粉喂养,出院时体重为3.2 kg,术后随访8个月,患儿未再接受PN支持治疗,每日摄入奶量550 mL左右,排便频率维持在每日4次,偶有稀水便,无发热、呕吐、腹胀等不适,生长发育较前改善,近期检查肝肾功能在正常范围内。
|
图 3 本例SBS患儿肠管外观情况,术中探查见残存小肠总长度约35 cm,其中约15 cm肠段扩张明显,最大直径约5 cm Fig.3 Intestinal tract morphology of this SBS child: Residual small intestine measured approximately 35 cm in total length.And a 15 cm segment exhibited marked dilatation with a maximal luminal diameter of approximately 5 cm. |
讨论 SBS主要是先天性肠管长度不足或者肠管大部分切除所致,SBS的主要病因包括坏死性小肠结肠炎、腹裂和肠闭锁等,其中约50%患儿为手术切除所致的获得性SBS[1-2]。SBS患者的肠上皮吸收面积减少或肠功能下降,导致营养物质吸收障碍,表现为呕吐、腹泻、电解质紊乱及生长迟缓等症状,难以满足正常生长发育的需要,因此SBS患者需要接受PN。但长期接受PN的患者可能出现肠衰竭相关肝损害(表现为胆汁淤积、脂肪变性、纤维化等)、胆石症、代谢性骨病、乳酸酸中毒及与中心静脉导管相关疾病等,从而影响患者预后[2],因此在医学允许的前提下应尽早实施EN。其可通过刺激肠黏膜增生、胃肠道激素及消化液分泌等机制促进肠道适应,在保障患儿正常生长发育的同时尽早实现EA,降低相关并发症风险[3]。有研究显示,部分患儿通过优化肠道适应机制可逐步脱离PN,最终实现EA,需要特别关注的是,残存肠道长度、回盲部保留状态、是否合并肝脏疾病以及胃肠动力正常与否,是决定患者能否成功实现EA的关键临床因素[4]。
对于EN增量受限且持续依赖PN的患者,需及时评估是否需要手术干预。目前公认的手术适应证为:①无法脱离PN(最常见);②肠管扩张(小肠直径≥4 cm)以及顽固性小肠细菌过度生长;③肠道排空过快[5]。手术时机的选择仍存在争议,更多与外科医师的经验有关。手术方式多种多样,对于单纯肠道排空过快的患者,可考虑人工瓣膜或括约肌构建术、短段结肠间置术及小段肠倒转间置术等;对于出现扩张的肠袢合并继发性肠蠕动障碍的患儿,可考虑尾状裁剪、螺旋缩窄延长术、LILT及STEP等[5-6]。
目前临床应用较多的是STEP,不仅可以缩小肠管直径,还可以延长肠管长度。该术式由Kim教授团队于2002年基于动物实验首次提出,其手术要点在于利用吻合器沿着扩张肠段的系膜缘及对系膜缘方向,以交替连续横向、部分重叠、垂直肠道长轴的方式创建形成锯齿形肠管通道,重复上述操作直至达到理想的肠管长度[7]。术中使用的吻合器利用不可吸收的钛钉达到组织固定的效果,其机制为在切口两侧各布置2~3排规律交错排列的钛钉,通过机械压闭从而闭合组织及血管,然后由内置切割刀进行组织离断[8]。相较于LILT,STEP有效降低了对肠系膜血管系统的损伤的风险,同时具有可重复性的优点,能根据病情需要进行多次手术[8]。而且STEP的临床应用范围较LILT更广泛,可用于超短肠综合征、十二指肠扩张等复杂病例。此外,STEP对肠道长度没有限制,但要求目标肠段的直径≥3.5 cm,且该术式改变了肠道肌纤维的正常排列方向,可能对肠道运动功能产生影响[9]。
综合患儿病情、家庭状况及器械条件等多方面因素考量,本例患儿采用手工缝合技术代替传统吻合器实施STEP,术后疗效满意。现有回顾性研究表明,在胃肠道手术中,吻合器缝合与传统手工缝合对吻合口发生渗漏及出血的概率无显著差异;但是该结论主要来自成人及年长儿童的数据,尚缺乏1岁以下婴儿的循证医学证据[10]。值得注意的是,有研究通过构建猪小肠模型对这两种缝合方式的力学性能进行了对比分析,结果显示手工缝合组发生吻合口破裂的压力范围显著高于吻合器组,且高年资外科医师组发生吻合口破裂的压力高于低年资医师组[11]。综上分析,我们认为该手术方式具有以下优势:①降低异物相关风险:术中未使用钛钉,不受器械限制,适用范围更广,降低了排异反应、炎症反应等的发生风险,减少了医疗费用,且有可能降低术后胃肠道出血及吻合口瘘的发生率;②术中可灵活调整:缝合时术者可以根据组织的张力、血运等情况,动态调整缝合的深度、宽度及力度等,特别是对于特殊解剖结构,此外高超的缝合技术可减少钛钉对肠黏膜的机械占位体积;③组织愈合特性更优:可吸收线经人体内酶解代谢反应后,创面瘢痕组织的功能逐渐恢复,其强度也将逐渐接近正常组织,从远期效果看肠管弹性更佳。但是,该改良STEP的长期临床疗效仍需进一步验证。
本例的手术方式存在以下方面的局限性:①肠腔的开放性操作增加了腹腔污染的概率,且创面对合的精确度依赖于手术者的经验,易发生错位,因此要求术者具有较高的手术水平;②术中的止血效果劣于钛钉导致出血量增多,可增加术后因出血过多出现的并发症概率;③手术时间延长,手术耐受性低的患者(如早产儿、低体重儿)可能会增加相关手术风险。本例手术中,我们采取了多种精细化操作以减少手术风险:首先,术中规范使用肠钳钳夹肠管以减少肠管出血;同时严格执行无菌规范如创面消毒等,尽可能降低腹腔污染风险。在肠系膜血管的处理方面,我们基于肠系膜血管解剖学特点,选择在血管稀疏区裁剪肠管,并且在肠系膜血管弓根部(主要针对三级或四级肠系膜血管弓)、距离肠管最近的位置进行血管结扎。
SBS的根治性手术为肠道移植术(intestinal transplantation, IT)。当出现下述情况之一方可考虑:①出现晚期和进行性肠衰竭相关肝损害;②丢失多个中心静脉导管部位导致难以维持PN;③超短小肠患者(儿童小肠长度<10 cm,成人<20 cm);④发现小肠中段以上的肠壁肌间神经节细胞缺(如Hirschsprung患者);⑤因感染性休克而入住重症监护室≥2次,大多数患儿在术后可停止PN,可提高SBS患儿的生存率(5年移植物和患者生存率分别为49%和66%)。但是进行了IT的患者易出现移植物感染、排斥反应和其他与免疫抑制相关的并发症,因此SBS患者应首先考虑药物治疗和非移植性手术。
综上所述,我们报道了1例采用手工缝合技术实施的改良STEP的成功案例,丰富国内SBS的外科治疗经验。改良STEP在异物相关风险、组织愈合特性等方面更具优势,手术安全可行,但其长期临床效果需要通过大样本、多中心的临床研究进行验证。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 彭慧玲负责临床资料收集、文献查找及分析、撰写论文;刘延龄、张惠茹,李雨珊负责临床资料收集、文献整理及分析、数据整理并制表;杨星海负责研究指导、论文审阅、经费支持
| [1] |
Cohran VC, Prozialeck JD, Cole CR. Redefining short bowel syndrome in the 21st century[J]. Pediatr Res, 2017, 81(4): 540-549. DOI:10.1038/pr.2016.265 |
| [2] |
Kaenkumchorn TK, Lampone O, Huebner K, et al. When parenteral nutrition is the answer: The case of pediatric intestinal rehabilitation[J]. Nutr Clin Pract, 2024, 39(5): 991-1002. DOI:10.1002/ncp.111799 |
| [3] |
Modi BP, Galloway DP, Gura K, et al. ASPEN definitions in pediatric intestinal failure[J]. JPEN J Parenter Enteral Nutr, 2022, 46(1): 42-59. DOI:10.1002/jpen.2232 |
| [4] |
Lakkasani S, Seth D, Khokhar I, et al. Concise review on short bowel syndrome: Etiology, pathophysiology, and management[J]. World J Clin Cases, 2022, 10(31): 11273-11282. DOI:10.12998/wjcc.v10.i31.11273 |
| [5] |
Höllwarth ME. Surgical strategies in short bowel syndrome[J]. Pediatr Surg Int, 2017, 33(4): 413-419. DOI:10.1007/s00383-016-4043-6 |
| [6] |
van Praagh JB, Hofker HS, Haveman JW. Comparing bowel leng-thening procedures: which, when, and why?[J]. Curr Opin Organ Transplant, 2022, 27(2): 112-118. DOI:10.1097/MOT.0000000000000957 |
| [7] |
Kim HB, Fauza D, Garza J, et al. Serial transverse enteroplasty (STEP): a novel bowel lengthening procedure[J]. J Pediatr Surg, 2003, 38(3): 425-429. DOI:10.1053/jpsu.2003.50073 |
| [8] |
Muff JL, Sokolovski F, Walsh-Korb Z, et al. Surgical treatment of short bowel syndrome-the past, the present and the future, a descriptive review of the literature[J]. Children (Basel), 2022, 9(7): 1024. DOI:10.3390/children9071024 |
| [9] |
Hommel MJ, van Baren R, Haveman JW. Surgical management and autologous intestinal reconstruction in short bowel syndrome[J]. Best Pract Res Clin Gastroenterol, 2016, 30(2): 263-280. DOI:10.1016/j.bpg.2016.03.006 |
| [10] |
Moursi AGA, Rohleder S, Christofi M, et al. Intestinal anastomosis during enterostomy takedown using a 5 mm miniature endostapler compared to conventional handsewn technique[J]. J Pediatr Surg, 2025, 60(3): 162041. DOI:10.1016/j.jpedsurg.2024.162041 |
| [11] |
McKinley TMR, Chow D, Livezey JB, et al. Impact of surgical experience on burst pressure of hand-sewn and stapled anastomoses[J]. J Surg Res, 2025, 310: 122-127. DOI:10.1016/j.jss.2025.03.063 |
 2025, Vol. 24
2025, Vol. 24


