2. 昆明医科大学附属儿童医院肿瘤科, 昆明 650100
2. Department of Oncology, Affiliated Children's Hospital, Kunming Medical University, Kunming 650100, China
多原发癌(multiple primary cancers, MPC)是指同一个体同时存在两种及以上组织学上不同的恶性肿瘤,这些肿瘤不是由于复发、转移或局部扩散引起,国内文献报道发病率为0.99%~1.3%,国外文献报道发病率为0.73%~11.7%,通常根据两种肿瘤发病间隔时间<6个月或≥6个月分为同时性或异时性[1-3]。神经母细胞瘤(neuroblastoma, NB)是儿童最常见的颅外实体肿瘤,占儿童恶性肿瘤病死率的10%~12%[4-5]。NB组织学类型包括NB、节细胞性神经母细胞瘤(ganglioneuroblastoma, GNB)和神经节细胞瘤(ganglioneuroma, GN),其中GNB生物学特性介于NB及GN之间,病理类型包括结节型(ganglioneuroblastoma-nodular, GNBn)和混合型(ganglioneuroblastoma-intermixed, GNBi)[6]。肾上腺皮质癌(adrenocortical carcinoma, ACC)是一种罕见的高度恶性内分泌肿瘤,发病率1/1 000 000~2/1 000 000,5岁以下儿童及40~50岁女性多见,预后较差,中位生存期约4年,5年总体生存率15%~44%[7-8]。本文回顾性分析昆明医科大学附属儿童医院收治的1例MPC患儿临床资料,并复习相关文献,总结ACC与GNBn的临床诊治经验。
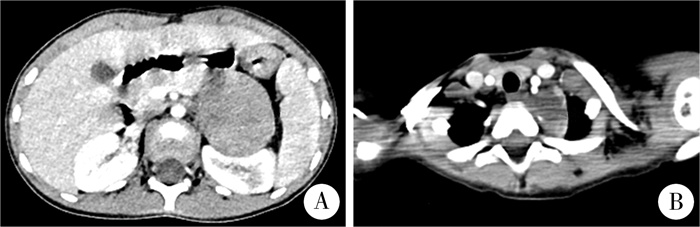
患儿,女,5岁2个月,因反复咳嗽1月余、发现胸腹腔肿物8 d于2023年11月20日就诊,腹部B超提示左侧腹部混杂回声;胸部CT提示右下肺炎征象,左上纵膈脊柱旁占位性病变,扫描范围内左上腹软组织密度影,建议完善增强扫描检查。入院后胸腹部增强CT提示左侧腹部脾胃肾间见一类圆形混杂密度灶,呈软组织密度,其内见多发斑片状钙化灶,边缘清楚,轻度强化,考虑:①神经源性肿瘤(神经母细胞瘤?);②左肾受压变形,部分肾盏及肾盂、输尿管上段稍扩张,输尿管壁增厚,左侧胰腺受推挤;③左上纵膈类椭圆形软组织、稍低密度灶,增强扫描部分明显强化,边界清楚,大小约2.7 cm×2.1 cm(图 1)。肿瘤标志物检测提示神经源特异性烯醇化酶轻度升高(17.22 ng/mL),甲胎蛋白、人绒毛膜促性腺激素、癌胚蛋白等均正常。肾上腺功能检查提示促肾上腺皮质激素、皮质醇水平均正常;甲状腺功能检查提示甲状腺素、促甲状腺素、三碘甲状腺原氨酸水平均正常。家族中无恶性肿瘤病史。
|
图 1 1例多原发癌患儿手术前胸腹部CT片 Fig.1 Preoperative chest and abdominal CT scans of one MPC child 注 A:左侧腹部肿块,疑神经源性肿瘤;B:左上纵膈低密度灶 |
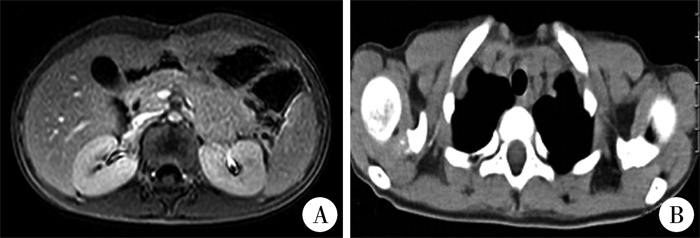
完善相关检查后行胸腔镜下左侧纵膈肿瘤切除术加开腹腹膜后肿瘤切除术。术中完整切除左侧纵膈肿瘤及腹膜后肿瘤,并清扫区域淋巴结。术中见左侧纵膈肿瘤位于后上纵膈脊柱旁,实性,约2.7 cm×2.1 cm×2.0 cm大小;腹腔肿瘤来源于左侧肾上腺,实性,约5.3 cm×5.0 cm×4.7 cm。术后病理检查提示:左纵膈节细胞性神经母细胞瘤(结节型),免疫组化结果:Syn(+)、NSE(+)、Cog(+)、PHOX2B(+)、CD56(+),NF(+)、S-100(+)、Ki-67(热点区10%+);左侧肾上腺皮质癌侵犯包膜,肾门淋巴结及肾周脂肪无肿瘤侵及;免疫组化结果:a-inhibin(+)、Vim(+)、MelanA(+)、Syn(散+)、CD56(散+)、P53(+)、Ki-67(热点区10%+)。基因扩增检测及分子核型分析均未见N-myc基因扩增。术后第7天患儿病情平稳出院,自行转诊至上海某医院继续治疗,经随访得知,患儿于该院接受依托泊苷+阿霉素+顺铂化疗,共4个疗程,并辅以米托坦靶向治疗。患儿于手术后8个月、化疗后3个月(此时患儿年龄5岁11个月)因双乳增大2个月在本院内分泌科诊断为外周性性早熟、肾上腺功能减退症及甲状腺功能减退症,予口服氢化可的松10 mg每日2次、优甲乐每日50 μg治疗。术后1年因肾上腺功能减退而停服米托坦。术后15个月复查胸部CT、腹部MRI未见明显异常(图 2),因肾上腺功能减退而继续口服氢化可的松。
|
图 2 1例多原发癌患儿术后18个月腹部MR及胸部CT片 Fig.2 Abdominal MR and chest CT scans of one MPC child at Month 18 post-operation 注 A:腹部MRI提示左肾边缘欠规则,其余无明显异常;B:胸部CT提示双肺及纵膈无明显异常 |
讨论 GNB是儿童最常见的原发性后纵隔肿瘤,常见于10岁以下儿童,尤其是1~2岁婴幼儿,青少年及成年人较少见[9]。该病起源于原始神经外胚层神经嵴细胞,可发生于肾上腺、后纵隔、颈部和盆腔,约15%的神经源性肿瘤发生在纵隔,原发于纵膈的NB预后较腹膜后及肾上腺NB好[10-11]。GNB与NB的重要病理学区别在于GNB组织中部分区域瘤细胞向神经母细胞分化,其内含分化程度不同的神经母细胞,因此GNB基本组织学分类主要依据施万细胞丰富程度及神经母细胞分化程度:GNBi施万细胞间质丰富,占肿瘤组织50%以上,成纤维背景中分布成熟或部分成熟神经节细胞及散在神经母细胞;研究显示大部分GNBi肿瘤局限,影像学形态较规则、轮廓更清晰,且多无N-myc基因扩增,也较少出现包埋血管情况,属于预后良好类型,手术完整切除后多可获得良好预后[12-13]。GNBn主要由神经母细胞组成,瘤体被纤维血管分割为分叶状结构,缺少施万细胞间质;低危GNBn的治疗以手术切除为主;中危GNBn手术后需辅以化疗,对出现术后肿瘤进展及耐药的患者需进行放疗;高危GNBn多采用术前辅助化疗、手术切除、术后辅助放化疗、自体干细胞移植及靶向治疗的综合治疗模式。尽管如此,高危GNBn患者的5年生存率仍不足50%[12]。
ACC的发病机制目前尚不明确,TP53基因突变、LncRNAs失调、IGF2及甲基化被认为与ACC发病有关,少数ACC病例与遗传性肿瘤综合征相关,包括Li-Fraumeni综合征、Lynch综合征、MEN-1和家族性腺瘤性息肉[14-15]。目前对于ACC的治疗建议主要基于回顾性研究和单臂Ⅱ期研究,对于Ⅰ~Ⅱ期ACC,手术仍然是首选治疗方案,不论是开放式肾上腺切除术或腹腔镜肾上腺切除术,保证切缘无肿瘤细胞残留(resection 0, R0)是治愈ACC的关键[16]。晚期患者需根据肿瘤分期制定治疗方案,目前主要治疗方案为米托坦联合依托泊苷、阿霉素、顺铂(为一线化疗方案)以及放疗等联合治疗[17]。一项针对ACC患者的Ⅲ期随机试验研究显示,与米托坦-链脲霉素相比,米托坦-依托泊苷-阿霉素-顺铂方案的中位无进展生存期延长了5个月,疾病控制率为58.3%[18-19]。
MPC的病因尚未明确,现有研究指出,遗传易感性及基因突变是MPC发病的重要危险因素,其他危险因素还包括衰老、放化疗史、环境暴露、免疫抑制、生活方式(吸烟、饮酒)或激素因素等;此外,免疫功能受损的个体发生MPC的风险较高,如在肾移植受者中,MPC的发生率约13.4%,高于一般人群[20]。
当临床证实为MPC时,应对每个肿瘤进行独立评估和分期,对于无手术禁忌的患者,应予同时切除两种肿瘤,必要时可联合放化疗、内分泌治疗或其他治疗方法;当两种肿瘤不适合同时手术时,对患者生活质量或预后影响更大的肿瘤应优先治疗[1]。MPC的预后主要取决于原发肿瘤类型和分期,有研究显示同时性肿瘤是影响预后的危险因素[2]。
本例患儿同时发生ACC及GNBn,既往体健,无放化疗史,亦无家族恶性肿瘤史及激素使用史等,考虑其发病多与基因突变相关,进一步完善全外显子基因检测可能对明确发病机制有一定帮助。治疗上,在根治性切除两个部位肿瘤后,根据欧洲肾上腺肿瘤网络研究分期系统及神经母细胞瘤国际委员会临床分期系统,该例ACC分期为Ⅲ期、GNBn为Ⅰ期,由于Ⅲ期ACC恶性程度及复发率高于Ⅰ期GNBn,且Ⅲ期ACC的化疗药物部分覆盖Ⅰ期GNBn的化疗药物,因此选择ACC化疗方案是合理的。其次,由于患儿ACC Ki-67>10%并侵犯包膜,因此术后辅以口服米托坦治疗,但患儿术后8个月出现双侧乳腺增大,在排除ACC复发后,诊断为外周性早熟与甲状腺功能减退症,因米托坦可导致激素结合球蛋白水平增加(性激素结合球蛋白、甲状腺结合球蛋白),因此考虑与口服米托坦相关:另外,米托坦可通过抑制类固醇激素合成,诱导肾上腺束状带、网状带细胞凋亡[21]。
综上所述,临床上GNBn并发ACC的MPC罕见,发病机制有待进一步研究,两种肿瘤分期不同,治疗方案及预后差异较大,对于此类患者,积极手术切除及辅以术后综合治疗有利于改善患儿预后,延长生存期。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 计凤鸣负责论文撰写,张黄成昊负责文献检索,张昆负责数据收集,宋元华、严兵负责研究结果分析与讨论,杨震负责全文知识性内容的审读与修正
| [1] |
Zhai CY, Cai YL, Lou F, et al. Multiple primary malignant tumors-A clinical analysis of 15, 321 patients with malignancies at a single center in China[J]. J Cancer, 2018, 9(16): 2795-2801. DOI:10.7150/jca.25482 |
| [2] |
Alhamadh MS, Alanazi RB, Algarni ST, et al. A descriptive study of the types and survival patterns of Saudi patients with multiple primary solid malignancies: a 30-year tertiary care center experience[J]. Curr Oncol, 2022, 29(7): 4941-4955. DOI:10.3390/curroncol29070393 |
| [3] |
王鑫, 俞凯杰, 詹镇润, 等. 同时性三重原发癌合并胃间质瘤1例[J]. 肿瘤预防与治疗, 2023, 36(7): 611-615. Wang X, Yu KJ, Zhan ZR, et al. Simultaneous triple primary malignancies plus gastric stromal tumor: one case report[J]. J Cancer Control Treat, 2023, 36(7): 611-615. DOI:10.3969/j.issn.1674-0904.2023.07.011 |
| [4] |
Li R, Polishchuk A, DuBois S, et al. Patterns of relapse in high-risk neuroblastoma patients treated with and without total body irradiation[J]. Int J Radiat Oncol Biol Phys, 2017, 97(2): 270-277. DOI:10.1016/j.ijrobp.2016.10.047 |
| [5] |
Zeineldin M, Patel AG, Dyer MA. Neuroblastoma: when differentiation goes awry[J]. Neuron, 2022, 110(18): 2916-2928. DOI:10.1016/j.neuron.2022.07.012 |
| [6] |
杨瑞雪, 王晓琳, 王一超, 等. 结节型节细胞神经母细胞瘤3例并文献复习[J]. 中国组织化学与细胞化学杂志, 2020, 29(3): 264-267, 273. Yang RX, Wang XL, Wang YC, et al. Nodular ganglioneuroblastoma: a report of 3 cases with a literature review[J]. Chin J Histochem Cytochem, 2020, 29(3): 264-267, 273. DOI:10.16705/j.cnki.1004-1850.2020.03.011 |
| [7] |
中国医师协会泌尿外科分会. 肾上腺皮质癌诊治专家共识[J]. 现代泌尿外科杂志, 2021, 26(11): 902-908. Branch of Urology, Chinese Medical Doctor Association. Expert Consensus on Diagnosing and Treating Adrenal Cortical Cancer[J]. J Mod Urol, 2021, 26(11): 902-908. DOI:10.3969/j.issn.1009-8291.2021.11.002 |
| [8] |
Li P, Su XN, Zhang XT, et al. Prognostic factors of adrenocortical carcinoma: experience from a regional medical center in eastern China[J]. Int J Gen Med, 2023, 16: 453-465. DOI:10.2147/IJGM.S399473 |
| [9] |
Zhang SL, Xiao BL, Zhang YW, et al. Retroperitoneal ganglioneuroblastoma with postoperative stress ulcer perforation in an adolescent: a case report and review of the literature[J]. Oncol Lett, 2022, 24(1): 208. DOI:10.3892/ol.2022.13329 |
| [10] |
Zhang QY, Zhou TT, Hou PM, et al. A single-center study of thoracoscopic surgery in the treatment of pediatric mediastinal neurogenic tumors[J]. Thorac Cancer, 2023, 14(1): 44-51. DOI:10.1111/1759-7714.14708 |
| [11] |
Heidari Z, Kaykhaei MA, Jahantigh M, et al. Adrenal ganglioneuroblastoma in an adult: a rare case report[J]. Int J Endocrinol Metab, 2018, 16(1): e63055. DOI:10.5812/ijem.63055 |
| [12] |
王浩入, 陈欣, 张黎, 等. 儿童腹膜后结节型和混合型节细胞神经母细胞瘤的临床及CT表现[J]. 中国临床医学影像杂志, 2022, 33(4): 279-282. Wang HR, Chen X, Zhang L, et al. CT findings and clinical features of retroperitoneal nodular and intermixed ganglioneuroblastoma in children[J]. J Chin Clin Med Imaging, 2022, 33(4): 279-282. DOI:10.12117/jccmi.2022.04.011 |
| [13] |
He WG, Yan Y, Tang W, et al. Clinical and biological features of neuroblastic tumors: a comparison of neuroblastoma and ganglioneuroblastoma[J]. Oncotarget, 2017, 8(23): 37730-37739. DOI:10.18632/oncotarget.17146 |
| [14] |
张琼, 任静祎, 纪洪辰, 等. 肾上腺皮质癌1例报道并文献回顾[J]. 现代肿瘤医学, 2021, 29(23): 4153-4158. Zhang Q, Ren JY, Ji HC, et al. Adrenocortical carcinoma: one case report with a literature review[J]. J Mod Oncol, 2021, 29(23): 4153-4158. DOI:10.3969/j.issn.1672-4992.2021.23.017 |
| [15] |
Lai GC, Liu H, Deng JL, et al. The characteristics of tumor microenvironment predict survival and response to immunotherapy in adrenocortical carcinomas[J]. Cells, 2023, 12(5): 755. DOI:10.3390/cells12050755 |
| [16] |
Margonis GA, Kim Y, Prescott JD, et al. Adrenocortical carcinoma: impact of surgical margin status on long-term outcomes[J]. Ann Surg Oncol, 2016, 23(1): 134-141. DOI:10.1245/s10434-015-4803-x |
| [17] |
Fassnacht M, Assie G, Baudin E, et al. Adrenocortical carcinomas and malignant phaeochromocytomas: ESMO-EURACAN Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2020, 31(11): 1476-1490. DOI:10.1016/j.annonc.2020.08.2099 |
| [18] |
Hescot S, Debien V, Hadoux J, et al. Outcome of adrenocortical carcinoma patients included in early phase clinical trials: results from the French network ENDOCAN-COMETE[J]. Eur J Cancer, 2023, 189: 112917. DOI:10.1016/j.ejca.2023.05.006 |
| [19] |
Fassnacht M, Terzolo M, Allolio B, et al. Combination chemotherapy in advanced adrenocortical carcinoma[J]. N Engl J Med, 2012, 366(23): 2189-2197. DOI:10.1056/NEJMoa1200966 |
| [20] |
Nyqvist J, Kovács A, Einbeigi Z, et al. Genetic alterations associated with multiple primary malignancies[J]. Cancer Med, 2021, 10(13): 4465-4477. DOI:10.1002/cam4.3975 |
| [21] |
Riedmeier M, Antonini SRR, Brandalise S, et al. International consensus on mitotane treatment in pediatric patients with adrenal cortical tumors: indications, therapy, and management of adverse effects[J]. Eur J Endocrinol, 2024, 190(4): G15-G24. DOI:10.1093/ejendo/lvae038 |
 2025, Vol. 24
2025, Vol. 24


