2. 山东大学药学院临床药学,济南 250012
2. Department of Clinical Pharmacy, School of Pharmaceutical Sciences, Shandong University, Jinan 250012, China
颅骨肿物在儿童及成人均可发生,包括但不限于郎格罕细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)、骨纤维结构不良(osteofibrous dysplasia,OFD)、颅骨筋膜炎、骨瘤、骨巨细胞瘤、尤文氏肉瘤、转移癌等[1-6]。手术切除颅骨肿物后会产生颅骨缺损,颅骨缺损可能造成颅内压不稳定、脑血流及脑脊液流动异常、脑功能异常等,往往需要人工材料进行颅骨修补,即颅骨成形术[7]。然而,不同部位颅骨的手术难度及策略各不相同。幕上或幕下凸面的颅骨肿物切除相对简单,颅底骨肿物的手术难度较大,而静脉窦相关颅骨肿物的手术治疗较少被单独讨论。山东大学齐鲁医院近年来收治儿童静脉窦相关颅骨肿物9例,均采取手术切除并行一期人工颅骨成形术,效果较好,现报告如下。
资料与方法 一、临床资料本研究为回顾性研究。收集2019年1月至2024年1月于本院手术治疗的儿童静脉窦相关颅骨病变患儿临床资料。本研究已取得山东大学齐鲁医院伦理委员会审核批准(KYLL-202312(YJ)-017)。患儿监护人均知情并签署知情同意书。病例纳入标准:①年龄小于18岁;②颅骨肿物与静脉窦关系密切;③术前定制聚醚醚酮(poly-ether-ether-ketone,PEEK)人工颅骨并行一期人工颅骨成形术。排除标准:①由于其他原因仅切除病变而未修补颅骨;②患儿家属不配合随访。
共纳入符合纳入排除标准病例9例,男性7例、女性2例,年龄4~13岁,中位年龄10岁。临床表现因病变位置及侵袭范围而不同,以头皮下肿块为最常见症状。其中,与上矢状窦相关5例,与窦汇区相关3例,与乙状窦相关1例。病变部位:额部2例,顶部2例,枕部5例。收集患儿临床特点、影像学结果、手术策略、治疗结果以及随访情况。
二、手术策略均行肿物切除术并一期行颅骨缺损修补术,修补材料均为术前定制的PEEK。术前根据薄层颅脑CT及MRI数据,利用IMPAX软件创建三维骨成像,勾画出病变切除范围及颅骨修补设计图。将手术方案告知患儿直系家属,征得其知情同意,再将数据及方案交予生产方(西安康拓医疗技术股份有限公司),定制个性化PEEK及条状金属导板,灭菌备用。术中严格保持无菌原则,以金属导板及无菌标记笔将预设的切除范围标记在颅骨表面。切除肿物后,对于肿物边缘骨质以高速磨钻打磨及咬骨钳咬除,直至PEEK能够顺利嵌入、外观满意,再以钛钉及连接片固定。术中切除病变时加强附近神经的保护,小心分离肿物与静脉窦。
结果 一、影像学特点本组病例中,5例LCH患儿CT及MRI表现为信号均匀或不均匀的软组织影,CT可见颅骨骨质破坏,MRI可见病变边缘强化。1例颅骨筋膜炎影像学表现类似于LCH,也存在骨质破坏及不均匀强化,有时单凭影像学较难区分。1例骨纤维结构不良表现为均匀或不均匀磨玻璃样信号的骨质病变。1例骨瘤影像学表现为增生性的均匀一致高密度影,较少有骨质破坏。术前磁共振静脉成像(magnetic resonance venography,MRV)对静脉窦与病变的三维关系有较好提示,本组6例患儿硬脑膜、帽状腱膜及皮下组织受到侵袭,病变长径1.5~13.5 cm。
二、治疗结果及术后病理检查结果术后病理检查证实为LCH 5例(图 1),非霍奇金B淋巴母细胞性淋巴瘤1例(图 2),骨纤维结构不良1例(图 3),颅骨筋膜炎1例,骨瘤1例。1例骨纤维结构不良及1例淋巴瘤为大部切除病变,其余7例为全切除病变。修补材料均采用PEEK。所有患儿术中无一例静脉窦损伤、脑损伤等并发症。术后无一例出现出血、感染、切口愈合不良等并发症。1例术后出现皮下积液,予消毒后局部穿刺抽吸积液并加压包扎,于出院前积液消退。
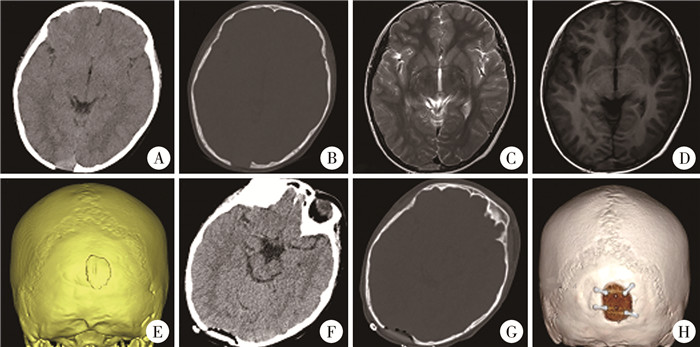
|
图 1 1例朗格罕细胞组织细胞增生症患儿的影像学资料 Fig.1 Imaging data of a child with LCH 注 A:术前颅脑CT轴位脑窗;B:术前颅脑CT轴位骨窗;C:颅脑MRI轴位T2;D:颅脑MRI轴位T1;E:术前颅脑CT骨窗三维重建;F:术后颅脑CT轴位脑窗;G:术后颅脑CT轴位骨窗;H:随访时颅脑CT骨窗三维重建 |
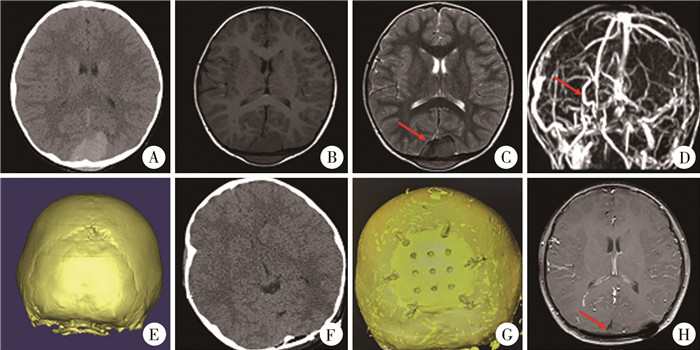
|
图 2 1例淋巴瘤患儿的影像学资料 Fig.2 Imaging data of a child with lymphoma 注 A:术前颅脑CT轴位脑窗;B:颅脑MRI轴位T1;C:颅脑MRI轴位T2,红色箭头提示上矢状窦受压移位;D:术前颅脑MRV,红色箭头提示上矢状窦受压移位;E:术前颅脑CT骨窗三维重建;F:术后颅脑CT轴位脑窗;G:随访时颅脑CT骨窗三维重建;H:随访时颅脑增强MRI轴位T1,红色箭头提示上矢状窦复位,局部无肿瘤复发 |
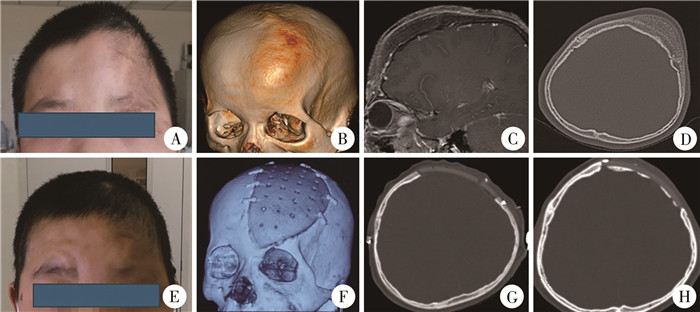
|
图 3 1例骨纤维结构不良患儿影像学资料 Fig.3 Imaging data of a child with OFD 注 A:术前外观,见左侧额顶及眉弓异常凸起;B:术前颅脑CT骨窗三维重建;C:术前颅脑MRI-T1增强矢状位;D:术前颅脑CT轴位骨窗;E:术后外观,见左侧额顶及眉弓形态正常;F:术后颅脑CT骨窗三维重建;G:术后颅脑CT轴位骨窗;H:随访时颅脑CT轴位骨窗 |
患儿均获随访,随访时间为术后1~6年,无一例复发或远期并发症发生。LCH患儿经术后风险评估(包括PET、X光、超声、血液学检查、骨髓穿刺活检等)后,4例予随诊;1例因超声检查出颈部淋巴结异常予化疗。骨瘤、骨纤维结构不良患儿均采取随诊策略。上述患儿随访期间均未见复发,正常生活。1例颅骨淋巴瘤患儿术中大部切除病变,术后进行放射治疗及化学治疗,随访5年无复发。
讨论儿童颅骨肿物可大体分类为非肿瘤性疾病及肿瘤性疾病。本组患儿以肿瘤性疾病为多(8/9),其中LCH最多(5/9)。就性别而言,男性占多数(7/9)。这可能与儿童颅骨疾病谱有关。本研究主要观察对象为与静脉窦相关的骨肿物,故病变以位于额、顶、枕部居多。本病较少见于婴幼儿,本组患儿发病年龄4~13岁,中位年龄10岁。
LCH是一种罕见的造血系统髓系前体细胞来源肿瘤。相比成人及青年,该病更常见于低龄儿童。患儿临床表现复杂,文献报道根据受累及系统的数量、是否累及危险器官、是否存在多灶病变、是否存在颅骨特殊部位的孤立病变(眼眶、颞骨/乳突、蝶骨、颧骨、筛骨、上颌骨、鼻窦等前颅底或中颅底、椎骨损害)进行危险程度分组[8-10]。典型影像学表现为无硬化环溶骨性骨质破坏[11]。如果合并多系统病变或多骨病变,或者发生于颅骨特殊部位的孤立病变,即使切除干净也需要化疗,或者仅取活检后进行化疗[8, 10]。对于单发且不累及特殊部位的颅骨孤立病变,可医学观察,也可局部手术治疗,无需化疗[8, 11]。手术时需注意保护静脉窦,若术中见静脉窦硬膜与LCH粘连紧密,宜尽可能全切肿瘤后,以神经剥离子及15号小圆刀片搔刮硬膜并低功率轻微电灼,以减少复发的可能。
骨纤维结构不良存在自限性,在青春期结束后可能停止进展。少年及儿童的单纯颅骨骨纤维结构不良,若未造成颅神经压迫症状且未引发美观问题,原则上首选随诊[12]。若随诊期肿物增长迅速,或出现颅神经压迫症状,或出现血清碱性磷酸酶迅速增高等明显进展表现,可考虑积极手术,但仍以神经减压或部分切除达到美观为目的[5, 12-13]。术后可选择临床观察,或使用唑来膦酸缓解病情进展[12]。若病变位于颅盖骨,凸出明显且影响美观者,可积极手术[5, 12-13]。本组1例存在手术指征,虽然跨过上矢状窦,但术中发现与静脉窦并无明显粘连,因此,术中切除骨病变及保护静脉窦相对容易。
1例非霍奇金B淋巴母细胞性淋巴瘤由于是单发,且全身无其他病灶,一般状况良好,故而选择了积极手术后再行放射治疗及化学治疗。术前影像学检查提示肿瘤侵袭广泛,骨瓣内外均有浸润,且与静脉窦关系紧密。术中见烂肉状肿瘤组织侵犯静脉窦内,窦壁及窦内瘤组织未强行切除,以免损伤静脉窦而造成失血过多或因止血而导致静脉窦栓塞。手术的目的在于最大程度减少肿瘤负荷,术后再辅以局部放射治疗及化学治疗。
另外,1例颅骨筋膜炎虽然病变边界欠清楚,但其质地较软,且与静脉窦粘连不紧密,故切除较彻底。对于未影响美观或无神经卡压的骨瘤可以仅随诊。本组1例骨瘤由于明显影响外观而采取切除手术,术中见肿瘤与静脉窦未粘连,较易切除。
在处理大脑或小脑凸面非静脉窦处的颅骨肿物时,如果病变侵犯硬脑膜且临床考虑存在侵袭性或恶性可能,可考虑将受累及硬脑膜一并切除,再用人工硬脑膜或自体筋膜修补缺损。而颅脑静脉窦是静脉血回流的重要通道,近颅骨处静脉窦壁为单层硬脑膜,如术中操作不当可导致大量出血或静脉窦栓塞,处理病变时须特别谨慎,以免损伤静脉窦。切除静脉窦相关颅骨肿物时需综合考虑多种因素,包括肿物性质、是否需要放射治疗或化学治疗等辅助治疗、肿物与静脉窦粘连程度,以及是否侵犯静脉窦等。原则上,良性肿物界限清楚,应选择保护静脉窦前提下的全切除肿物。对于恶性肿物,若粘连不紧也应争取全切除或次全切除;若粘连紧密甚至侵犯静脉窦,则不必强求全切除,窦壁及窦内残留病变可待后续辅助治疗。不推荐切除瘤化的静脉窦壁后再行人工硬脑膜或自体筋膜重建静脉窦壁的方法。术前利用MRV评估肿物与静脉窦的关系,有利于术中切除肿物前做出预判(图 2)。
文献报道1岁以内婴儿的小型颅骨缺损(小于3 cm)骨再生修复的可能性较大;随着年龄增大,骨缺损处骨再生修复能力明显下降[7]。如颅骨肿物病变已明显破坏骨膜甚至帽状腱膜及皮下组织,骨再生修复将更加困难。本组淋巴瘤及所有LCH患儿病变处骨膜均受到侵袭或明显破坏,其他患儿虽然骨膜完好,但病变面积大、切除范围广,且患儿年龄偏大,切除病变后颅骨缺损难以骨再生修复,因此,修补颅骨缺损是必要的。为了尽量减少病变残留,所有病例均由病变边缘外扩3 mm至1 cm去除骨缘骨质,建议术前根据影像学资料,预判切除范围,以患儿正常侧颅骨形态镜像化定制人工颅骨,以便术中切除病变后同时行一期颅骨缺损修补,其意义在于尽快重建颅腔完整性,保护脑组织和静脉窦,维护颅内压稳定,避免二期修补的再次手术伤害。
常用的颅骨修补材料包括钛网、PEEK、羟基磷灰石等[14]。目前国际上关于儿童颅骨缺损修补的最佳材料尚没有统一标准,PEEK具有刚性大、不导电、隔绝温度、无影像学伪影、生物相容性好等优点,是目前国内外首选的人工颅骨材料[14]。但PEEK为嵌入式修补材料,手术难度稍高。钛网为覆盖式修补材料,成本低,手术难度低,也是可选材料。本组随访无一例发生人工颅骨与自体骨生长冲突、移位、脱落、破碎等情况,效果良好。
总之,儿童静脉窦相关颅骨肿物较其他部位颅骨肿物的手术风险高、难度大。术前评估影像学特点,预判肿物与静脉窦的关系;术中注意仔细解剖及剥离,争取最大化切除;术后合理使用放射治疗及化学治疗,对获得良好预后有重要意义。建议术前定制人工颅骨,术中一期进行颅骨缺损修补,以达到恢复颅腔完整性的目的。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 王延召,王传伟负责文献检索;王传伟,宫杰负责论文设计;王延召,杨晨,张润鲁,邱伟,卜佳伟负责数据收集;王延召,杨晨,张润鲁,邱伟,卜佳伟,王传伟,宫杰负责研究结果分析与讨论;王延召,杨晨,张润鲁,邱伟,卜佳伟,王传伟,宫杰负责论文撰写;王延召,杨晨,张润鲁,王传伟,宫杰负责全文知识性内容的审读与修正
| [1] |
Wei M, Jiang WB, Wang R, et al. Langerhans cell histiocytosis of the skull in 23 children[J]. Eur J Med Res, 2024, 29(1): 136. DOI:10.1186/s40001-024-01727-5 |
| [2] |
Martin E, Senders JT, Ter Wengel PV, et al. Treatment and survival of osteosarcoma and Ewing sarcoma of the skull: a SEER database analysis[J]. Acta Neurochir (Wien), 2019, 161(2): 317-325. DOI:10.1007/s00701-018-3754-y |
| [3] |
Wagner RD, Wang EK, Lloyd MS, et al. Cranial fasciitis: a systematic review and diagnostic approach to a pediatric scalp mass[J]. J Craniofac Surg, 2016, 27(1): e65-e71. DOI:10.1097/SCS.0000000000002230 |
| [4] |
Langlie JA, Hullfish H, Jabori SK, et al. Diagnosis and management of craniofacial osteomas[J]. J Craniofac Surg, 2023, 34(5): 1515-1521. DOI:10.1097/SCS.0000000000009395 |
| [5] |
Dalle Carbonare M, Manisali M. Surgical management of syndromic versus non-syndromic craniofacial fibrous dysplasia: a systematic review and meta-analysis[J]. Br J Oral Maxillofac Surg, 2022, 60(9): 1166-1175. DOI:10.1016/j.bjoms.2022.06.002 |
| [6] |
Villavisanis DF, Schmidt RJ, Napoli JA. Pediatric maxillary giant cell tumors: surgical management by transoral and endoscopic transnasal enucleation and curettage[J]. J Craniofac Surg, 2022, 33(7): e747-e750. DOI:10.1097/SCS.0000000000008689 |
| [7] |
Sveikata L, Vasung L, El Rahal A, et al. Syndrome of the trephined: clinical spectrum, risk factors, and impact of cranioplasty on neurologic recovery in a prospective cohort[J]. Neurosurg Rev, 2022, 45(2): 1431-1443. DOI:10.1007/s10143-021-01655-6 |
| [8] |
Goyal G, Tazi A, Go RS, et al. International expert consensus recommendations for the diagnosis and treatment of Langerhans cell histiocytosis in adults[J]. Blood, 2022, 139(17): 2601-2621. DOI:10.1182/blood.2021014343 |
| [9] |
尹国阳, 刘翠翠, 肖以磊, 等. 颅骨朗格汉斯组织细胞增生症的临床特点及诊疗体会[J]. 中华神经医学杂志, 2021, 20(5): 495-500. Yin GY, Liu CC, Xiao YL, et al. Clinical characteristics and diagnosis and treatment experiences of Langerhans cell histocytosis in skull[J]. Chin J Neuromedicine, 2021, 20(5): 495-500. DOI:10.3760/cma.j.cn115354-20200901-00701 |
| [10] |
Döring K, Ivanyi P, Lanfermann H, et al. Langerhans cell histiocytosis involving the temporal bone with destruction and subsequent reossification of the bony labyrinth boundaries[J]. Rofo, 2024, 196(10): 1063-1067. DOI:10.1055/a-2254-5536 |
| [11] |
李春旺, 尹一伟, 蔡齐芳, 等. 儿童朗格汉斯细胞组织细胞增生症累及中枢神经系统及颅面骨的影像学特征分析[J]. 临床小儿外科杂志, 2023, 22(8): 768-772. Li CW, Yin YW, Cai QF, et al. Imaging features of Langerhans cell histiocytosis involving central nervous system and craniofacial bone in children[J]. J Clin Ped Sur, 2023, 22(8): 768-772. DOI:10.3760/cma.j.cn101785-202305023-013 |
| [12] |
Ishida K, Sakamoto Y, Kosugi K, et al. The long-term natural history of fibrous dysplasia[J]. J Craniofac Surg, 2024, 35(6): e540-e541. DOI:10.1097/scs.0000000000010245 |
| [13] |
Gharibi Loron A, Tunaboylu MF, Bite U. Technologically comprehensive reconstruction of fronto-orbito-sphenoidal craniofacial fibrous dysplasia[J]. J Craniofac Surg, 2025, 36(1): 58-60. DOI:10.1097/scs.0000000000010514 |
| [14] |
Frassanito P, Beez T. Cranial repair in children: techniques, materials, and peculiar issues[J]. Adv Tech Stand Neurosurg, 2024, 49: 307-326. DOI:10.1007/978-3-031-42398-7_14 |
 2025, Vol. 24
2025, Vol. 24


