淋巴管畸形(lymphatic malformations, LMs)多为淋巴系统的先天性发育异常,每2 000~6 000例活产婴儿中就有1例发生[1-2]。先天性LMs多见于淋巴丰富的部位(如头颈部、腋窝、纵隔、腹股沟和腹膜后),最多见于面颈部,腹部位置相对少见[3]。对LMs遗传学和分子生物学的认识较少,目前认为RASA1基因突变可能与其有关[4]。义乌市妇幼保健院于2021年8月至2022年9月诊治了3例儿童腹膜后LMs,现报告如下。
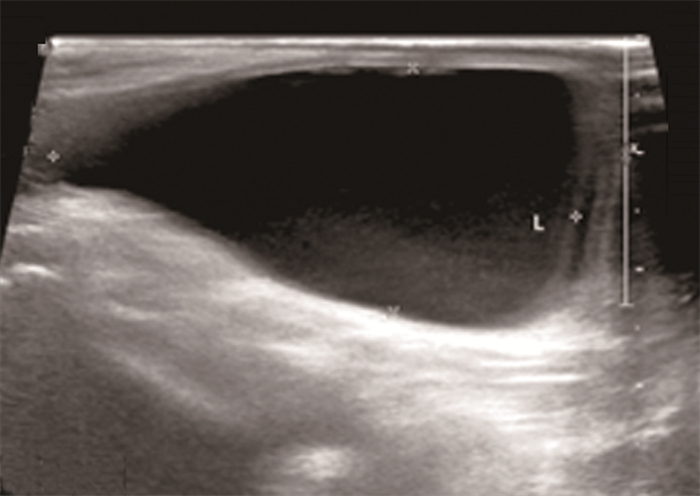
病例1, 男,2岁,因“左侧腹股沟区肿物2个月”入院,查体左侧腹股沟区触及肿物,质软,按压不能回纳入腹腔,透光试验阳性。彩超检查:左侧腹股沟处睾丸上方可见45 mm×21 mm液性暗区(图 1)。术前诊断为左侧精索鞘膜积液。术中腹腔镜下见左侧腹膜后近内环口处一大小约4 cm×2 cm囊肿,部分向下延伸至左侧腹股沟管处,向上沿髂血管方向延伸,腔镜下予以完整切除,同时结扎鞘状突。术后病理检查提示为LMs。术后6个月复查无复发。
|
图 1 淋巴管畸形患儿(病例1)超声检查,见液性暗区 Fig.1 Ultrasonographic detection of Case No.1 with lymphatic malformation revealed dark fluid areas |
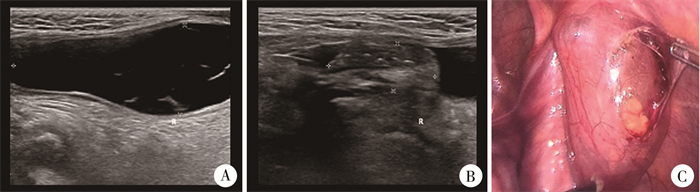
病例2,男,3岁,因“右侧腹股沟区肿物1年”入院,查体右侧腹股沟区睾丸上方触及包块,质软,透光试验阳性,挤压后部分肿物可回纳腹腔。彩超检查提示:右侧腹股沟区睾丸上方可见约50 mm×20 mm液性暗区,内可见条状光带分隔(图 2A),右侧腹股沟区见约24 mm×11 mm疝囊团块,内容物为肠管(图 2B)。术前诊断为右侧精索鞘膜积液合并腹股沟斜疝。手术时,患儿取平卧位,麻醉成功后,挤压腹股沟肿物,部分肿物回纳后不再突出,术中腹腔镜探查见内环口后方腹膜后约3 cm×2 cm×2 cm椭圆型肿物,考虑腹膜后囊肿,部分囊肿通过右侧未闭鞘状突向下疝入至腹股沟管处,打开腹膜可见囊肿与周围组织有一定间隙(图 2C),无明显粘连,囊壁光滑,保护好输精管及精索血管,分离囊肿,助手同时适当向腹腔推挤右侧阴囊及腹股沟管,辅助将囊肿更多暴露于腹腔,利于完整切除,遂连同鞘状突内部分,腔镜下予以完整切除,见右侧内环口缺损约1.5 cm并予以结扎。术后诊断:右侧腹股沟区腹膜后LMs合并腹股沟斜疝。由于LMs较大,存在时间长,使右侧内环口缺损大,患儿腹腔压力增高时,部分肠管随囊肿疝入腹股沟区。病理检查证实为LMs。术后6个月复查无复发。
|
图 2 淋巴管畸形患儿(病例2)影像学及手术资料 Fig.2 Imaging and surgical profiles of Case No.2 with lymphatic malformation 注 A:超声检查见液性暗区;B:超声见腹股沟区肠管回声;C:术中打开腹膜后可见囊肿 |
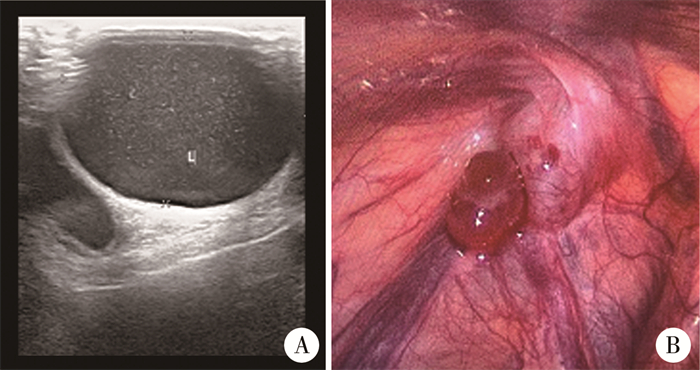
病例3,男,4岁,因“左侧鞘状突结扎术后3年,发现左侧阴囊肿大2年”入院。患儿3年前曾因左侧鞘膜积液在外院行左侧鞘状突结扎术。入院查体左侧腹股沟区及阴囊内触及肿物,质软,按压不能回纳入腹腔,透光试验阳性。彩超提示:左侧睾丸上方可见约31 mm×15 mm×24 mm液性暗区(图 3A)。术前诊断左侧鞘膜积液复发。术中腹腔镜下见左侧腹膜后囊肿,近内环口处,部分向下延伸至左侧腹股沟区及阴囊内,向上沿输精管方向延伸,左侧鞘状突已闭合。打开后腹膜,见囊肿膨出,腔镜下予以完整切除(图 3B),病理诊断为LMs。术后3个月复查无复发。
|
图 3 淋巴管畸形患儿(病例3)影像学及手术资料 Fig.3 Imaging and surgical profiles of Case No.3 with lymphatic malformation 注 A:超声检查见液性暗区;B:术中见腹膜后囊肿 |
讨论 LMs是由原始淋巴管胚胎发育缺陷导致的良性病变,由不同大小扩张的异常淋巴管组成,可分为微囊型、巨囊型以及混合型[5]。LMs的病因包括外伤、感染、手术损伤等,这些异常淋巴结构不能正常连接或引流到静脉系统,淋巴管之间引流不畅,导致淋巴液积聚,淋巴管囊性扩张形成肿块[6]。本组前2例患儿考虑为先天形成的病变;第3例患儿有同侧鞘状突手术史,曾因左侧鞘膜积液在外院行开放手术,术后1年出现术侧阴囊肿大,腹腔镜探查见左侧鞘状突已闭,考虑LMs可能因首次手术时损伤了周围淋巴管,而导致淋巴回流障碍,形成病变。
LMs可表现为生长缓慢的局灶性或弥漫性病变。儿童腹膜后LMs较为少见,通常无特殊的临床表现,容易误诊,当同时伴出血、感染时,才会因腹痛等临床症状而就诊[7]。本研究中3例临近腹股沟部的腹膜后LMs因为囊肿疝入腹股沟管(甚至疝入阴囊)而作为腹股沟区阴囊肿物被发现,无其他临床症状。超声、CT、MRI是常用的检查方法,由于超声无辐射、不需要镇静配合、性价比高,故作为首选。典型腹部LMs表现为单房或多房囊性肿块,可沿组织间隙生长,大多界限清晰(多个微囊存在时也可表现为界限不清)。在超声检查中,LMs常表现为多房囊性肿块,透性增强;可能出现低水平的内部浮动回声或液-液面表示内部的乳糜液、血性或脓性液体,提示囊内存在出血或感染,在纤维分隔和包膜内可以看到周围的血管[8]。但超声对病变范围、周围组织受侵情况的判断能力有限,MRI也是LMs较好的检查方法,病灶在T2加权像上通常表现为高信号[9]。CT有助于与其他囊性腹部病变鉴别,在LMs中很少出现大量钙化[10]。本组3例彩超均报告了液性暗区,只有病例2提示了内部条状分隔,为LMs常有的超声表现;因为经验不足,未考虑LMs可能,故未进一步行CT或MRI。
LMs常表现为无痛性囊性肿块,囊内液体较多时,透光试验阳性。通常缓慢增大,若有囊内出血时,肿块体积可迅速增大。腹股沟斜疝或鞘膜积液与LMs类似,可表现为阴囊及腹股沟区无痛性肿物。腹股沟斜疝未嵌顿时表现为可复性肿物,而鞘膜积液通常是不可复的。超声下腹股沟斜疝能见其疝内容物(如网膜或肠管),鞘膜积液则表现为无回声液性暗区,这与LMs的超声表现易混淆,尤其LMs为巨囊、单房囊肿时会增加鉴别难度。超声检查时若未向腹股沟区及腹腔探查,仅检查阴囊则易误诊。本组3例患儿的术前超声均检查到了阴囊及腹股沟管内肿物,但未向腹膜后延伸检查,造成术前诊断不准确。此外LMs还需与睾丸扭转、附睾炎等鉴别,但儿童阴囊急症通常表现为阴囊红肿、疼痛;还有发病率较低的儿童睾丸肿瘤,通常表现为阴囊内质地偏硬的实质性肿块。
腹部LMs发病率低,其中腹膜后LMs占比不足腹部LMs的1%[11]。临床上无明显症状及体征,容易误诊。本研究中2例患儿鞘状突未闭,腹膜后LMs生长位置靠近腹股沟管处,疝入了腹股沟管,才以腹股沟肿物被发现,其中1例同时合并腹股沟斜疝。另1例有同侧鞘状突手术史,LMs沿腹股沟管延伸至阴囊。腹膜后LMs囊内液体较多时透光试验阳性,易与鞘膜积液混淆。3例患儿术前均仅行超声检查,未能提供更多的影像学检查信息(如CT、MRI)辅助诊断,第2例患儿术前B超提示了内部的条状分隔,这正是LMs的超声表现,但由于医师经验不足,未能识别。而第3例患儿有同侧鞘状突手术史,是LMs发病原因之一,我们考虑LMs形成与首次手术相关,患儿术后出现同侧阴囊透光肿物,却误诊为鞘膜积液复发。
LMs多采用手术切除,但创伤大,复发率高。介入硬化治疗由于创伤小、操作简单、无瘢痕等特点,被越来越多地作为治疗首选(特别是对头颈部LMs);其主要是通过药物注入囊腔后刺激淋巴细胞产生非特异性炎症,使淋巴管闭塞硬化,从而缩小病变面积,常用博来霉素、平阳霉素、聚桂醇等。也有报道硬化剂对存在囊内出血的LMs有效果[12-13]。此外,针对LMs的治疗方案还包括激光治疗、口服药物以及外用药物等方法。手术是治疗腹膜后LMS的主要方式,手术需要尽量做到完整切除,远期预后良好,如果病灶未完全切除,需长期随访,关注复发情况[10]。目前腹腔镜手术逐渐成为首选[14-15]。
综上所述,腹膜后LMs发病率低,常无明显症状及体征,当临床上发现腹股沟区或阴囊肿物时,首先容易考虑鞘膜积液、腹股沟斜疝等常见疾病,但需警惕LMs,尤其是肿块较大,短期增长明显,既往有同侧手术史的患儿,需进一步检查。当超声提示分隔或向腹腔延伸,需考虑LMs可能,可进一步利用CT、MRI等协助评估。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 文献检索为黄彬,论文调查设计为黄彬、袁小建,数据收集分析为黄彬,论文结果撰写、讨论分析为黄彬、袁小建
| [1] |
Defnet AM, Bagrodia N, Hernandez SL, et al. Pediatric lymphatic malformations: evolving understanding and therapeutic options[J]. Pediatr Surg Int, 2016, 32(5): 425-433. DOI:10.1007/s00383-016-3867-4 |
| [2] |
Kennedy TL, Whitaker M, Pellitteri P, et al. Cystic hygroma/lymphangioma: a rational approach to management[J]. Laryngoscope, 2001, 111(11 Pt 1): 1929-1937. DOI:10.1097/00005537-200111000-00011 |
| [3] |
Amodeo I, Cavallaro G, Raffaeli G, et al. Abdominal cystic lymphangioma in a term newborn: a case report and update of new treatments[J]. Medicine (Baltimore), 2017, 96(8): e5984. DOI:10.1097/MD.0000000000005984 |
| [4] |
Bagrodia N, Defnet AM, Kandel JJ. Management of lymphatic malformations in children[J]. Curr Opin Pediatr, 2015, 27(3): 356-363. DOI:10.1097/MOP.0000000000000209 |
| [5] |
Wassef M, Blei F, Adams D, et al. Vascular anomalies classification: recommendations from the international society for the study of vascular anomalies[J]. Pediatrics, 2015, 136(1): e203-e214. DOI:10.1542/peds.2014-3673 |
| [6] |
Levine C. Primary disorders of the lymphatic vessels-a unified concept[J]. J Pediatr Surg, 1989, 24(3): 233-240. DOI:10.1016/s0022-3468(89)80001-6 |
| [7] |
Greene AK, Perlyn CA, Alomari AI. Management of lymphatic malformations[J]. Clin Plast Surg, 2011, 38(1): 75-82. DOI:10.1016/j.cps.2010.08.006 |
| [8] |
Mittal A, Anand R, Gauba R, et al. A step-by-step sonographic approach to vascular anomalies in the pediatric population: a pictorial essay[J]. Indian J Radiol Imaging, 2021, 31(1): 157-171. DOI:10.1055/s-0041-1729486 |
| [9] |
Crivelli L, Millischer AE, Sonigo P, et al. Contribution of magnetic resonance imaging to the prenatal diagnosis of common congenital vascular anomalies[J]. Pediatr Radiol, 2021, 51(9): 1626-1636. DOI:10.1007/s00247-021-05031-w |
| [10] |
Wohlgemuth WA, Brill R, Dendl LM, et al. Abdominal lymphatic malformations[J]. Radiologe, 2018, 58(S1): 29-33. DOI:10.1007/s00117-017-0337-5 |
| [11] |
Muramori K, Zaizen Y, Noguchi S. Abdominal lymphangioma in children: report of three cases[J]. Surg Today, 2009, 39(5): 414-417. DOI:10.1007/s00595-008-3854-z |
| [12] |
谢乂民, 宁金波, 姚明木, 等. 囊内出血对儿童大囊型淋巴管畸形硬化治疗效果的影响[J]. 临床小儿外科杂志, 2021, 20(1): 65-68. Xie YM, Ning JB, Yao MM, et al. Effect of hemorrhage of large cystic lymphatic malformation on therapeutic efficacy of sclerotherapy in children[J]. J Clin Ped Sur, 2021, 20(1): 65-68. DOI:10.12260/lcxewkzz.2021.01.013 |
| [13] |
林向上, 邓立才, 姚佳星, 等. 淋巴管畸形介入硬化治疗的效果分析[J]. 临床小儿外科杂志, 2020, 19(6): 518-522. Lin XS, Deng LC, Yao JX, et al. Clinical efficacies of interventional sclerotherapy for lymphatic malformation[J]. J Clin Ped Sur, 2020, 19(6): 518-522. DOI:10.3969/j.issn.1671-6353.2020.06.011 |
| [14] |
Sato T, Matsuo Y, Shiga K, et al. Laparoscopic resection of retroperitoneal lymphangioma around the pancreas: a case report and review of the literature[J]. J Med Case Rep, 2015, 9: 279. DOI:10.1186/s13256-015-0760-z |
| [15] |
Kogo H, Matsumoto S, Uchida E. Single-port laparoscopic-assisted resection for a large abdominal cystic lymphangioma: a case report[J]. Surg Case Rep, 2018, 4(1): 92. DOI:10.1186/s40792-018-0501-9 |
 2025, Vol. 24
2025, Vol. 24


