随着心脏外科手术技术的提高,法洛四联症(tetralogy of Fallot, TOF)患儿的存活率大大提高,但手术后远期并发症不容忽视。其中最常见并发症为肺动脉瓣反流(pulmonary regurgitation, PR),可导致右心功能不全,患儿活动耐力下降,心律失常,甚至发生猝死,严重影响TOF患儿远期生存质量。肺动脉瓣置换术(pulmonary valve replacement, PVR)是治疗PR的主要方法,包括体外循环下PVR、外科微创PVR(镶嵌手术)、经导管肺动脉瓣置换术(transcatheter pulmonary valve replacement, TPVR)等[1]。其中TPVR自2000年全球首例开展以来,已成为治疗右心室流出道(right ventricular outflow tract, RVOT)功能障碍的公认方法[2]。本文报道浙江大学医学院附属儿童医院开展的1例法洛四联症术后肺动脉瓣反流经导管肺动脉瓣置换术患儿的诊疗经验。
患儿,男,16岁4个月,因法洛四联症术后15年余、晕厥发作1次入院。患儿15年余前行体外循环下法洛四联症根治手术,术中Gortex补片修补室间隔缺损,疏通右室流出道,自体心包片跨瓣环补片重建右室流出道。术后定期随访,肺动脉瓣反流进展为重度。入院前2周打羽毛球后出现黑矇,随后晕厥,自行好转。体格检查:心率82次/分,血压115/72 mmHg (1 mmHg=0.133 kPa),肺动脉瓣区可闻及Ⅲ/Ⅵ级舒张期杂音。辅助检查:头颅CT未见明显异常。心电图提示Q-T间期延长(380 ms)。经胸超声心动图(图 1)显示肺动脉瓣中重度反流,右心增大。心脏大血管CT血管造影(图 2)提示右室增大,右室流出道扩张。心脏磁共振(Cardiovascular magnetic resonance, CMR) 提示肺动脉反流,右心室扩大,三尖瓣反流,右心房稍大。氨基末端脑利钠肽前体75.4 pg/mL。平板运动试验阴性。

|
图 1 法洛四联症术后肺动脉瓣反流患儿超声心动图显示肺动脉瓣环内径24.4 mm,右室FAC 32.2% Fig.1 Echocardiogram of the patient with postoperative pulmonary valve regurgitation following Tetralogy of Fallot repair, showing a pulmonary valve annulus diameter of 24.4 mm and right ventricular FAC of 32.2% |
|
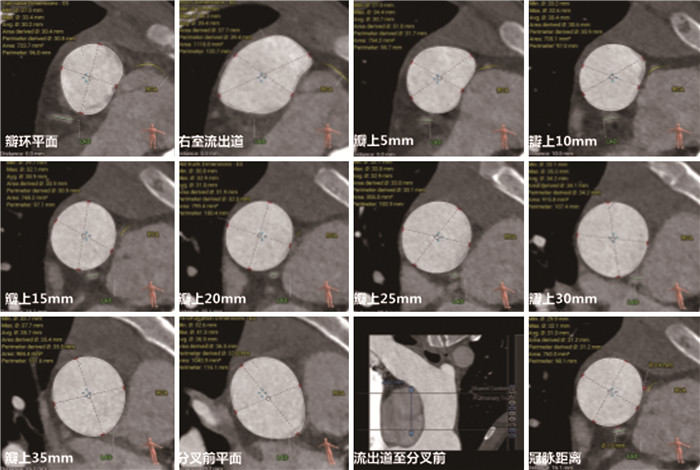
图 2 法洛四联症术后肺动脉瓣反流患儿术前心脏大血管CT血管造影各断层平面测量结果 Fig.2 Preoperative CT angiography measurements of the great vessels in the patient with postoperative pulmonary valve regurgitation following Tetralogy of Fallot repair, showing results across various imaging planes |
患儿超声心动图提示肺动脉瓣中重度反流,磁共振、CT血管造影等影像学检查提示解剖学适合行TPVR,术前心脏大血管CT血管造影三维重建及支架植入模拟未提示支架压迫冠状动脉可能(图 3),有运动后晕厥,且CMR测得右心室舒张末期容积指数≥150 mL/m2、右心室收缩末期容积指数≥80 mL/m2、右心室射血分数 < 45%,经专家团队评估后拟行经导管肺动脉瓣置换术。患儿及家属均知情同意,并签署知情同意书。

|
图 3 法洛四联症术后肺动脉瓣反流患儿术前心脏大血管CT血管造影三维重建及支架植入模拟 Fig.3 Preoperative 3D reconstruction of cardiac and great vessels CT angiography and stent implantation simulation in the patient with postoperative pulmonary valve regurgitation following Tetralogy of Fallot repair |
手术采取全身麻醉,术中先行经食道超声检查,并行左右心导管检查。取右股静脉、左股动静脉穿刺,经皮扩张后插入5F外鞘,行肺总动脉多角度造影,显示肺动脉瓣缺如、重度反流,测量肺动脉内径26 mm,肺总动脉分叉处至右心室流出道长度65 mm,升主动脉造影显示左、右冠状动脉显影,测量右心室压力29/7(15)mmHg,肺总动脉压力27/12(18)mmHg,右肺动脉压力33/8(18)mmHg,左肺动脉压力20/12(15)mmHg。送入10F输送鞘,将雅培测量球囊送至肺总动脉,测量肺动脉瓣环直径28 mm,同时冠状动脉造影未见冠状动脉压迫(图 4)。将超硬导丝放至左肺动脉远端,交换22F输送鞘将启明PA P32 — 25自膨瓣膜循导引导丝送至相关位置,逐步释放瓣膜并造影确认瓣膜位置,瓣膜中段主肺动脉贴壁良好稳固,花冠成形完整,左、右肺动脉血流通畅,瓣膜无明显反流(图 5、图 6)。术后予口服阿司匹林抗血小板治疗。术后第1、3天复查超声心动图提示肺动脉带瓣支架位置固定,未见明显瓣膜反流,右心室缩小,术后第4天出院。出院后1、3、6个月复查超声心动图,提示肺动脉血流通畅,瓣膜处无赘生物,无明显反流,右心室明显缩小、收缩功能较前提升。
|
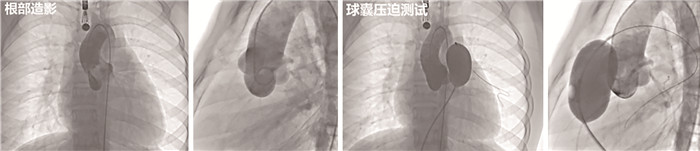
图 4 法洛四联症术后肺动脉瓣反流患儿术中数字减影血管造影根部造影及球囊压迫测试 Fig.4 Intraoperative DSA root angiography and balloon occlusion test in the patient with postoperative pulmonary valve regurgitation following Tetralogy of Fallot repair |
|
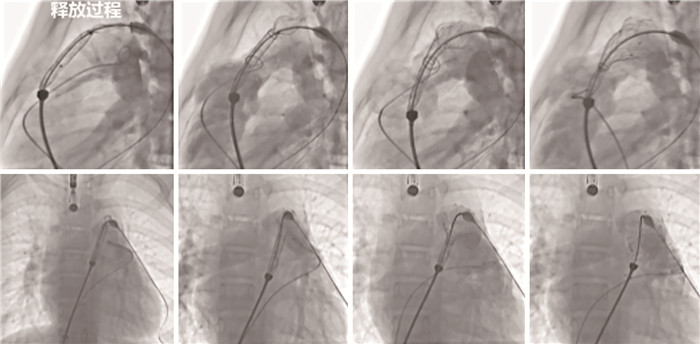
图 5 法洛四联症术后肺动脉瓣反流患儿术中人工肺动脉瓣释放过程 Fig.5 Intraoperative deployment of an artificial pulmonary valve in the patient with postoperative pulmonary valve regurgitation following Tetralogy of Fallot repair |
|
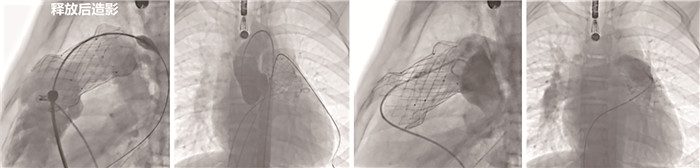
图 6 法洛四联症术后肺动脉瓣反流患儿肺动脉瓣释放完成后主动脉及肺动脉造影 Fig.6 Aortic and pulmonary angiography following the deployment of an artificial pulmonary valve in the patient with postoperative pulmonary valve regurgitation after Tetralogy of Fallot repair |
TOF在婴儿期即可施行一期根治手术,主要包括重建RVOT、修补室间隔缺损等。国内多采用跨瓣补片扩大术重建右室流出道,约48%的患儿术后立即出现明显肺动脉瓣反流(pulmonary regurgitation, PR),约85%的患儿在手术后2年出现明显PR,虽然大多数PR显著的患儿可能多年没有症状,但仍然面临右心室进行性扩张和右心功能下降、心律失常或猝死的风险。研究证实TOF术后接受PVR可显著改善右心室功能,并具有更好的远期预后[3-4]。体外循环下肺动脉瓣置换术(surgical pulmonary valve replacement, SPVR)虽然是治疗PR的有效手段,但创伤大、恢复慢、术后并发症发生率较高。Park等[5]对行SPVR的293例先天性心脏病(congenital heart disease, CHD)患儿进行回顾性研究,患儿平均年龄14.9岁,中位随访时间10.5年,多因素分析显示,尽管SPVR具有良好的长期疗效,但对于曾经接受过多次心内直视手术的患儿,尤其是接受过3次以上心内直视手术者而言,病死率显著高于心内直视手术少于3次者,这可能与反复胸骨切开和心内直视手术增加了手术难度和体外循环时间有关。TOF术后PVR的管理策略是尽可能推迟手术干预,以最大程度减少手术次数。然而,推迟手术干预,右心功能障碍势必有不可逆转的风险。在进展的右心功能障碍和尽量减少患者终生手术次数之间取得平衡,促进了微创瓣膜置换术的发展。与SPVR相比,TPVR中远期疗效相当,并发症发生率显著降低,有望减少接受生物瓣膜PVR的患者一生中的手术次数[6]。随着更多生物瓣膜的开发,TPVR已逐渐成为治疗PR的主要方式。本例患儿法洛四联症术后15年,术前评估显示肺动脉瓣中重度反流,合并临床症状,符合TPVR的手术适应证[7]。
TOF根治手术往往在1岁以内实施,也就意味着很多TOF患儿在尚未成年时就可能出现了PR,为避免不可逆右心功能障碍的发生,可以在儿童期进行TPVR。Pagourelias等[8]的研究纳入20例TOF术后患儿,年龄(13.9±9.2)岁,均为重度PR,其中15%的患儿有症状,85%的患儿无症状,但伴有右室扩张。与RVOT重建术后超过7年的患者相比较,RVOT重建术后7年内患者在进行TPVR后,右心室重建更好,更接近正常右室大小和功能。Borik等[9]纳入了包括23例16岁以下患儿在内的51例病例,随访5年结果显示TPVR术后心功能均显著改善,认为在16岁以下行TPVR会获得更好的右室重建,从而获得更好的右室功能恢复。Martin等[10]回顾性分析了4个中心43例成功实施TPVR的患者,平均年龄5.8岁(3.3~10岁),平均体重17.7 kg(13.5~19.8 kg),多为法洛四联症,患儿随访均存活,且瓣膜功能良好。Jin等[11]报道了中国6家医院使用Venus P瓣膜完成TPVR的术后5年随访结果,存活率96.4%,并获得了持续的血流动力血改善。
根据亚洲专家共识,TPVR的适应证主要包括:合并ROVT梗阻的先心病外科矫治术后并发中重度或重度PR,伴或不伴ROVT梗阻;解剖学上适合TPVR;有RVOTD相关临床症状[7]。若患者没有明显临床症状,则需要满足以下条件之一:右室扩大,心脏磁共振测得右室舒张末期容积指数≥150 mL/m2和(或)右室收缩末期容积指数≥80 mL/m2;合并中度及以上功能性三尖瓣关闭不全;严重右心室功能下降或半年内随访进行性下降;合并严重ROVT梗阻:右心室收缩压>80 mmHg和(或)右心室收缩压≥2/3体循环收缩压;有猝死高危因素等。在儿童TPVR的适应证中,优化干预时机至关重要,早期干预与更好的长期预后相关,并能避免出现RVOT/PA过度增大,增加TPVR难度;另一方面,延迟干预最大限度提高了TPVR的可行性,并延迟了可能的再干预。El-Saiedi等[12]报道了5例出生时就接受射频穿孔和球囊扩张术的室间隔完整型肺动脉闭锁,最小年龄7岁,最低体重20 kg,均成功实施了TPVR,扩大了TPVR的年龄和体重限制:只要肺动脉瓣环大小超过20 mm,就可以尝试进行干预,如果等待这些患儿达到30 kg的最低干预体重,则可能发展到肺动脉瘤样扩张,肺动脉超过现有肺动脉瓣膜,且使右室处于进行性扩张和功能障碍的风险之中,因而直接影响预后。
我们需要关注儿童TPVR的一些重要并发症,TPVR在儿童患者中存在挑战,介入治疗血管通路,尤其是股静脉可能太细而不能安全通过输送系统。Martin等[10]回顾性分析了4个中心43例体重 < 20 kg儿童施行TPVR的经验,19例经颈静脉瓣膜置换术患儿未出现与颈静脉通路相关的并发症,24例经股静脉入路者出现4例血管不良事件,股静脉通路并发症发生在最小的患者中,其中2例体重 < 14 kg。手术前使用超声或血管造影来评估静脉通路是否合适值得研究,TPVR后这些血管的通畅对于未来的再次瓣膜植入有重要意义。关于儿童TPVR术后亚临床血管通路并发症的问题值得进一步研究。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 邱芸香、张庆负责文献检索,徐玮泽负责论文设计,李昳负责数据收集,邱芸香、解春红、高立超负责研究结果分析与讨论,邱芸香、张庆、蒋炜负责论文撰写;邱芸香、舒强、徐玮泽负责全文知识性内容的审读与修正
| [1] |
李建强, 苏俊武. 经皮介入肺动脉瓣置入术的研究进展[J]. 中华胸心血管外科杂志, 2016, 32(10): 634-637. Li JQ, Su JW. Advances in percutaneous pulmonary valve implantation[J]. Chin J Thorac Cardiovasc Surg, 2016, 32(10): 634-637. DOI:10.3760/cma.j.issn.1001-4497.2016.08.015 |
| [2] |
Bonhoeffer P, Boudjemline Y, Saliba Z, et al. Percutaneous replacement of pulmonary valve in a right-ventricle to pulmonary-artery prosthetic conduit with valve dysfunction[J]. Lancet, 2000, 356(9239): 1403-1405. DOI:10.1016/S0140-6736(00)02844-0 |
| [3] |
Bokma JP, Geva T, Sleeper LA, et al. Improved outcomes after pulmonary valve replacement in repaired tetralogy of Fallot[J]. J Am Coll Cardiol, 2023, 81(21): 2075-2085. DOI:10.1016/j.jacc.2023.02.052 |
| [4] |
Van den Eynde J, Sá MPBO, Vervoort D, et al. Pulmonary valve replacement in tetralogy of Fallot: an updated meta-analysis[J]. Ann Thorac Surg, 2022, 113(3): 1036-1046. DOI:10.1016/j.athoracsur.2020.11.040 |
| [5] |
Park WY, Kim GB, Lee SY, et al. Long-term outcome and risk factor analysis of surgical pulmonary valve replacement in congenital heart disease[J]. Congenit Heart Dis, 2022, 17(3): 335-350. DOI:10.32604/chd.2022.018666 |
| [6] |
Megaly M, Han K, Sedhom R, et al. Outcomes of percutaneous and surgical pulmonary valve implantation[J]. Cardiovasc Revasc Med, 2021, 32: 27-32. DOI:10.1016/j.carrev.2020.12.035 |
| [7] |
中国医师协会心血管内科医师分会结构性心脏病学组, 亚洲心脏病学会, 国家放射与治疗临床医学研究中心. 经导管肺动脉瓣置换术亚洲专家共识[J]. 中国介入心脏病学杂志, 2023, 31(6): 404-412. Group of Structural Cardiology, Branch of Cardiovascular Physicians, Chinese Medical Doctor Association, Asian Society of Cardiology, National Clinical Research Center for Interventional Medicine. Asian Expert Consensus on Transcatheter Pulmonary Valve Replacement[J]. Chin J Intervent Cardiol, 2023, 31(6): 404-412. DOI:10.3969/j.issn.1004-8812.2023.06.002 |
| [8] |
Pagourelias ED, Daraban AM, Mada RO, et al. Right ventricular remodelling after transcatheter pulmonary valve implantation[J]. Catheter Cardiovasc Interv, 2017, 90(3): 407-417. DOI:10.1002/ccd.26966 |
| [9] |
Borik S, Crean A, Horlick E, et al. Percutaneous pulmonary valve implantation: 5 years of follow-up: does age influence outcomes?[J]. Circ Cardiovasc Interv, 2015, 8(2): e001745. DOI:10.1161/CIRCINTERVENTIONS.114.001745 |
| [10] |
Martin MH, Shahanavaz S, Peng LF, et al. Percutaneous transcatheter pulmonary valve replacement in children weighing less than 20 kg[J]. Catheter Cardiovasc Interv, 2018, 91(3): 485-494. DOI:10.1002/ccd.27432 |
| [11] |
Jin QC, Long YL, Zhang GJ, et al. Five-year follow-up after percutaneous pulmonary valve implantation using the Venus P-valve system for patients with pulmonary regurgitation and an enlarged native right ventricular outflow tract[J]. Catheter Cardiovasc Interv, 2024, 103(2): 359-366. DOI:10.1002/ccd.30916 |
| [12] |
El-Saiedi SA, Attia WA, Hanna BM, et al. Staged percutaneous management of pulmonary atresia and intact interventricular septum: stretching the limits[J]. J Interv Cardiol, 2023, 2023: 9709227. DOI:10.1155/2023/9709227 |
 2025, Vol. 24
2025, Vol. 24


