1992年,de Ville首次应用Rex手术治疗肝外门静脉梗阻(extra-hepatic portal venous obstruction, EHPVO),至今已经30年。尽管Rex手术已经是一种成熟的技术,但能开展该技术的中心数量依然有限。笔者通过总结自身开展Rex手术的临床经验和国内外的应用情况,详细分析Rex手术的技术难点和应用进展,为已经实施Rex手术、初步应用该技术和准备开展该技术的医师、科室或医院提供一定的借鉴。
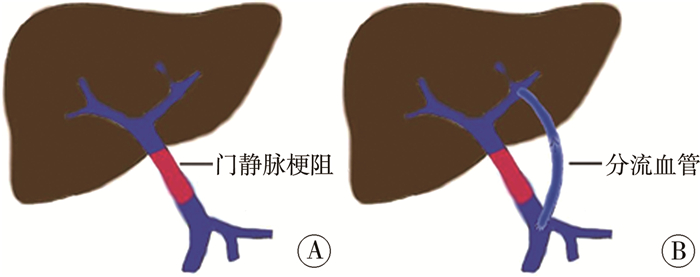
一、Rex手术原理和适应证 (一) 治疗原理Rex手术是指通过移植或转位分流血管的方式,将门静脉系统血液分流入Rex隐窝内的门静脉左支,实现门静脉血液分流进入肝脏的目的。该手术将分流血管绕过肝外门静脉梗阻部位,重建了门静脉入肝通道,既实现恢复入肝血流、避免肝功能不全的作用,又达到降低门静脉高压、预防上消化道出血的目的[1-2]。由此可见,Rex手术的技术原理是重建门静脉入肝血流,具体入肝的部位是Rex隐窝内的门静脉左支(图 1)。
|
图 1 Rex手术方法示意图 Fig.1 Rex shunt operative modes 注 A:门静脉梗阻;B:Rex手术重建门静脉入肝血流 |
Rex手术因其重建门静脉入肝血流的作用,常用于治疗EHPVO引发的肝外门静脉高压,亦可用于肝移植中的门静脉重建。其实施条件包括:①肝脏正常,无肝纤维、肝硬化;②门静脉左支通畅;③合适的搭桥血管(直径大于5 mm,长度可实现无张力吻合)[1-2]。术前评估病人满足该实施条件,是明确Rex手术可行性的关键。
1. 肝脏的条件 肝脏正常是实施Rex手术的必要前提条件。很多肝硬化性门静脉高压患者也可能存在门静脉海绵样变,但不适宜接受Rex手术治疗。肝硬化引发门脉高压的机制包括:①肝内增生的纤维束和再生的肝细胞结节挤压肝小叶内的肝窦,使其变窄或闭塞,导致门脉血流受阻;②肝内假小叶压迫小叶下静脉,使肝窦内血液流出受阻,进而影响门静脉血流入肝窦;③肝小叶间汇管区的肝动脉小分支与门静脉小分支之间的动静脉交通支开放,使压力高的肝动脉血流入门静脉内[3]。由此可见,肝硬化者若接受Rex手术,门静脉血流经Rex分流血管进入肝内时会不可避免遭受肝内的阻力,导致分流血管内的门静脉血液较难注入肝内。在此情况下,Rex手术后肝外门静脉系统依然面临门静脉高压状态。除此之外,Rex分流血管内的门静脉血液因不能通畅进入肝内,不可避免地会导致血液瘀滞在分流血管内,进而引发分流血管血栓形成风险增加,最终导致手术失败。因此,为了保障Rex手术的分流效果和实现降低门静脉压力的作用,Rex手术实施的前提之一是术中肝活检显示肝脏正常,无肝纤维化和肝硬化。
2. 血管的条件 门静脉左支通畅和合适的搭桥血管是实施Rex手术的另一条件。如果门静脉左支不通畅,Rex手术后肝外门静脉血液便无法通过Rex分流血管顺利进入肝内,以实现重建门静脉入肝血流的目的。尽管超声和CT都能判断门静脉的结构,但门静脉造影和手术解剖才是最终判断门静脉左支通畅状态的方法[4]。超声和CT常需要血管内有足够的血流才能显像或显影,达到判断血管通畅状态的目的;而门静脉海绵样变常导致门静脉的入肝血流减少,引发门静脉肝内分支血流减少,导致超声和CT探测困难,甚至不显像。但这并不代表门静脉左支不存在,为此需要门静脉造影或手术探查进一步明确。
综上所述,为了成功实施Rex手术,做好术前评估工作是必不可少的,包括:①术前介入下门静脉血管造影或术中门静脉血管造影明确肝外门静脉梗阻和门静脉左支通畅;②术中行肝脏活检明确肝脏正常,无肝纤维化或肝硬化。这两点是明确Rex手术能否实施的关键。
二、国内外Rex手术的应用情况 (一) 应用数量1. 文献报道的应用数量 笔者在PubMed中,以“extra-hepatic”, “portal vein obstruction”, “Rex shunt ”, “meso-Rex shunt”, “Rex bypass”为关键词,且将年龄限制在0~18岁,检索有关Rex手术应用的报道并对其进行分析,发现全世界有10个国家的13个医疗中心曾报道采用Rex手术治疗EHPVO,截至2019年总应用例数达到444例,其中以中国报道的例数最多,达到197例[5-19]。
2. 预计的应用数量 2018年1月,美国芝加哥Ann & Robert H. Lurie儿童医院在官网报道,其已经开展Rex手术200余例;但其最近的文献报道仅70例Rex手术(1997—2010年)[11]。2022年7月,首都儿科研究所在官网报道,其已经开展Rex手术300余例,但其最近的文献报道仅99例(2008—2017年)[20]。由此推断,实际开展Rex手术的国家和医疗中心不止于上述10个国家的13个医疗中心,实际开展的Rex手术数量也不低于444例,世界上实际开展的Rex手术数量估计千余例。根据Rex手术30年的应用历史来推测,全球每年平均开展Rex手术的数量保守估计为30余例。
(二) 应用趋势通过对历年Rex手术报道例数的分析发现,Rex手术的应用例数呈现逐年递增的趋势。该现象可能与Rex手术治疗EHPVO的疗效逐渐被明确,并被公认为治疗儿童EHPVO的首选术式有关,由此导致既往采用其他手术方法(如门体分流术、脾切除术或肝移植术)治疗的EHPVO患儿选择了Rex手术治疗。
(三) 世界三大治疗中心从文献报道的应用数量上,中国北京的首都儿科研究所、美国芝加哥的Ann & Robert H. Lurie儿童医院和中国广州的广州市妇女儿童医疗中心是目前报道应用Rex手术最多的三家医疗中心,而其他欧洲国家应用的例数稀少。
(四) 应用困境从世界各医疗中心应用Rex手术的数量可见,Rex手术治疗儿童EHPVO与小儿外科其他常见病(包括胆总管囊肿、胆道闭锁、肛门闭锁和先天性巨结肠)相比,仍是一种应用较少的手术方法。制约Rex手术开展的最主要因素是病人数量较少,如果没有一定的病人实施手术,医师技术将很难提高。并且,因病例数量较少也难以实施高质量的临床研究,进而获得有价值的临床发现。
三、小儿外科实施Rex手术的局限性 (一) 技术方面血管重建技术是医师开展Rex手术的核心技术,亦是Rex手术异于小儿外科一些常见病多发病手术(包括巨结肠根治术、胆总管囊肿根治术、肛门成形术和Kasai手术等)的关键技术。基于血管重建技术的要求,导致国外实施Rex手术的医师常为器官移植外科医师和开展Rex手术的医疗机构常为器官移植外科机构。然而,在中国小儿外科界,拥有器官移植技术的儿外科医师凤毛麟角。缺乏血管重建技术的现状成为制约中国儿外科医师实施Rex手术的重要障碍之一。
绝大多数儿外科医师实施的手术主要由组织分离(包括肠管、胆管、腹部肿物和血管等)和大管腔脏器重建(吻合肠管、胆管等)组成,极少进行血管重建(该技术一般为血管外科和移植外科的常用技术)。该特点造成儿外科医师缺乏或不善于实施血管重建技术,进而影响了Rex手术的实施。以上现实情况导致手术经验丰富的儿外科医师,在实施Rex手术前,亦应具备熟练的血管重建技术。若不具备该技术,强行实施Rex手术将造成严重后果,甚至手术失败不可避免,为病人造成严重创伤。因此,虽然很多国内儿外科中心开展了该技术,但实施之初并非一帆风顺,甚至有些病人术后便出现分流血管血栓形成。出现该现象的主要原因与儿外科医师的血管重建技术储备不足有关。由此可见,技术不足是制约儿外科医师实施Rex手术的重要方面。
(二) 流行病学和治疗观念方面EHPVO发病率低、病人数量少,进而限制了医师技术的提高,是制约Rex手术实施的另一个重要因素。尽管当前Rex手术被公认为是治疗儿童EHPVO的首选手术,但仍有部分应实施Rex手术的EHPVO患者接受了其他手术方式(包括门体分流术、脾切除术和肝移植手术等),这可能也是限制Rex手术实施的原因之一。为此,通过提高Rex手术在大众中的认可度,可能有利于扭转该局面。
四、Rex手术的技术难点及克服方法Rex手术的关键技术是分离血管和吻合血管。
(一) 血管的分离操作分离血管即将移植血管(包括颈内静脉、肠系膜下静脉、脾静脉、回肠静脉、空肠静脉等)与周围组织相分离。手术关键是保障移植血管不损伤和周围组织少出血甚至不出血。为此,需要操作过程精确、减少损伤。由于肉眼能观察的细微程度有限,为了提高操作精确性,手术参加者均应配备2.5~5倍的手术放大镜(头戴式)以放大手术视野,这点在实施血管吻合时至关重要。在分离血管过程中,为了减少血管损伤,采用的分离方法因人而异,包括采用组织剪和血管钳钝性分离和采用电刀低功率切凝结合进行血管的分离。若术者在开展其他手术时习惯于采用电刀分离,可选择电刀,但谨记分离时电刀应远离移植血管,不应对其造成热损伤,并且功率一定要低,达到简单切凝的程度即可。据笔者在美国和国内肝移植中心的学习经验,发现采用钝性分离是最佳的血管分离方法,常采用血管钳和组织剪配合使用进行分离,这样可以减少对血管损伤。
(二) 血管的吻合操作吻合血管包括将移植血管与肝外门静脉血管(包括肠系膜上静脉和门静脉主干)相吻合和将移植血管与肝内门静脉左支相吻合。肝外的门静脉与移植血管的吻合相对较简单,只要配上放大镜将视野放大,与实施肝管空肠吻合或肠吻合没有太大区别,关键是实施吻合前需对肝外门静脉血管做好阻断,避免吻合过程中出血。然而,移植血管与门静脉左支的吻合是Rex手术最主要和最困难的技术。这是由于门静脉左支在Rex隐窝内,而Rex隐窝又在肝脏裂隙里,位置较深,暴露困难,因而导致吻合困难。
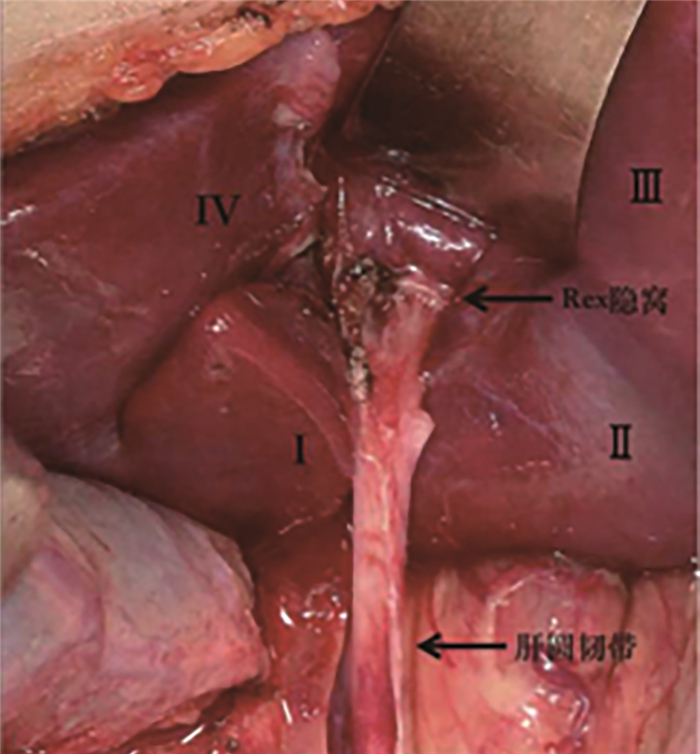
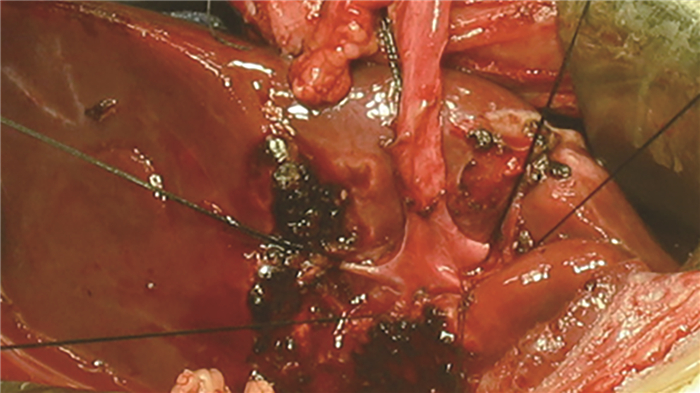
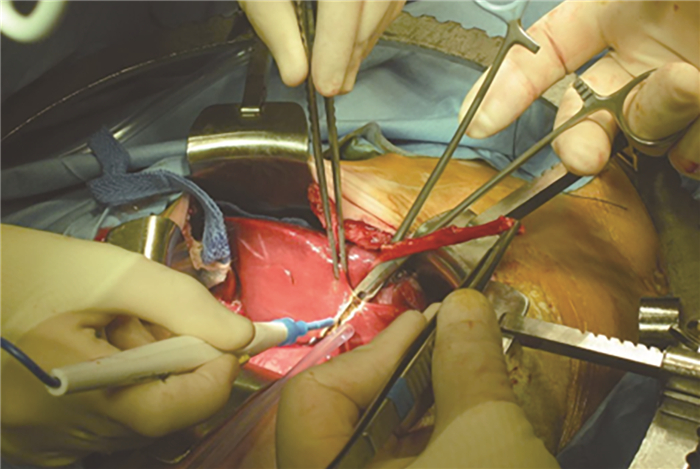
1. 暴露Rex隐窝的方法 为了克服移植血管与门静脉左支吻合的困难,充分暴露Rex隐窝和门静脉左支是成功的关键。方法如下:首先,劈开肝桥,将Rex隐窝充分暴露。肝桥是位于肝脏Ⅰ段和Ⅱ段之间的肝脏组织,其与肝脏前缘形成一个陷窝,肝圆韧带根部穿行其中,便形成了Rex隐窝(图 2)。肝桥的发育因人而异,有时十分肥厚,劈离时会引发出血。此时应将电刀功率调大,边切开边止血,直至将肝桥彻底劈开,将脐静脉根部彻底暴露。有时肝桥呈分离状态,便简化了劈离肝桥的操作,更容易暴露Rex隐窝。其次,应对脐静脉根部进行充分的解剖。劈离肝桥后,肝圆韧带根部便暴露了出来。在此处,脐静脉汇入门静脉左支,一般能在脐静脉根部分出3~5个肝内分支,应将其一一分离,用细线阻断牵引(图 3)。该操作不仅有助于暴露门静脉左支,还可以达到阻断血管、避免出血的作用。最后,助手需要密切配合。如果助手不能充分拉开Rex隐窝,该手术实施很困难。而且拉钩用力不能过猛,过猛则将肝脏拉入肋弓下;而用力过小又不能将Rex隐窝拉开,这对助手是一个非常大的考验。在美国芝加哥移植中心实施Rex手术时,常选择倒T型切口,将肝脏搬出,用辅助拉钩而非助手暴露该部位(图 4)。采用倒T型切口和辅助拉钩的优点是省去了一个助手,暴露充分;但缺点是手术伤口巨大,术中需反复调整拉钩,手术时间较长。另外,Rex隐窝内门静脉左支的直径是固定的,该处的血管吻合不像胆管吻合,可以将肝门处胆管扩大,以增加吻合口直径。唯一有效的办法是将Rex隐窝完全暴露,充分将脐静脉根部与门静脉左支连接处剪开,才能将门静脉左支完全显露,以利于吻合口的扩大。另外,吻合口直径取决于门静脉左支的直径,单纯选择粗大的移植血管不能扩大吻合口直径。
|
图 2 Rex隐窝的位置 Fig.2 Location of Rex recess 注 Rex隐窝位于肝脏Ⅲ段、Ⅳ段和肝桥之间;肝桥为Ⅰ段和Ⅱ段相连接的肝组织 |
|
图 3 肝外门静脉梗阻患者实施Rex手术图片 Fig.3 Rex shunt in patients with extrahepatic portal venous obstruction 注 Rex术中分离Rex隐窝内的脐静脉分支,暴露门静脉左支用于血管吻合 |
|
图 4 肝外门静脉梗阻患者实施Rex手术图片 Fig.4 Rex shunt in patients with extrahepatic portal venous obstruction 注 采用倒T切口和辅助拉钩实施Rex手术,用电刀劈开肝桥以暴露Rex隐窝 |
2.吻合血管的方法 吻合技术是实施Rex手术的另一个挑战。克服该挑战的方法如下:①在血管吻合前应将移植血管进行一定的修剪。剔除血管吻合口周围多余的脂肪组织,使吻合口边缘整齐,更容易暴露吻合口,避免吻合时将多余组织缝进吻合口。②在实施吻合前,应将脐静脉根部门静脉左支起始部和移植血管用阻断钳阻断,避免出血影响手术视野。但阻断时间不能过长,长时间阻断门静脉左支将导致吻合口损伤甚至血栓形成。因此,应经常对吻合口进行充分的肝素灌洗。③为确保吻合成功,吻合血管时应采用外翻缝合的方法使两侧内膜对合,若外膜缘进入吻合口内,极易导致血栓形成,引发分流失败。在缝合时,可采用后壁连续缝合,前壁间断缝合的办法,不仅提高了缝合效率,还能避免因缝合问题导致的吻合口狭窄。尤其在缝合前壁时,切忌因进针较深导致前壁与后壁缝合。为此,应将血管前壁稍提起,在可视范围内实施缝合,避免盲区出现。
(三) 移植血管的选择移植血管的选择不是Rex手术的技术难点。但为了提高Rex手术成功率,应满足Rex手术移植血管的条件,其包括[21]:①血管直径:大于5 mm(指血管的全程直径至少5 mm);②血管长度:无张力吻合;③血管条件:自然状态下,血管较直,分叉少(主要是针对胃冠状静脉),最好为无分支者。关于颈内静脉是否优于其他血管的争议,在国内学术界时有提起。但迄今未见任何一篇文献报道颈内静脉的疗效优于其他移植血管。出现该现象的原因可能是:在实施Rex手术时,术者必然要选择最佳的移植血管进行手术,这就导致所选择的移植血管应是条件最好的血管才能实施Rex手术,反之Rex手术必然失败。因此,只要血管条件满足上述标准,均是合适的移植血管。但颈内静脉因具有较粗的直径及合适的长度,是理想的移植血管之一。
(四) 门静脉右支分流的实施条件肝内门静脉左支通畅与否是决定能否行Rex手术的关键,但约13.6%的EHPVO患儿因门静脉左支闭塞或发育不良不能行Rex手术,而不得不选择行Warren手术等其他手术治疗[11]。李龙等[22]提出采用门静脉主干-门静脉右支分流的方法成功治疗5例该类患儿,表明门静脉右支是可以作为Rex手术入肝部位的。但由于门静脉右支位置较深,暴露和吻合困难,成为该术式实施的主要限制。
五、术后管理 (一) 围手术期的监护及处置围手术期监护的重点是术后出血和分流血管的通畅情况。
1. 术后出血 术后出血一般源于手术分离区域的出血和血管吻合口的出血,而后者是术后出血的主要原因。若经输血治疗后,生命体征仍不稳定,血红蛋白持续降低,腹腔穿刺或腹腔引流管出现不凝的鲜血,应紧急手术探查进行止血。
2. 分流血管通畅性 术后应采用腹部超声和增强CT明确分流血管的通畅情况,若术后超声和CT显示分流血管不通或堵塞,应再次手术进行血管重新吻合或选择其他的搭桥血管。抗凝治疗能有效的提高分流血管通畅率[23]。因此,为了避免分流血管血栓形成引发堵塞,应术后常规采用肝素抗凝治疗。
(二) 分流失败后的再次手术对于分流失败的治疗包括介入治疗(包括溶栓、球囊扩张和放置支架)和分流手术。
1. 介入治疗 对于分流血管血栓形成者,可先行采用介入下溶栓和血管内血栓移除的方法治疗,但对于治疗失败者应进一步采用手术治疗[2]。Guérin等[13]报道9例Rex术后分流血管狭窄或血栓形成患者,其中6例再次手术治疗(3例接受门体分流术,3例接受再次Rex手术治疗),3例接受非手术治疗(2例血管内血栓移除,1例抗凝治疗)。
2. 分流手术 Warren手术和Rex手术是治疗Rex术后复发的主要手术方法。Superina等[24]报道3例Rex术后复发患者中2例成功接受Warren手术治疗。Zhang等[25]通过对再次手术治疗Rex术后复发者的疗效对比发现,再次Rex手术的失败率为62.5%(5/8),Warren手术的失败率为20%(1/5)。由此可见,在再次手术治疗方面,Warren手术的疗效优于Rex手术。但由于Rex手术具有重建门静脉入肝血流的功能,仍应将Rex手术作为首选的手术治疗方案,对于多次Rex手术失败,不能满足行Rex手术的条件时才应选择Warren手术治疗[2]。
利益冲突 所有作者声明不存在利益冲突
| [1] |
张金山, 李龙. Rex手术治疗小儿肝外门静脉高压的应用进展[J]. 中华小儿外科杂志, 2017, 38(8): 636-640. Zhang JS, Li L. Recent advances of Rex shunt for extra-hepatic portal venous obstruction[J]. Chin J Pediatr Surg, 2017, 38(8): 636-640. DOI:10.3760/cma.j.issn.0253-3006.2017.08.018 |
| [2] |
Zhang JS, Li L. Rex shunt for extra-hepatic portal venous obstruction in children[J]. Children (Basel), 2022, 9(2): 297. DOI:10.3390/children9020297 |
| [3] |
张金山, 李龙. 小儿肝硬化门脉高压症的研究新进展[J]. 中华小儿外科杂志, 2010, 31(9): 702-705. Zhang JS, Li L. New advances in the study of portal hypertension in children with liver cirrhosis[J]. Chin J Pediatr Surg, 2010, 31(9): 702-705. DOI:10.3760/cma.j.issn.0253-3006.2010.09.014 |
| [4] |
Superina R, Shneider B, Emre S, et al. Surgical guidelines for the management of extra-hepatic portal vein obstruction[J]. Pediatr Transplant, 2006, 10(8): 908-913. DOI:10.1111/j.1399-3046.2006.00598.x |
| [5] |
de Ville de Goyet J, Alberti D, Clapuyt P, et al. Direct bypassing of extrahepatic portal venous obstruction in children: a new technique for combined hepatic portal revascularization and treatment of extrahepatic portal hypertension[J]. J Pediatr Surg, 1998, 33(4): 597-601. DOI:10.1016/s0022-3468(98)90324-4 |
| [6] |
Brichard M, Iesari S, Lerut J, et al. Meso-Rex bypass for the management of extrahepatic portal vein obstruction in adults (with video)[J]. Hepatobiliary Pancreat Dis Int, 2022, 21(1): 25-32. DOI:10.1016/j.hbpd.2021.08.003 |
| [7] |
de Ville de Goyet J, Alberti D, Falchetti D, et al. Treatment of extrahepatic portal hypertension in children by mesenteric-to-left portal vein bypass: a new physiological procedure[J]. Eur J Surg, 1999, 165(8): 777-781. DOI:10.1080/11024159950189573 |
| [8] |
Sharif K, McKiernan P, de Ville de Goyet J. Mesoportal bypass for extrahepatic portal vein obstruction in children: close to a cure for most![J]. J Pediatr Surg, 2010, 45(1): 272-276. DOI:10.1016/j.jpedsurg.2009.08.019 |
| [9] |
Alberti D, Colusso M, Cheli M, et al. Results of a stepwise approach to extrahepatic portal vein obstruction in children[J]. J Pediatr Gastroenterol Nutr, 2013, 57(5): 619-626. DOI:10.1097/MPG.0b013e31829fad46 |
| [10] |
Luoto T, Pakarinen M, Mattila I, et al. Mesoportal bypass using a constructed saphenous vein graft for extrahepatic portal vein obstruction-technique, feasibility, and outcomes[J]. J Pediatr Surg, 2012, 47(4): 688-693. DOI:10.1016/j.jpedsurg.2011.10.065 |
| [11] |
Lautz TB, Keys LA, Melvin JC, et al. Advantages of the meso-Rex bypass compared with portosystemic shunts in the management of extrahepatic portal vein obstruction in children[J]. J Am Coll Surg, 2013, 216(1): 83-89. DOI:10.1016/j.jamcollsurg.2012.09.013 |
| [12] |
Cortez AR, Kassam AF, Jenkins TM, et al. The role of surgical shunts in the treatment of pediatric portal hypertension[J]. Surgery, 2019, 166(5): 907-913. DOI:10.1016/j.surg.2019.05.009 |
| [13] |
Guérin F, Bidault V, Gonzales E, et al. Meso-Rex bypass for extrahepatic portal vein obstruction in children[J]. Br J Surg, 2013, 100(12): 1606-1613. DOI:10.1002/bjs.9287 |
| [14] |
Krebs-Schmitt D, Briem-Richter A, Grabhorn E, et al. Effectiveness of Rex shunt in children with portal hypertension following liver transplantation or with primary portal hypertension[J]. Pediatr Transplant, 2009, 13(5): 540-544. DOI:10.1111/j.1399-3046.2008.01109.x |
| [15] |
Ha TY, Kim KM, Ko GY, et al. Variant meso-Rex bypass with transposition of abdominal autogenous vein for the management of idiopathic extrahepatic portal vein obstruction: a retrospective observational study[J]. BMC Surg, 2015, 15: 116. DOI:10.1186/s12893-015-0101-6 |
| [16] |
Ateş O, Hakgüder G, Olguner M, et al. Mesenterico left portal bypass for variceal bleeding owing to extrahepatic portal hypertension caused by portal vein thrombosis[J]. J Pediatr Surg, 2006, 41(7): 1259-1263. DOI:10.1016/j.jpedsurg.2006.03.043 |
| [17] |
Zhang JS, Li L, Cheng W. The optimal procedure of modified Rex shunt for the treatment of extrahepatic portal hypertension in children[J]. J Vasc Surg Venous Lymphat Disord, 2017, 5(6): 805-809. DOI:10.1016/j.jvsv.2017.02.011 |
| [18] |
Ruan ZM, Wu M, Shao CC, et al. Effects of Rex-bypass shunt on the cavernous transformation of the portal vein in children: evaluation by the color Doppler ultrasonography[J]. Insights Imaging, 2020, 11(1): 4. DOI:10.1186/s13244-019-0815-6 |
| [19] |
Wu HY, Zhou N, Lu LW, et al. Value of preoperative computed tomography for meso-Rex bypass in children with extrahepatic portal vein obstruction[J]. Insights Imaging, 2021, 12(1): 109. DOI:10.1186/s13244-021-01057-8 |
| [20] |
Zhang JS, Li L. Imaging features and clinical relevance of portal venous systems shown by extrahepatic portal angiography in children with extrahepatic portal venous obstruction[J]. J Vasc Surg Venous Lymphat Disord, 2020, 8(5): 756-761. DOI:10.1016/j.jvsv.2019.11.016 |
| [21] |
张金山, 李龙. 改良Rex手术治疗小儿肝外门静脉高压的疗效及最佳方法探讨[J]. 中华小儿外科杂志, 2017, 38(8): 585-590. Zhang JS, Li L. Optimal procedure of modified Rex shunt for extrahepatic portal hypertension in children[J]. Chin J Pediatr Surg, 2017, 38(8): 585-590. DOI:10.3760/cma.j.issn.0253-3006.2017.08.007 |
| [22] |
Li L, Zhang JS, Chen Z, et al. Portal-to-right portal vein bypass for extrahepatic portal vein obstruction[J]. J Pediatr Surg, 2018, 53(7): 1403-1407. DOI:10.1016/j.jpedsurg.2017.10.059 |
| [23] |
张金山, 李龙. 肝素联合波立维抗凝方案在Rex手术治疗小儿肝外门静脉梗阻中的应用及疗效分析[J]. 临床小儿外科杂志, 2022, 21(2): 146-150. DOI: 10.3760/cma.j.cn101785-202102027-009. Zhang JS, Li L. Anticoagulant therapy of heparin plus plavix after Rex shunt for children with extrahepatic portal venous obstruction[J]. DOI: 10.3760/cma.j.cn101785-202102027-009. |
| [24] |
Superina R, Bambini DA, Lokar J, et al. Correction of extrahepatic portal vein thrombosis by the mesenteric to left portal vein bypass[J]. Ann Surg, 2006, 243(4): 515-521. DOI:10.1097/01.sla.0000205827.73706.97 |
| [25] |
Zhang JS, Li L, Cheng W. Surgical treatment for rebleeding caused by bypass failure after Rex shunt: re-Rex shunt or Warren shunt?[J]. Pediatr Surg Int, 2018, 34(5): 521-527. DOI:10.1007/s00383-018-4246-0 |
 2025, Vol. 24
2025, Vol. 24

