儿童胰腺实性假乳头状瘤是临床上较为少见的低度恶性或交界性肿瘤,占胰腺原发肿瘤的0.13% ~2.70%,治疗以手术切除为主,预后良好[1]。儿童因腹腔空间狭小,同时因胰腺的特殊解剖位置,与周围脏器和脾血管紧邻,导致胰腺手术较为复杂,术后并发症较多,国内外儿童腹腔镜胰腺肿瘤手术文献报道较少。机器人手术系统灵活的机械臂和放大的三维视野在胰腺肿瘤手术中能一定程度上克服上述困难。本研究旨在初步探讨机器人在儿童胰腺实性假乳头状瘤手术中应用的安全性与临床应用价值。
资料与方法 一、一般资料本研究为回顾性研究,收集2020年4月至2023年7月在浙江大学医学院附属儿童医院收治的5例胰腺实性假乳头状瘤患儿临床资料,包括患儿性别、年龄、体重、病变位置、影像学检查、术前及术后实验室检查结果、手术时间、术中出血量、引流管放置时间、术中术后并发症、住院天数、术后病理诊断及住院费用。男1例、女4例,年龄6岁9个月至14岁9个月,中位年龄10岁11个月。体重21.5~45.0 kg(中位体重29.1 kg)。5例术前均因出现不同程度的腹痛、呕吐等症状就诊,患儿术前丙氨酸转氨酶(alanine aminotransferase, ALT)、天门冬氨酸转氨酶(aspartate aminotransferase, AST)均无异常,其中1例术前血淀粉酶(amylase, AMY)、脂肪酶(lipase, LPS)轻度升高。
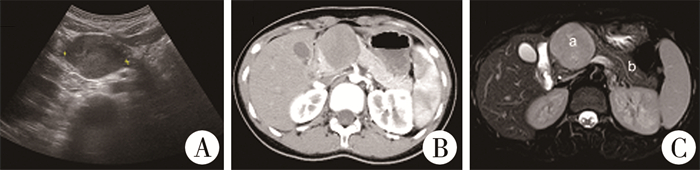
二、影像学检查患儿术前均行超声、全腹增强CT及MRI检查(图 1)。肿瘤位于胰头部2例,体尾部1例,尾部2例;肿瘤长径2.6~5.6 cm(中位长径为4.00 cm),均未发现周围组织侵犯及远处转移。
|
图 1 胰腺实性假乳头状瘤影像学检查图片 Fig.1 Images of pancreastic solid pseudopapilloma 注 A:胰头部低回声包块,边界清楚,形态欠规整,内部回声不均匀;B:胰头部类圆形占位,边界尚清,密度欠均匀, 增强见强化;C:胰头部稍长T1稍长T2信号肿块影(a),边界清晰,与胰管位置密切,胰管稍扩张(b) |
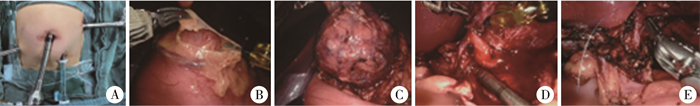
采用da Vince Xi机器人手术系统。以脐部纵切口为主视镜孔,操作孔分别置于脐两侧、病灶与脐连线的垂直线上,孔间距5~8 cm,在主视镜孔与机械臂操作孔中点后方3 cm布置辅助孔,分别置入马里兰钳、电凝钩或超声刀。打开小网膜囊,悬吊胃壁,显露胰腺,找到肿瘤位置,切开胰腺组织,沿肿瘤包膜游离肿瘤周围组织。由于胰腺实性假乳头状瘤质地较脆,多有坏死,分离时易造成肿瘤破裂,可贯穿肿瘤缝制牵引线以利于牵拉。较粗的血管用Hem-o-lock结扎后电凝离断。术中仔细辨别主胰管及脾动脉静脉,若胰管不慎损伤可用7 - 0可吸收线及时修补。胰腺创面予以电灼或电喷止血,肿瘤剜除后常规于肿瘤剥离创面放置负压引流管(图 2)。
|
图 2 机器人辅助胰头部胰腺实性假乳头状瘤剜除术图片 Fig.2 Robot-assisted enucleation of solid pseudopapilloma of pancreatic head 注 A:手术布孔,脐部为主视镜孔,操作孔分别布置在右下腹及左上腹,辅助孔布置在左下腹;B:打开胃结肠韧带,暴露瘤体;C:沿肿瘤包膜分离;D:瘤体与主胰管紧临;E:7-0可吸收线间断缝合修补胰管破裂 |
术后予广谱抗生素抗感染治疗,动态评估患儿营养状况,有营养不良风险患儿给予静脉高营养支持。同时予生长抑素抑制胰酶分泌及奥美拉唑抑制胃酸分泌等治疗。关注患儿胃肠减压引流量及腹腔引流量,维持患儿液体出入量平衡。术后2~3 d动态检测患儿血常规、超敏C反应蛋白及生化五类等(尤其是感染指标、血淀粉酶及脂肪酶变化)。术后4~5 d逐渐恢复饮食后复查胰腺B超及腹水B超。
五、统计学处理采用SPSS 22.0进行统计分析。非正态分布的计量资料采用M(Q1, Q3)描述,手术前后比较采用配对秩和检验,P<0.05为差异有统计学意义。
结果5例均顺利完成机器人辅助胰腺实性假乳头状瘤剜除术,无一例中转开腹手术,见表 1。其中1例肿瘤与胰管关系密切,术中剥离肿瘤后发现胰管损伤行胰管修补,术后禁食1周后复查淀粉酶及胰腺超声无明显异常后逐渐恢复饮食。其余患儿术后禁食4天后进食,饮食恢复后复查胰腺B超及淀粉酶无明显异常,引流液少于20 mL后拔除腹腔引流,引流管留置时间5~10天。5例患儿手术前后白细胞计数、超敏C反应蛋白、ALT、AST、AMY、LPS差异无统计学意义(P>0.05),见表 2。术后病理均为胰腺实性假乳头状瘤(图 3)。患儿术后均顺利康复出院,无一例围术期并发症及术后死亡。随访2个月至3年,无一例出现肿瘤复发、胰漏、胰管狭窄等并发症。平均住院费用89 699.83(70 474.94~110 899.07)元。
| 表 1 5例行达芬奇机器人胰腺手术患儿临床资料 Table 1 Profiles of 5 children undergoing Da Vinci robotic pancreatic surgery |
|
|
| 表 2 5例行机器人胰腺手术患儿术前、术后实验室检查指标对比[M(Q1,Q3)] Table 2 Comparison of perioperative laboratory parameters in 5 children undergoing robotic pancreatic surgery[M(Q1, Q3)] |
|
|
|
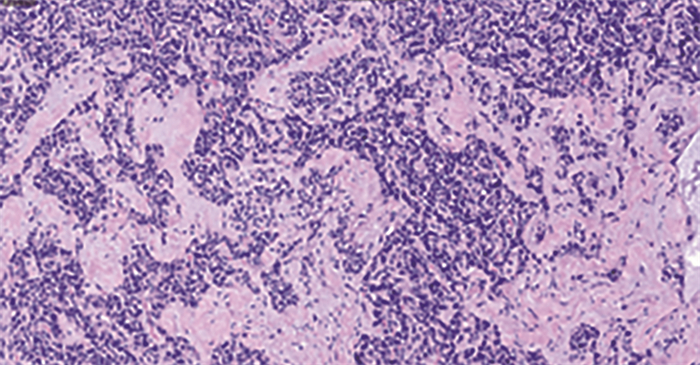
图 3 胰腺实性假乳头状瘤患儿的病理图片(HE染色, 200×) Fig.3 Pathological images of children with solid pancreastic pseudopapillom (HE, 200×) 注 镜下见肿瘤细胞呈乳头状排列,部分成片分布 |
儿童胰腺肿瘤临床上较少见,以实性假乳头状瘤为主,女性群体发病率较高,生长缓慢,具有低度恶性潜能,多伴有坏死出血,常位于胰腺尾部[2-3]。儿童胰腺微创技术的发展较为缓慢,胰腺实质切除后的内、外分泌不足等术后并发症的发生率也较高。
胰腺实性假乳头状瘤的手术方式需根据肿瘤位置、肿瘤大小及与临近器官血管的关系决定,常见手术包括保留脾脏的胰腺体尾部切除术、胰十二指肠根治术及胰腺肿瘤剜除术等。近年来儿童腹腔镜下保留脾脏胰尾切除术治疗胰腺实性假乳头状瘤已在多家机构开展,随着微创技术的发展与临床经验的不断积累,机器人辅助胰十二指肠根治术或保留幽门的胰十二指肠根治术也可达到类似于开腹手术的临床效果[4-8]。机器人辅助胰腺肿瘤剜除术也有个案报道[9]。本组5例胰腺实性假乳头状瘤患儿均行机器人辅助胰腺肿瘤剜除术,术中暴露瘤体后用超声刀紧贴肿瘤真、假包膜分离,考虑胰腺实性假乳头状瘤低度恶性的特点,在保留肿瘤完整的前提下可将少量周围胰腺实质同时剥离。术中注意辨别主胰管、胆总管、脾血管,尤其是肿瘤位于胰头部时,十二指肠乳头、胃十二指肠动脉和胰十二指肠上、下血管等重要结构都需要仔细辨别,在明确血管位置后再沿肿瘤包膜分离可减少损伤周围结构的机会。荧光导航成像技术也可用于术中胆管及血管显影[4, 10]。胰腺肿瘤剜除术的重点和难点在于主胰管的识别与保护,邻近胰管时剥离肿瘤可采用钝性分离,影像学检查(如磁共振胰胆管造影)在术前评估瘤体与主胰管间距离中有着重要作用。机器人胰腺手术的国际共识认为,手术时间、肿瘤和主胰管的距离是胰腺肿瘤剜除术后胰漏的高危因素,建议肿瘤与主胰管的安全距离≥2 mm[11]。随着微创技术的不断发展,其手术指征已逐渐放开。本组1例胰头部实性假乳头状瘤患儿术前磁共振胰胆管造影发现瘤体紧贴主胰管,术中行瘤体剜除时不慎切开主胰管,予反复冲洗暴露胰管缺损,发现胰管裂口 < 1 cm,直接予7 - 0可吸收线间断缝合修补,同时予周围胰腺组织缝合覆盖,并放置引流管充分引流。术后延长禁食时间至1周,配合生长抑素应用,动态复查淀粉酶及脂肪酶,待淀粉酶正常后予逐渐恢复饮食。术后恢复良好,随访无肿瘤复发、胰漏、胰腺炎以及内分泌相关并发症。儿童主胰管细小且管壁较成人薄弱,机器人三维立体高清视野、7个自由度的器械活动让其在处理胰管损伤时更具优势,同时降低了胰漏的发生率。
机器人胰腺手术于2002年首次在文献中被报道,具有高清三维立体成像视野及在精细操作(如血管分离)上更具优势[12]。Jin等[13]对比开腹手术与机器人辅助腹腔镜技术用于胰腺肿瘤剜除术的疗效,发现两者在胰腺炎、胰漏等围术期并发症发生率上无明显差异,而机器人手术组的术中出血量、手术时间及术后康复时间均明显少于开腹手术组,在保脾成功率上也更占优势[14]。也有研究提出机器人在胰腺恶性肿瘤治疗中发挥巨大作用,保留幽门的胰十二指肠切除术降低了胃排空延迟、倾倒综合征等术后并发症的发生率,改善了儿童的长期生活质量[15]。王乐等[8]实现了在腹腔镜下较难开展的术中淋巴结清扫和肿瘤扩大切除,尽可能保留正常胰腺实质和保护胰腺功能, 降低了儿童因胰腺实质大部分缺损、功能不全导致的生长发育影响,同时术中出血少,手术时间短,恶性肿瘤复发率更低,延长了总生存期[16]。本组患儿术后住院时间相对较长,这与本院机器人胰腺肿瘤剜除术处于起步阶段相关,但患儿在住院期间早已恢复饮食,术后淀粉酶、脂肪酶等指标恢复较快。达芬奇手术在胰腺疾病治疗中的优势明显,但也存在一定的缺陷,如开机费用昂贵、手术花费不能纳入医保等,这往往是患儿监护人选择手术方式的主要决定因素;同时机器人系统缺乏触觉反馈系统,一定程度上依赖于视觉辅助以及手术经验的积累。
总体而言,机器人手术系统在胰腺外科中的应用扩展了腹腔镜技术的适应证,机器人辅助腹腔镜手术用于儿童胰腺实性假乳头状瘤安全、可行, 其解剖层次显示清晰, 操作精细, 术后恢复更具优势,是胰腺实性假乳头状瘤微创手术的理想选择,具有广泛的应用前景。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 宣笑笑、陈青江负责研究的设计、实施和起草文稿;宣笑笑、张书豪、蔡多特、高志刚、罗文娟、陈肯、胡迪进行数据收集与分析;宣笑笑、陈青江、高志刚负责数据质量监管,并对文章知识性内容进行审阅
| [1] |
Papavramidis T, Papavramidis S. Solid pseudopapillary tumors of the pancreas: review of 718 patients reported in English literature[J]. J Am Coll Surg, 2005, 200(6): 965-972. DOI:10.1016/j.jamcollsurg.2005.02.011 |
| [2] |
Brecht IB, Schneider DT, Klöppel G, et al. Malignant pancreatic tumors in children and young adults: evaluation of 228 patients identified through the Surveillance, Epidemiology, and End Result (SEER) database[J]. Klin Padiatr, 2011, 223(6): 341-345. DOI:10.1055/s-0031-1287836 |
| [3] |
Picado O, Ferrantella A, Zabalo C, et al. Treatment patterns and outcomes for pancreatic tumors in children: an analysis of the National Cancer Database[J]. Pediatr Surg Int, 2020, 36(3): 357-363. DOI:10.1007/s00383-020-04617-z |
| [4] |
徐晓钢, 曾纪晓, 刘斐, 等. 腹腔镜吲哚菁绿荧光导航下精准保留脾血管胰尾切除治疗儿童实性假乳头状瘤[J]. 中华腔镜外科杂志(电子版), 2022, 15(4): 245-248. Xu XG, Zeng JX, Liu F, et al. Laparoscopic splenic vessel-preserving distal pancreatectomy accurately for solid pseudopapillary neoplasm in children with indocyanine green fluorescent navigation technique[J]. Chin J Laparosc Surg (Electron Ed), 2022, 15(4): 245-248. DOI:10.3877/cma.j.issn.1674-6899.2022.04.012 |
| [5] |
尹强, 彭宇明, 谢惟心, 等. 小儿腹腔镜保脾胰腺体尾部切除手术七例[J]. 临床小儿外科杂志, 2021, 20(7): 627-630. Yin Q, Peng YM, Xie WX, et al. Experience of laparoscopic resection of spleen-preserving pancreatic body and tail in children[J]. Journal of Clinical Pediatric Surgery, 2021, 20(7): 627-630. DOI:10.12260/lcxewkzz.2021.07.006 |
| [6] |
Hagendoorn J, Nota CLMA, Borel Rinkes IHM, et al. Robotic pancreatoduodenectomy for a solid pseudopapillary tumor in a ten-year-old child[J]. Surg Oncol, 2018, 27(4): 635-636. DOI:10.1016/j.suronc.2018.07.013 |
| [7] |
Chinnusamy P, Dey S, Chittawadagi B, et al. First robotic pylorus preserving pancreaticoduodenectomy for Frantz's tumour in an adolescent girl[J]. J Minim Access Surg, 2018, 14(4): 349-353. DOI:10.4103/jmas.JMAS_272_17 |
| [8] |
王乐, 沈丽萍. 运用达芬奇手术机器人辅助系统治疗小儿胰腺肿瘤[J]. 临床小儿外科杂志, 2018, 17(5): 363-366. Wang L, Shen LP. Treatment of pediatric pancreatic tumors by robotic surgical system[J]. J Clin Ped Sur, 2018, 17(5): 363-366. DOI:10.3969/j.issn.1671-6353.2018.05.011 |
| [9] |
朱真闯, 闫学强, 段栩飞, 等. 达芬奇机器人手术系统在儿童胰腺疾病治疗中的应用4例并文献复习[J]. 中华小儿外科杂志, 2022, 43(11): 981-987. Zhu ZC, Yan XQ, Duan XF, et al. Application of Da Vinci robotic surgical system for pediatric pancreatic diseases: a report of 4 cases with a literature review[J]. Chin J Pediatr Surg, 2022, 43(11): 981-987. DOI:10.3760/cma.j.cn421158-20220711-00486 |
| [10] |
游欣雨, 程东辉, 蒋佶朋, 等. "单孔+1"荧光腹腔镜下保留十二指肠胰头切除术在胰头良性肿瘤中的应用[J]. 中国普通外科杂志, 2023, 32(9): 1287-1295. You XY, Cheng DH, Jiang JP, et al. Application of" single-incision plus one port"laparoscopic duodenum-preserving pancreatic head resection for benign pancreatic head tumors[J]. Chin J Gen Surg, 2023, 32(9): 1287-1295. DOI:10.7659/j.issn.1005-6947.2023.09.001 |
| [11] |
Liu R, Wakabayashi G, Palanivelu C, et al. International consensus statement on robotic pancreatic surgery[J]. Hepatobiliary Surg Nutr, 2019, 8(4): 345-360. DOI:10.21037/hbsn.2019.07.08 |
| [12] |
Melvin WS, Needleman BJ, Krause KR, et al. Robotic resection of pancreatic neuroendocrine tumor[J]. J Laparoendosc Adv Surg Tech A, 2003, 13(1): 33-36. DOI:10.1089/109264203321235449 |
| [13] |
Jin JB, Qin K, Li H, et al. Robotic enucleation for benign or borderline tumours of the pancreas: a retrospective analysis and comparison from a high-volume centre in Asia[J]. World J Surg, 2016, 40(12): 3009-3020. DOI:10.1007/s00268-016-3655-2 |
| [14] |
Chen S, Zhan Q, Chen JZ, et al. Robotic approach improves spleen-preserving rate and shortens postoperative hospital stay of laparoscopic distal pancreatectomy: a matched cohort study[J]. Surg Endosc, 2015, 29(12): 3507-3518. DOI:10.1007/s00464-015-4101-5 |
| [15] |
曾纪晓, 徐晓钢, 刘斐, 等. 全球首例机器人辅助保留幽门的胰十二指肠切除术治疗儿童壶腹部横纹肌肉瘤(附视频)[J]. 机器人外科学杂志, 2023, 4(6): 606-611. Zeng JX, Xu XG, Liu F, et al. Robot-assisted pylorus-preserving pancreaticoduodenectomy for rhabdomyosarcoma in hepatopancreatic ampulla in children: a first-ever case report (with video)[J]. Chin J Robot Surg, 2023, 4(6): 606-611. DOI:10.12180/j.issn.2096-7721.2023.06.017 |
| [16] |
McCarron FN, Vrochides D, Martinie JB. Current progress in robotic hepatobiliary and pancreatic surgery at a high-volume center[J]. Ann Gastroenterol Surg, 2023, 7(6): 863-870. DOI:10.1002/ags3.12737 |
 2024, Vol. 23
2024, Vol. 23


