引起儿童胃流出道梗阻(gastric outlet obstruction, GOO)的常见良性病变包括先天性肥厚性幽门狭窄(congenital hypertrophic pyloric stenosis, CHPS)、消化性溃疡、消化道重复畸形、异位胰腺等。根据病变性质及GOO严重程度的不同,可采用不同的治疗方法,内科治疗包括胃镜下球囊扩张术(endoscopic balloon dilation, EBD)或内镜下黏膜剥离术(endoscopic submucosal dissection, ESD)。外科治疗包括Heineke-Mikulicz幽门成形术(Heineke-Mikulicz pyloroplasty,HMP)、Billroth Ⅰ式胃大部切除术(毕Ⅰ术)、Billroth Ⅱ式胃大部切除术(毕Ⅱ术)、胃空肠Roux-en-Y术等;后3种术式出现胆汁反流性胃炎、吻合口溃疡、吻合口狭窄等并发症的可能性较大,严重影响患儿长期生存质量及生长发育。国内针对HMP在儿童胃流出道梗阻良性病变中的应用研究较少,本研究旨在初步探讨HMP在儿童胃流出道梗阻良性病变中的应用指征及手术疗效。
资料与方法 一、一般资料回顾性收集2015年8月至2021年1月广州医科大学附属广州市妇女儿童医疗中心胃肠外科收治的11例因良性胃流出道梗阻病变接受HMP患儿的临床资料,其中男5例,女6例,年龄1.3个月至11岁9个月,平均年龄4岁7个月。11例均以非胆汁性呕吐入院,症状持续时间6 d至21个月。其他症状包括腹痛7例,腹胀4例,黑便1例,恶心反酸1例。行HMP前诊断:4例为消化性溃疡致幽门或十二指肠球部狭窄,3例为胃壁肿物,2例为嗜酸性粒细胞性胃肠炎(eosinophilic gastroenteritis, EGE)致幽门狭窄,1例为CHPS幽门环肌切开术后幽门再梗阻,1例为化学性损伤致胃窦远端狭窄。本研究已通过广州医科大学附属广州市妇女儿童医疗中心伦理委员会批准[(2022)第178A01号],家属均知情同意并签署知情同意书。
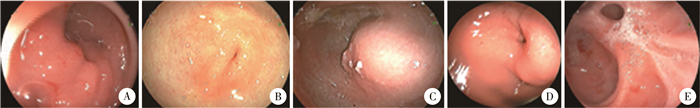
二、术前检查11例患儿术前均行上消化道造影(upper gastrointestinal contrast, UGC), 均提示不同程度GOO表现。10例行胃镜检查(图 1),其中4例见十二指肠球部溃疡并球部或幽门部狭窄;这4例患儿中有3例同时行EBD;2例分别予扩张1次、4次后复查UGC及胃镜,提示狭窄无明显改善;1例在扩张过程中合并十二指肠穿孔,行急诊腹腔镜探查手术。3例胃壁肿物患儿胃窦局部隆起;2例EGE于镜下见幽门狭窄,胃黏膜活检均可见嗜酸性粒细胞(eosinophil, EOS)大量浸润;1例误吞氯化锌溶液的患儿镜下证实胃窦部多发瘢痕形成,胃镜无法通过。4例行腹部电子计算机断层扫描(computed tomography, CT),提示胃窦部病变,其中3例为胃壁肿物,2例病变累及幽门。2例行超声检查,1例为CHPS,1例EGE患儿胃扩张并幽门肥厚。
|
图 1 胃流出道梗阻良性病变患儿术前胃镜检查图片 Fig.1 Findings of preoperative gastroscopy in GOO children caused by benign lesions 注 A:溃疡性十二指肠球部狭窄;B: 溃疡性幽门狭窄;C: 胃窦部肿物;D:EGE导致的胃窦及幽门狭窄;E:化学性损伤后胃窦部远端瘢痕狭窄 |
术前1 d使用奥美拉唑保护胃黏膜,术前30 min常规应用第二代头孢类抗生素预防感染,所有患儿术前经鼻置入胃管。
(二) 手术方法手术要点:充分显露胃窦至十二指肠球部,必要时松解十二指肠降部,为横形缝合创造条件,能量器械只在幽门部切开位置进行操作,避免对迷走神经的损伤。对于幽门部肿物予完整切除并送术中冰冻病理检查,如肿物为恶性或性质难以判断且边界不清,则行胃部分切除术。腹腔镜下行Kocher法分离牵拉十二指肠时动作轻柔,以保护肾脏及其血管,同时避免损伤胰腺头部。部分病例纵行切开处胃壁组织水肿增厚明显,出血较多,腹腔镜下止血及暴露困难,可用电钩切开、建立突破点后再用超声刀切开。对于胃壁组织水肿增厚明显者行幽门成形时,先使用鱼骨线连续缝合全层,后使用可吸收线间断缝合浆肌层。
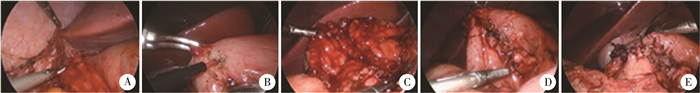
手术步骤:①腹腔镜手术组:采用3孔法,经脐开放置入5 mm腹腔镜穿刺器Trocar作为观察孔,常规建立气腹后于右侧腋前线肋缘下1 cm及平脐下2 cm处分别置入5 mm Trocar作为操作孔。分离胃窦及十二指肠球部周围组织,充分暴露后观察胃流出道病变情况,通过Kocher法继续游离十二指肠球部及降部。以Mayo静脉(幽门前静脉)为中心由胃窦远端至十二指肠近端沿前壁纵轴全层切开,切口长4~5 cm,一般不超过7 cm;切口过短有缝合后瘢痕收缩导致狭窄的风险; 切口过长不但不能增加管径,而且可能增加横向缝合的困难[1-2]。如病变为肿物,则在肿物靠近前壁处切开,完整切除肿物,切除组织送冰冻病理检查,明确病变性质。在两侧切缘中点各悬吊一针使切缘横形对齐,并为缝合提供所需张力,可用4-0多股可吸收线间断缝合切口,如果局部张力较高,可选用4-0鱼骨线连续缝合,缝合后自胃管注入空气以确认吻合口无渗漏且通过良好。最后用大网膜覆盖吻合口(图 2)。②开放手术组:于右肋下1 cm靠近中线做长约5 cm的横切口入腹,其余手术步骤同腹腔镜手术组。
|
图 2 1例十二指肠球部溃疡并狭窄患儿腹腔镜下Heineke-Mikulicz幽门成形术流程图 Fig.2 Laparoscopic HMP in a child with peptic duodenal bulb stenosis 注 A:分离暴露十二指肠;B:自胃窦部切开;C:完成纵行切开;D:两侧切口中点各悬吊一针;E: 幽门成形后 |
患儿术后进食流质饮食前使用奥美拉唑保护胃黏膜;术后48 h内应用第二代头孢类抗生素预防感染,复查血常规、C反应蛋白等以决定是否继续使用抗生素;待饮水无呕吐后拔除胃管;对于术后超过3 d仍不能实施肠内营养的患儿给予静脉营养支持。
四、统计学处理采用SPSS 25.0进行统计学分析。分别于行HMP前1 d和术后1年,空腹抽取患儿静脉血,检测血清白蛋白、前白蛋白,测量身高(长)、体质量并计算身体质量指数(body mass index, BMI)。服从正态分布的计量资料以x±s表示,不服从正态分布的计量资料以M(Q1, Q3)表示;采用配对t检验与配对秩和检验比较患儿手术前后上述指标;P<0.05为差异有统计学意义。
结果 一、手术情况及相关病理结果11例患儿共行14次手术,8例一期行HMP,其中6例为开放手术、2例为腹腔镜手术;3例行2次手术,其中2例分别为CHPS、EGE患儿,第1次手术均行腹腔镜幽门环肌切开术,术后症状持续不缓解,分别于术后第10天、第60天行第2次手术,均为开放HMP。1例为化学性损伤患儿,第1次手术为腹腔镜辅助空肠造瘘术+空肠营养管置入术,术后3个月行开放HMP。本组患儿HMP手术时间(162±92)min,术中出血量(10±3)mL。3例胃壁肿物术后病理结果显示2例为异位胰腺,1例为胃重复畸形。2例EGE术后病理结果均提示肌层水肿肥厚,EOS大量浸润。1例化学性损伤患儿术后胃壁病理提示肌纤维增生,排列紊乱,局灶坏死。
二、出院时情况所有患儿行HMP后住院时间(12±4)d,出院时伤口甲级愈合,复查感染指标基本正常,经口进食无呕吐、腹痛、腹胀等。化学性损伤患儿带空肠造瘘营养管出院,术后45 d于门诊拔除造瘘营养管,该患儿出院时需半流质饮食,其余患儿出院时饮食恢复至正常。
三、随访结果随访通过门诊复诊、电话和互联网完成。出院后随访(38±23)个月,11例术后3个月均能正常进食。无一例出现倾倒综合征、吻合口狭窄、吻合口溃疡、黏连性肠梗阻、胃食管反流等并发症。1例术后6个月内偶有胃潴留,经保守治疗后好转;2例饱食后偶有轻微腹痛。所有患儿术后6个月内完成1次UGC或胃镜检查,10例造影剂通过良好,1例球部溃疡并狭窄患儿胃镜提示幽门及十二指肠无狭窄,十二指肠腔变形但黏膜光滑。所有患儿随访至术后1年时身高、身体质量发育正常,BMI、血清白蛋白、前白蛋白均较前显著升高(P<0.05)。见表 1、表 2。
| 表 1 11例胃流出道梗阻良性病变患儿临床资料 Table 1 Clinical data of 11 GOO children |
|
|
| 表 2 11例胃流出道梗阻良性病变患儿HMP术前与术后1年营养指标的比较 Table 2 Comparison of nutritional parameters at preoperation and 1 year post-HMP in 11 GOO children |
|
|
HMP最早用于治疗由消化性溃疡导致的GOO,以后逐渐扩展到对克罗恩病、放射性肠炎、幽门部膜状闭锁、CHPS等所致GOO的治疗中,其适应证如下:①非占位性病变,如先天性幽门前瓣膜、CHPS、化学性损伤引起的幽门管狭窄、消化性溃疡引起的球部或幽门管狭窄、EGE引起的幽门梗阻等;②占位性病变,如累及幽门管的胃重复畸形、异位胰腺、错构瘤、成熟型畸胎瘤等。
一、先天性肥厚性幽门狭窄CHPS是导致婴幼儿GOO的最主要原因,手术是唯一有效的治疗方法,腹腔镜幽门环肌切开术以其疗效确切、损伤小、术后恢复快等优点,成为主流手术方式,且术后复发率低,术后超过1周的呕吐不缓解多由肌层切开不充分导致[3]。再手术患儿多于幽门部其他位置再次行幽门环肌切开术。Simeonov等[4]曾报道4例再手术CHPS,2次手术间隔时间3~12 d,平均7.5 d,其中3例再行幽门环肌切开术,1例行HMP,术后均恢复良好。本组1例CHPS患儿第1次手术后呕吐无缓解,复查超声及UGC提示幽门梗阻,于术后第10 d行开放幽门环肌切开术,术中见幽门处瘢痕增生明显,遂行HMP,术后呕吐症状明显缓解。HMP是较早用于CHPS的术式,后因其较复杂而逐渐被幽门环肌切开术取代[5]。但对于不适宜再行幽门环肌切开的患儿,HMP仍可以相对较小的损伤取得较好的效果。
二、幽门部肿物儿童幽门部良性占位少见,临床上较常遇到胃重复畸形、异位胰腺、胃息肉、成熟型畸胎瘤等,大部分患儿因频繁呕吐、腹痛就诊[6]。根据占位体积及与幽门管的关系可采用不同手术方式,包括单纯肿物切除、胃十二指肠吻合术等[7]。Doya等[8]曾应用HMP治疗1例幽门部重复畸形,随访4年未出现并发症。对凸向胃腔的胃重复畸形、异位胰腺可行ESD,并取得良好效果[9-10]。但相较于胃内其他部位的肿物,因幽门部病变行ESD者肿块切除率和完整切除率均较低,由于幽门管空间有限,对于涉及幽门管甚至十二指肠球部的病变,其完整切除率更低,复发风险也更高[11]。本组3例胃壁占位性病变,2例术前CT检查提示累及幽门管,行肿物切除+HMP,术后恢复良好。
三、溃疡性胃流出道梗阻儿童消化性溃疡多由幽门螺旋杆菌(helicobacter pylori, HP) 感染或长期应用非甾体类消炎药导致,且临床症状不典型,较少有机会接受正规治疗,大部分因并发症就诊[12]。本组4例患儿中HP筛查2例阳性。对于儿童消化性溃疡是除CHPS外引起GOO最常见的病因,目前对于早期出现的GOO可采用EBD治疗,据报道约65%的患儿在接受EBD后可以短期内缓解梗阻症状,但大多数患儿需接受1次以上的EBD治疗,且行2次以上EBD后症状仍有反复,需积极手术治疗[13]。本组HP阳性患儿行规律内科治疗后转阴,有3例术前行EBD,2例治疗过程顺利,其中1例行4次EBD治疗,梗阻症状仍有反复,1例怀疑穿孔患儿腹腔镜探查见十二指肠周围结缔组织充气表现。目前消化性溃疡的手术方式包括胃窦部切除联合迷走神经切断术、毕Ⅱ术联合迷走神经干切断术、HMP联合或不联合迷走神经切断术。对于胃出口附近组织瘢痕形成不严重的患儿,HMP是相对安全和简单的术式,它可以避免或降低前两种术式吻合口张力高、吻合口溃疡及胆汁反流性胃炎等并发症的风险[2]。本组4例均行HMP,术后随访13~59个月,其中1例术后6个月内偶有胃潴留,经胃肠减压、使用促胃动力药物、逐步过渡饮食等保守治疗后好转。
四、嗜酸性粒细胞性胃肠炎EGE是一种以EOS异常浸润消化道各层为特征的少见疾病,部分患儿与进食特殊食物导致过敏相关,可分为黏膜型、肌型、浆膜型,混合型[14]。其诊断方法目前按Tally等[15]提出的标准,EOS浸润常呈局灶性分布,多部位、多黏膜活检(至少6点)可提高EGE的诊断率。本组2例患儿有牛奶过敏史,术前影像学检查提示幽门部及周围胃壁肌层增厚,行胃镜黏膜活检提示EOS大量浸润[>20个/高倍视野(high-power field, HPF)],排除其他可能引起EOS增多的疾病后确诊为肌型EGE。大部分EGE内科治疗效果良好,手术只适用于出现胃肠梗阻后不能缓解的病例[16]。据以往报道胃部病变可采用的术式包括胃部分切除或加Roux-en-Y术、毕Ⅱ术等[17]。本组2例合并明显的GOO症状,经激素治疗后症状无改善而行HMP,术后病理结果提示肌层水肿肥厚,EOS大量浸润。2例术后分别随访15个月、32个月,未再出现腹痛及梗阻症状,由于EGE往往累及多部位,对于EGE致胃流出道梗阻患儿行HMP的远期效果的评价,需在增加病例的基础上进一步长期随访。
五、化学性损伤GOO是儿童误服强腐蚀性化学制剂(强酸、强碱等)最常见的并发症,一般出现于误服后2~8周,治疗方式包括EBD和手术,但EBD失败及出现并发症的概率较高,手术仍是目前主要治疗手段之一,具体手术方式可根据病变范围、程度及手术医师经验来决定[18]。部分研究认为应在该并发症出现早期进行手术以降低死亡率,也有报道认为应延期手术,主要原因是早期胃壁水肿与周围组织粘连严重,另外胃壁纤维化仍在继续发展,早期手术不利于确定病变范围[19]。本组1例误服氯化锌溶液的患儿在GOO出现后先行空肠造瘘术解决喂养问题,3个月后行开放手术见胃窦近幽门处瘢痕狭窄,遂行HMP,术后恢复良好。
综上所述,针对不同良性病因引起的GOO,可先行幽门环肌切开术、ESD、EBD、内科药物治疗等,HMP对于经以上治疗效果不佳的GOO患儿可以起到很好的效果;且相比其他消化道重建手术,该方法简便易行,创伤小,最大限度保留了胃出口的正常生理和解剖,可以减少胆汁反流性胃炎、吻合口溃疡及狭窄等并发症的发生,减轻对患儿生长发育的影响,但远期预后有待进一步随访研究。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明 陶波圆、兰梦龙、梁子建负责研究的设计、实施和起草文章;刘斐、徐晓钢进行病例数据收集及分析;曾纪晓负责研究设计与酝酿,并对文章知识性内容进行审阅
| [1] |
Lovasik BP, Dodson TF, Srinivasan JK. Heineke, Mikulicz, Jaboulay, and Finney: innovators of surgical pyloroplasty[J]. Am Surg, 2021, 87(5): 737-740. DOI:10.1177/0003134820952820 |
| [2] |
Søreide K, Sarr MG, Søreide JA. Pyloroplasty for benign gastric outlet obstruction-indications and techniques[J]. Scand J Surg, 2006, 95(1): 11-16. DOI:10.1177/145749690609500103 |
| [3] |
Al-Ansari A, Altokhais TI. Recurrent pyloric stenosis[J]. Pediatr Int, 2016, 58(7): 619-621. DOI:10.1111/ped.12958 |
| [4] |
Simeonov M, Yonkov A. Recurrent hypertrophic pyloric stenosis-diagnostics and treatment[J]. Khirurgiia (Sofiia), 2016, 82(2): 52-56. |
| [5] |
Mazurak M, Patkowski D. A history of the surgical correction of pyloric stenosis[J]. J Pediatr Surg, 2021, 56(10): 1904-1907. DOI:10.1016/j.jpedsurg.2021.05.009 |
| [6] |
潘静, 杨天佑, 杨纪亮, 等. 小儿胃部占位性病变的诊治分析[J]. 临床小儿外科杂志, 2017, 16(5): 439-443. Pan J, Yang TY, Yang JL, et al. Diagnosis and treatment of space-occupying gastric mass in children[J]. J Clin Ped Sur, 2017, 16(5): 439-443. DOI:10.3969/j.issn.1671-6353.2017.05.006 |
| [7] |
Liu F, Xu XG, Lan ML, et al. Clinical characteristics of gastric duplication in children[J]. Front Pediatr, 2022, 10: 857056. DOI:10.3389/fped.2022.857056 |
| [8] |
Doya LJ, Hassan NT, Bijow FW, et al. An unusual cause of recurrent pediatric vomiting (an extraluminal pyloric duplication cystic): a case report[J]. Oxf Med Case Reports, 2020, 2020(12): omaa119. DOI:10.1093/omcr/omaa119 |
| [9] |
Fang Y, Gao TJ, Yang HB, et al. Removal of an infant's gastric duplication cyst through endoscopic submucosal dissection: a case report[J]. Medicine (Baltimore), 2019, 98(12): e14820. DOI:10.1097/MD.0000000000014820 |
| [10] |
Noh JH, Kim DH, Kim SW, et al. Endoscopic submucosal dissection as alternative to surgery for complicated gastric heterotopic pancreas[J]. World J Clin Cases, 2020, 8(20): 4708-4718. DOI:10.12998/wjcc.v8.i20.4708 |
| [11] |
Gong EJ, Kim DH, Jung HY, et al. Clinical outcomes of endoscopic resection for gastric neoplasms in the pylorus[J]. Surg Endosc, 2015, 29(12): 3491-3498. DOI:10.1007/s00464-015-4099-8 |
| [12] |
Gryboski JD. Peptic ulcer disease in children[J]. Med Clin North Am, 1991, 75(4): 889-902. DOI:10.1016/s0025-7125(16)30419-9 |
| [13] |
Chao HC. Update on endoscopic management of gastric outlet obstruction in children[J]. World J Gastrointest Endosc, 2016, 8(18): 635-645. DOI:10.4253/wjge.v8.i18.635 |
| [14] |
朱莉, 龙梅, 王颖. 儿童嗜酸性粒细胞性胃肠炎[J]. 中国实用儿科杂志, 2021, 36(4): 245-249. Zhu L, Long M, Wang Y. Eosinophilic gastroenteritis in children[J]. Chin J Pract Pediatr, 2021, 36(4): 245-249. DOI:10.19538/j.ek2021040602 |
| [15] |
Talley NJ, Shorter RG, Phillips SF, et al. Eosinophilic gastroenteritis: a clinicopathological study of patients with disease of the mucosa, muscle layer, and subserosal tissues[J]. Gut, 1990, 31(1): 54-58. DOI:10.1136/gut.31.1.54 |
| [16] |
Koutri E, Papadopoulou A. Eosinophilic gastrointestinal diseases in childhood[J]. Ann Nutr Metab, 2018, 73(Suppl 4): 18-28. DOI:10.1159/000493668 |
| [17] |
Vargas-Rubio R, Meek-Benigni E, Henao-Pérez F, et al. Gastric outlet obstruction as manifestation of eosinophilic gastroenteritis[J]. Rev Gastroenterol Peru, 2020, 40(2): 173-176. DOI:10.47892/rgp.2020.402.1086 |
| [18] |
Soomro MA, Aftab M, Hasan M, et al. Heineke-Mikulicz pyloroplasty for isolated pyloric stricture caused by corrosive ingestion in children[J]. Pak J Med Sci, 2020, 36(1): S87-S90. DOI:10.12669/pjms.36.ICON-Suppl.1714 |
| [19] |
Özokutan BH, Ceylan H, Ertaşkin I ·, et al. Pediatric gastric outlet obstruction following corrosive ingestion[J]. Pediatr Surg Int, 2010, 26(6): 615-618. DOI:10.1007/s00383-010-2613-6 |
 2023, Vol. 22
2023, Vol. 22


