胃穿孔是Ⅲ型先天性食管闭锁较少见的一种并发症,在先天性食管闭锁中发生率约为1%[1],病死率达12.5% ~29%[2, 3]。患者病情进展快,诊治难度大,若不采取积极有效的治疗,病死率可达100%[4]。本文回顾性分析湖南省儿童医院收治的7例Ⅲ型食管闭锁并胃穿孔患者临床特点及诊治经验。
材料与方法 一、临床资料2007年1月1日至2021年1月1日本院新生儿外科收治先天性食管闭锁623例,其中7例发生胃穿孔,发生率为1.1%。7例中男6例,女1例,均为Ⅲ型食管闭锁,出生体重1 350~3 000 g,平均(2 278.5±639.5)g;胎龄33~40+1周,平均(35.5±2.6)周;入院时年龄1~3 d,平均(1.5±0.7) d;发生胃穿孔时年龄2~4 d,平均(3.2±0.9)d。6例予气管插管呼吸机辅助通气,呼吸机使用模式为SIMV模式。均无重要脏器畸形。临床资料详见表 1。
| 表 1 7例Ⅲ型食管闭锁并胃穿孔患者临床资料 Table 1 General characteristic of 7 patients with type-Ⅲ EA complicated by gastric perforation |
|
|
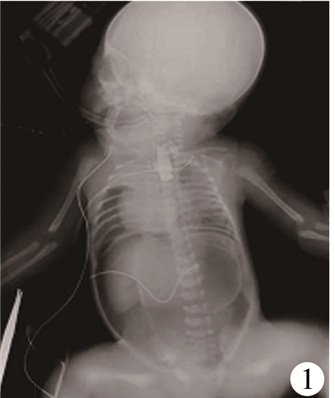
予禁食、食管近盲端置管抽吸、呼吸机辅助通气、抗感染、加强呼吸道管理等对症处理。胸腹部X线检查见胃管卷曲于近端食管盲袢内,双肺纹理增多、模糊,可见斑片状模糊影,腹部见肠气影。经食管造影明确诊断为Ⅲ型食管闭锁,并确定食管近端闭锁位置。治疗过程中腹胀、呼吸困难加重,胸腹X线检查提示气腹,其中病例2、7入院时存在明显呼吸困难、腹胀,食管造影明确诊断为食管闭锁并发胃穿孔(图 1)。
|
图 1 Ⅲ型食管闭锁并发胃穿孔患者食管造影检查结果 注 食道于T3水平呈盲端改变,腹部可见大片状透亮影,双膈下呈弧形透亮影 Fig.1 Esophagography picture of type-Ⅲ EA complicated by gastric perforation |
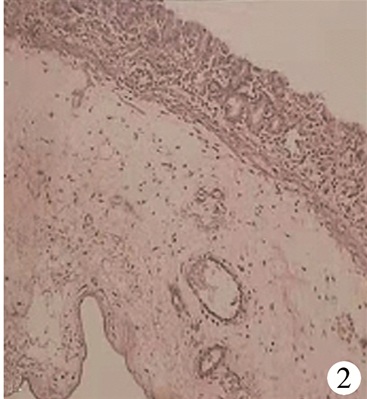
7例胃穿孔后即出现腹部膨隆、呼吸困难加重、血氧饱和度下降等,上调呼吸机参数难以维持呼吸稳定,予紧急腹腔穿刺抽气减压,取脐与剑突连线中点为腹腔穿刺抽气点,穿刺后注射器回抽出大量气体,腹胀缓解,呼吸情况及氧合状况暂时好转。经确诊先天性食管闭锁并发胃穿孔后行急诊手术,但病例5、6、7家长放弃手术出院。病例4行开胸食管气管瘘结扎、食管端端吻合、开腹坏死胃壁切除胃修补术,病例1、2、3行胸腔镜下食管气管瘘结扎、食管端端吻合、开腹胃穿孔修补术。病例4术后病理检查提示先天性胃壁肌层缺损(图 2),其余3例因术中探查未见异常,故未行组织病理检查。4例手术患者术中情况见表 2。
|
图 2 病例4病理检查结果(HE, ×40倍) 注 黏膜及黏膜下层未见肌层,部分黏膜坏死脱落,符合先天性胃壁肌层缺损并胃壁出血坏死改变 Fig.2 Pathology test image of patient 4 (40×) |
| 表 2 4例经手术治疗的Ⅲ型食管闭锁并发胃穿孔患者手术情况 Table 2 Perioperative management of 4 patients with type-Ⅲ EA complicated by gastric perforation |
|
|
7例Ⅲ型食管闭锁并发胃穿孔患者中,3例放弃手术病例于出院后不久即死亡,4例经手术治疗痊愈出院。术后呼吸机辅助呼吸时间5~10 d, 手术后开始喂养时间为术后第7天,总住院时间20~92 d,平均(41±34)d。出院后随访1~2年,平均随访(1.5±0.3)年,无一例复发气管食管瘘;1例出现吻合口狭窄,经球囊扩张治疗后治愈。目前4例均经口喂养,进食可,生长发育良好,体重增长正常。
讨论根据Gross五型分类法,Ⅲ型食管闭锁是食管闭锁中最常见类型,占82% ~85%[5]。气体可随呼吸经食管气管瘘进入胃肠道,尤其是需机械辅助通气时,由于患者食管闭锁无法行胃肠减压,大量气体进入胃肠道引起腹胀,甚至发生胃穿孔[6, 7]。同时约37%的先天性食管闭锁患者为早产儿或低出生体重儿,其出生后因肺发育不良、肺表面活性物质缺乏、合并吸入性肺炎等原因,容易并发新生儿呼吸窘迫综合征而需要机械辅助通气,因此发生胃穿孔的风险增加[8, 9]。有学者认为机械辅助通气是先天性食管闭锁胃穿孔的病因之一[6]。也有文献报道先天性食管闭锁在没有机械辅助通气的情况下发生胃穿孔[3]。因此有学者认为先天性食管闭锁并发胃穿孔的原因可能是胎儿期胃肠道缺乏羊水营养而使胃壁肌层先天发育不全所致[10]。本组除病例4不需机械辅助通气外,其余6例均需机械辅助通气;除病例4合并先天性胃壁肌层缺损、胃穿孔范围较大外,其余3例胃穿孔范围较小,且无胃壁肌层发育异常。同时病例1、2、3的气管导管末端位于气管食管瘘口附近,因此我们也认为气管插管后机械辅助通气、气管导管末端位置位于瘘管附近可能是Ⅲ型食管闭锁发生胃穿孔的诱因[1, 6]。同时呼气机参数过高可增加进入消化道的气体量,增加胃穿孔的风险,建议使用压力限制性通气、同步间歇正压通气、高频振荡通气等方式辅助通气,以降低通气压力,减少进入消化道的气体量,降低胃穿孔发生率[1]。我们的体会是早期明确诊断,加强食管近盲端抽吸及有效的呼吸道管理,减少使用呼吸机辅助通气的概率;若确实需呼吸机辅助通气,气管导管末端位置应尽可能低,将气管导管置于瘘管以远的位置,以避免远端瘘管开放,减少气体进入胃肠道,降低胃内压,减少胃扩张的发生。
胃穿孔发生后大量气体进入腹腔,腹腔压力急剧升高,引起膈肌抬高,同时限制膈肌运动,出现潮气量减少、静脉回流量减少、心血管功能衰竭等一系列病理生理改变,使呼吸衰竭、循环衰竭等病情继续恶化[11]。呼吸衰竭加重则需上调呼吸机参数以维持足够的氧合和保持良好的通气,此时进入胃肠道内的气体量增加进而加重腹腔高压,形成恶性循环。因此,当Ⅲ型食管闭锁患者突发腹胀或腹胀急剧加重、呼吸困难加重而上调呼吸机参数仍难以维持呼吸平稳时,需考虑发生胃穿孔的可能,应立即行腹部X线检查以明确诊断[12]。
一旦发生胃穿孔,紧急处理措施应着重于将逐渐增加的腹压降低至患者可耐受水平[13]。此时患者难以耐受复杂及长时间的有创操作,采取简单有效的处理方式非常关键。腹腔穿刺抽吸或腹腔穿刺置管引流被认为是一种有效且安全的处理方法[2]。腹腔穿刺抽吸或腹腔穿刺置管引流可降低腹腔内高压,缓解腹胀,解除膈肌钳闭状态,降低呼吸机使用参数,减轻患者呼吸困难。这样不仅缓解了急剧恶化的病情,还可为后续手术治疗创造条件。该操作简单易行,术前术中可重复操作。
Ⅲ型食管闭锁并发胃穿孔病死率高达12.5% ~29%,是食管闭锁患者的灾难性并发症[1, 4, 14]。一经确诊,需急诊手术治疗,首要任务是结扎气管食管瘘阻止空气持续进入消化道,重塑呼吸道的完整性[4]。该病发病率低,病例数较少,相关诊疗经验尚不足,因此,其手术方式及治疗策略尚未形成共识,相关文献以个案报道为主。Othersen[15]首次报道1例先天性食管闭锁并胃穿孔患者的成功经验,其手术方式为先行穿孔胃壁修补、胃造瘘术,同期再行开胸气管食管瘘修补、食管端端吻合术,患者术后恢复良好。Mikami等[16]采用同样方式治愈1例先天性食管闭锁并胃穿孔患者。Jones等[17]报道先行穿孔胃壁修补、胃造瘘,再行开胸气管食管瘘修补、食管端端吻合术的方式治疗4例先天性食管闭锁并胃穿孔,但仅有1例治愈出院。Maoate等[18]认为先天性食管闭锁一旦发生胃穿孔,患者病情极其危重,手术风险极大,因此宜先行剖腹探查后经胃壁穿孔处放置球囊导管封堵气管食管瘘,再开胸结扎气管食管瘘,根据病情决定是否同期行食管端端吻合术,最后行穿孔胃壁修补、胃造瘘术;在其收治的6例患者中,2例行延期食管端端吻合术,3例治愈出院。Rathod等[3]认为对先天性食管闭锁并胃穿孔患者行一期开胸气管食管瘘结扎、食管端端吻合,剖腹探查后行胃壁穿孔修补的方式是可行的,其诊治的6例患者中除2例术后死于败血症外,其余4例均治愈出院,且长期随访患者生活质量良好。
我们的诊治体会是患者经术前紧急处理后若能耐受麻醉及单肺通气,可待其呼吸、循环功能稳定后尽早结扎气管食管瘘。本组4例手术患者均于腹腔穿刺抽吸、呼吸及循环功能稳定后在胸腔镜下结扎食管气管瘘,疗效确切,且耗时短,结扎食管气管瘘后患者呼吸情况得到极大改善,保证了后续手术的安全性。同时患者胃穿孔范围小,无外源性食物经穿孔胃壁进入腹腔,且有局部大网膜包裹,腹腔感染较轻,因此先行胸部手术再行腹部手术,不会加重腹腔感染而影响患者预后,理论上更加合理;另外胸腔镜下手术治疗先天性食管闭锁也更具优势[19, 20]。若患者不能耐受麻醉及单肺通气,则可先行胃造瘘术,待病情好转后再行二期手术治疗食管闭锁。
综上所述,Ⅲ型食管闭锁并发胃穿孔后,腹腔穿刺抽吸或腹腔穿刺置管引流是有效的紧急处理方式。胸腔镜下气管食管瘘结扎、食道端端吻合术后再行开腹胃壁修补术是可行的。但由于本组病例数较少,如何把握机械辅助通气时机、如何准确调节呼吸机参数以避免大量气体进入胃肠道、进而预防胃穿孔的发生以及是否需要常规行胃造瘘术等,尚需更多临床病例的进一步研究。
| [1] |
Thompson A, Thakkar H, Khan H, et al. Not all neonates with oesophageal atresia and tracheoesophageal fistula are a surgical emergency[J]. J Pediatr Surg, 2018, 54(2): 244-246. DOI:10.1016/j.jpedsurg.2018.10.074 |
| [2] |
Okumuş M, Zübarioglu AU, Atalan R. Treatment of two newborns with esophageal atresia and distal tracheoesophageal fistula complicated by gastric perforation: choosing the simple way[J]. Acta Chir Belg, 2020, 120(4): 282-285. DOI:10.1080/00015458.2018.1564491 |
| [3] |
Rathod KK, Bawa M, Mahajan JK, et al. Management of esophageal atresia with a tracheoesophageal fistula complicated by gastric perforation[J]. Surg Today, 2011, 41(10): 1391-1394. DOI:10.1007/s00595-010-4460-4 |
| [4] |
Yang CY, Lien R, Fu RH, et al. Prognostic Factors and Concomitant Anomalies in Neonatal Gastric Perforation[J]. J Pediatr Surg, 2015, 50(8): 1278-1282. DOI:10.1016/j.jpedsurg.2015.04.007 |
| [5] |
Lennep MV, Singendonk M, Dall' Oglio L, et al. Oesophageal atresia[J]. Nat Rev Dis Primers, 2019, 5(1): 26. DOI:10.1038/s41572-019-0077-0 |
| [6] |
Gupta A, Pande D, Kachru N, et al. Tracheoesophageal fistula complicated by iatrogenic gastric perforation in a low birth weight neonate[J]. J Nepal Health Res Counc, 2020, 18(2): 324-326. DOI:10.33314/jnhrc.v18i2.2408 |
| [7] |
蔡威, 孙宁, 魏光辉. 小儿外科学[M]. 北京: 人民卫生出版社, 2014: 231-235. Cai W, Sun N, Wei GH. Pediattric Surgery[M]. Beijing: People's Medical Publishing House, 2014: 231-235. |
| [8] |
Sulkowski JP, Cooper JN, Lopez JJ, et al. Morbidity and mortality in patients with esophageal atresia[J]. Surgery, 2014, 156(2): 483-491. DOI:10.1016/j.surg.2014.03.016 |
| [9] |
Malone PS, Kiely EM, Brain AJ, et al. Tracheo-oesophageal fistula and pre-operative mechanical ventilation[J]. Aust N Z J Surg, 2010, 60(7): 525-527. DOI:10.1111/j.1445-2197.1990.tb07419.x |
| [10] |
Acer T, Karnak I, Yalçin S, et al. Why gastric perforation occurs in patients with isolated esophageal atresia: more vulnerable stomach?[J]. Turk J Pediatr, 2012, 54(3): 312-316. DOI:10.1007/s003830050504 |
| [11] |
Taneja B, Saxena KN. Endotracheal intubation in a neonate with esophageal atresia and trac trachea-esophageal fistula: pitfalls and techniques[J]. J Neonatal Surg, 2014, 3(2): 18. DOI:10.1007/BF03020635 |
| [12] |
Bonanno C, Wapner RJ. Antenatal corticosteroids in the management of preterm birth: are we back where we started?[J]. Obstet Gynecol Clin North Am, 2012, 39(1): 47-63. DOI:10.1016/j.ogc.2011.12.006 |
| [13] |
Li XW, Jiang YJ, Wang XQ, et al. A scoring system to predict mortality in infants with esophageal atresia: A case-contronl study[J]. Medicine, 2017, 96(32): e7755. DOI:10.1097/MD.0000000000007755 |
| [14] |
Roumiantsev S. Invasive Mechanical Ventilation in Premature Infants: Where do we Stand Today?[J]. J Pulm Respir Med, 2013, 13(1). DOI:10.4172/2161-105X.S13-002 |
| [15] |
Othersen HB, Gregorie HB. Pneumatic rupture of the stomach in a newborn infant with esophageal atresia and tracheoesophageal fistula[J]. Surgery, 1963, 53(3): 362. DOI:10.1016/S0911-6044(99)00020-2 |
| [16] |
Mikami K, Terazaki T, Kimura T, et al. Case of congenital tracheo-esophageal fistula complicated by gastric perforation[J]. Iryo, 1967, 21(11): 1327-1330. |
| [17] |
Jones TB, Kirchner SG, Lee FA, et al. Stomach rupture associated with esophageal atresia, tracheoesophageal fistula, and ventilatory assistance[J]. Ajr Am J Roentgenol, 1980, 134(4): 675-677. DOI:10.2214/ajr.134.4.675 |
| [18] |
Maoate K, Myers NA, Beasley SW. Gastric perforation in infants with oesophageal atresia and distal tracheo-oesophageal fistula[J]. Pediatr Surg Int, 1999, 15(1): 24-27. DOI:10.1007/s003830050504 |
| [19] |
周崇高, 李碧香. 胸腔镜下手术治疗先天性食管闭锁[J]. 临床小儿外科杂志, 2018, 17(3): 12-15. Zhou CG, Li BX. Thoracoscopic surgery for esophageal atresia[J]. J Clin Ped Sur, 2018, 17(3): 12-15. DOI:10.3969/j.issn.1671-6353.2018.03.002 |
| [20] |
夏仁鹏, 周崇高, 李碧香, 等. 胸腔镜手术与开胸手术治疗Ⅲ型食管闭锁的对比研究[J]. 临床小儿外科杂志, 2018, 17(3): 179-183. Xia RP, Zhou CG, Li BX, et al. Comparative study of thoracoscopy and thoracotomy for the treatment of type Ⅲ esophageal atresia[J]. J Clin Ped Sur, 2018, 17(3): 179-183. DOI:10.3969/j.issn.1671-6353.2018.03.005 |
 2021, Vol. 20
2021, Vol. 20


