寄生胎是指一个具有围绕着椎骨轴排列的器官或肢芽的胎儿被包裹在另一个分化完全、正常的胎儿体内,通常发生于上腹膜后。该疾病非常罕见,其发病机制存在争议,通常经母亲孕期常规产检时发现,表现为胎儿腹部出现逐渐增大的囊实性包块,典型的影像学表现为椎骨轴样钙化,预后良好。本文总结了华中科技大学同济医学院附属湖北妇幼保健院7例腹膜后寄生胎病例资料,对其产前超声特征、病理特征、术前术后AFP和手术方式进行分析,并对相关文献进行回顾,旨在分析产前超声对寄生胎的评估作用以及寄生胎的治疗方式。
材料与方法对2016年11月至2019年11月华中科技大学同济医学院附属湖北妇幼保健院小儿外科收治的腹膜后寄生胎病例进行分析,纳入标准:①产前检查考虑为寄生胎;②于我院行手术治疗且病理检查诊断为寄生胎。排除标准:①产前诊断为寄生胎,但未在本院手术治疗;②病理检查提示其他疾病。根据以上标准,共纳入患者7例,其中男4例,女3例。收集其性别、年龄、产前超声、寄生部位、寄生胎数目、手术方式、术前术后AFP、合并症以及病理结果资料整理成表。
以“寄生胎”、“胎中胎”或“fetus-in-fetu”,“parasite twin”为关键词在中国知网、万方数据库、PubMed自2010—2020年收录的文献进行检索,将文献中报道的病例与本次收集病例进行比较。纳入标准:①病理诊断为寄生胎或影像学提示有脊柱或长骨; ②病例资料相对完善。排除标准:①缺乏病理和影像学结果; ②重复病例; ③联体双胎; ④病例资料不完善。根据以上标准,共检索到96篇文献、144例病例,总结患者临床信息并制作成表。
结果本组无一例手术死亡。患者年龄1~21 d,出生体重(3.25~3.85)kg。7例均在产前超声检查时发现腹部肿块,发现腹部肿块的时间为孕22~30周,超声检查提示胎儿腹部可见囊实性包块,边界清楚,胎内可见胚胎样结构及骨性成分,彩色多普勒超声可见内有血流信号,4例(57.14%)可见脐带样血管结构。产前超声检查主要表现为随孕周逐渐增大的腹部包块,部分病例出生后喂养出现呕吐症状。其中3例寄生胎位于左腹膜后,3例位于右腹膜后,1例位于中腹膜后。5例为单胎寄生胎,2例为双胎寄生胎。术前、术后通过辅助检查发现1例合并不全性肠梗阻及先天性肠粘连,1例合并新生儿肠梗阻,1例合并梅克尔憩室,1例合并右肾上腺区畸胎瘤。7例中有4例行开腹手术,2例行微创手术,1例行微创转开腹手术。7例住院时间14~20 d,其中两例微创手术患者住院时间为14 d,住院期间无特殊情况,临床治愈出院,1例双寄生胎患者术后1个月复诊,因“B超下见胰头前方及下方8.6 cm×5.0 cm无回声区”再次入院,入院后全麻下行腹腔镜探查+经皮腹腔包裹性积液穿刺引流+腹腔引流术,术后11 d治愈出院。本组相关临床资料见表 1。典型病例照片见图 1至图 3。
| 表 1 7例腹膜后寄生胎患者资料 Table 1 Clinical data of 7 cases of retroperitoneal parasitic fetus |
|
|

|
图 1 病例3双寄生胎产前彩超(37w)、手术后标本平片及标本a的正位片 Fig.1 Prenatal ultrasound (37w) of double FIF, radiography of postoperative specimen and anteroposterior radiograph of specimen a in Case 3 A:彩超示正常胎儿腹腔内可见两个不成形的胎儿,两个胎儿之间见光带分隔,右侧胎儿较大,可见部分肢体及躯干结构,左侧胎儿可见骨性结构及脊柱回声;B:标本a可见脊柱、肋骨、双下肢以及足样组织,标本b可见脊柱及肋骨样骨组织;C:标本a正位片可见四肢、双足以及脐带样、生殖器样结构 |
|
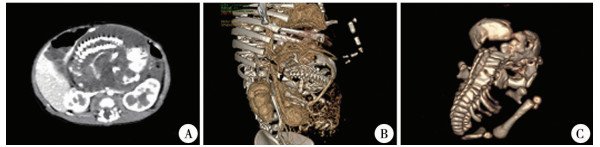
图 2 病例5生后CT增强、三维重建及术后标本的三维重建 Fig.2 Postnatal CT enhancement, 3D reconstruction and 3D reconstruction of postoperative specimens in Case 5 A:中上腹中线略偏左侧见巨大混杂密度占位,病灶大小约5.8 cm×5.9 cm×7.5 cm,边界清晰,增强扫描病灶局部强化,可见颅骨、脊柱、四肢骨骼影,以及软组织、液体、脂肪组织影;B: 示肠系膜上动脉分支血管进入病灶(黑色箭头);C:标本三维重建左骶前位片,可见颅骨、脊柱、四肢骨骼影 |
|
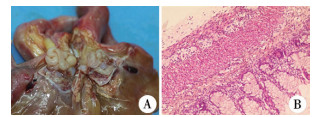
图 3 病例2双胎之一解剖及病理图 Fig.3 Anatomical specimen and pathological examination of one of double FIF A:可见肠管及骨性结构;B:HE染色(×10)示肠管结构,肌间可见神经节细胞 |
共搜索出中文文献35篇(63例),其中男27例(42.86%),女30例(47.62%),未描述性别6例(9.52%)。单胎59例(93.65%),双胎3例(4.76%),三胎1例(1.59%)。位于腹膜后37例(58.73%),其中左腹膜后11例,右腹膜后10例,下腹膜后1例,中腹膜后1例,全腹部3例,未描述具体位置11例;腹腔17例(26.98%);骶尾部3例(4.76%);口腔2例(3.17%);盆腔2例(3.17%);肠系膜1例(1.59%);左隐睾内1例(1.59%)。合并畸胎瘤2例(3.17%),左侧隐睾2例(3.17%),左肾错构瘤1例(1.59%),肛门闭锁+双肾积水1例(1.59%,生后因呼吸窘迫综合征死亡),双肾积水1例(1.59%),不孕1例(1.59%),双侧睾丸鞘膜积液1例(1.59%)。传统开放手术56例(88.89%),腹腔镜辅助手术2例(3.17%),引产4例(6.35%),死亡1例(未手术)(1.59%)。产前疑诊为寄生胎16例(25.40%),最早一例为孕16周于患者口腔中发现肿物,引产后病理证实为寄生胎。年龄最大者为一60岁男性。肿物大小为(3~ 39)cm×(3~26)cm×(2~15)cm。大部分文献并未描述肿物的供应血管,较多见的供应血管是腹主动脉或肠系膜上动脉及其分支。
国外文献61篇,多为单病例报道,最多为10例报道,共81例。其中男36例(44.44%),女39例(48.15%),未描述性别6例(7.41%)。单胎75例(92.59%),双胎5例(6.17%),三胎1例(1.23%)。腹膜后54例(66.67%,左腹膜后16例,右腹膜后23例,下腹膜后1例,全腹部1例,未描述具体位置13例);腹腔7例(8.64%);骶尾部5例(6.17%);颅内5例(6.17%);纵膈3例(3.70%);口腔1例(1.23%);胸腔1例(1.23%);左肺1例(1.23%);口颈部1例(1.23%);左阴囊1例(1.23%);右阴囊1例(1.23%);右侧附件1例(1.23%)。合并左侧睾丸萎缩1例(1.23%),NEC 1例(1.23%),主动脉缩窄1例(1.23%),代谢性骨病1例(1.23%)。传统开放手术78例(96.30%),术后死亡4例(4.94%),未手术死亡3例(3.70%)。产前疑诊为寄生胎32例(39.51%),最早一例孕19周于患者骶尾部发现肿物,术后病理结果证实为寄生胎。年龄最大者为一17岁女性,肿物大小(3~30)cm×(2~16)cm×(2~10)cm。大部分文献未描述供应血管,其中腹主动脉供血17例(20.99%),肠系膜上动脉供血4例(4.94%),肾动脉供血4例(4.94%,1例与腹主动脉共同供血,1例与肠系膜上动脉共同供血),脾动脉供血3例(3.70%),胸主动脉供血1例(1.23%),右肝动脉供血1例(1.23%),右睾丸动脉供血1例(1.23%),右髂内动脉+骶正中动脉供血1例(1.23%)。总结中外文献所收集的144例病例资料见表 2。
| 表 2 144例寄生胎患者临床信息 Table 2 Clinical profiles of 144 parasitic fetuses |
|
|
寄生胎又称胎中胎,是一种非常罕见的先天性疾病,其发病率为1/500 000[1]。1800年Meckel首次描述寄生胎,1953年Willis将其定义为包含椎骨轴以及周围具有其他器官和肢体的肿块[1]。寄生胎多为单胎寄生,也有多胎寄生,多在婴儿期被发现[2]。本文回顾国内外文献发现, 男女发病率无明显差异。寄生胎多位于寄主胎儿的腹膜后区,也有位于颅内、口腔、纵隔、肺部、肝脏、阴囊、骨盆、肠系膜、骶尾部的报道[3-5]。
一、发病机制寄生胎的发病原因尚不清楚,目前大多数人接受的观点是单卵双胎理论或畸胎瘤理论。单卵双胎理论是指由于受精卵在胚胎发育早期不均等分裂,导致较小的内细胞团被包裹进较大的内细胞团所发育的胎儿体内。可通过检验寄生胎、寄主之间是否具有相同的性别、血型以及DNA等位基因来验证[6]。Lee[7]报道了一例21三体综合征患者,其腹内寄生胎经基因型测定证实也为21三体综合征。但根据Hing[8]报道,寄生胎和寄主之间具有相同的性别、血型以及等位基因,也只能说明寄生胎与卵巢畸胎瘤的发病机制不同,并不能够用于区分寄生胎和高度分化的性腺外畸胎瘤、睾丸畸胎瘤,可能需要一个新的办法来验证寄生胎的单卵双胎理论。畸胎瘤理论是指寄生胎本质上为高度分化的畸胎瘤,但Wills提出,畸胎瘤是由于多功能内细胞团的聚集引起,多位于下腹膜后,不能分化出成形的器官和椎骨轴,具有恶性潜能,推翻了寄生胎等同于畸胎瘤的理论。但寄生胎和畸胎瘤同时出现在同一患者体内的现象暂时无法得到解释,如本组病例,所以寄生胎的发病机理仍需研究[5]。
二、临床表现及诊断寄生胎的临床症状与其所在部位有关,表现为肿块的占位效应,例如腹胀、呼吸困难、呕吐、黄疸、肠梗阻以及对肾脏的压迫作用[9]。Willis强调影像学中有椎骨轴的存在可确定寄生胎的诊断,以前寄生胎大多通过X线、CT以及MRI进行初步诊断,术后病理检查确诊,所以产前诊断寄生胎的病例较少。但随着影像学的发展,B超逐渐成为产前诊断寄生胎的主要手段,具有经济、安全、精准、可重复等优点。本组7例均经产前超声诊断为寄生胎,最早疑诊为寄生胎的1例在孕22+2周即被诊断。
常规产前超声检查时可以在胎儿腹内看到混合肿块,边界清楚、壁薄(代表羊膜),包含软组织、骨性结构(散在骨、软骨、长骨等)以及不规则无回声区(代表羊水)。随着孕周增加,可见类似胎儿脊柱呈串珠状排列,逐渐具备胎儿形态,彩色多普勒超声可见其内有血流信号及脐带样血管结构。同时,产前MRI可以清晰显示包块的包膜、低信号的羊水以及无信号的脊柱、肋骨等骨性成分,进一步验证超声结果。胎儿出生后CT可见腹部囊实性肿块,包含液体、软组织以及显示清晰的椎骨轴和长骨,同时三维CT可见寄生胎与其血液供应之间的关系,有利于手术方案的制定[2]。但回顾文献发现并非所有病例都能发现椎骨轴,Hoeffel[10]回顾了87例寄生胎,并指出影像学在诊断中起着重要的作用,但在腹部平片或CT扫描中不显示椎骨轴并不能排除该诊断。β-HCG和AFP水平可升高或者正常,新生儿期AFP可达5×104 ng/mL,6个月至1岁时逐渐降至正常成人水平,本组病例AFP的升高存在生理因素的影响,但术后可下降(病例3、病例4、病例7),尤其是病例4、病例7两者复查时间相近,AFP下降明显,考虑AFP的升高可能也与寄生胎有关;对于术后AFP未降者(病例5、病例6),考虑术后复查时间较近,导致AFP下降不明显。
三、鉴别诊断寄生胎的鉴别诊断主要是腹部有钙化结构的肿块,如畸胎瘤、胎粪性假性囊肿等。畸胎瘤属于生殖细胞肿瘤,起源于异位具有多向分化潜能的干细胞,系胚胎发育时期生殖细胞从卵黄囊向泌尿生殖嵴迁移失败、脱落聚集所致,一般含有外、中、内三个胚层的多组织成分,也可含有1~2层的胚层成分,多发生在下腹部、盆腔、骶尾部。非典型寄生胎(不含椎骨轴)与成熟畸胎瘤难以鉴别,在超声检查下,成熟畸胎瘤为混合回声,边界清楚,有包膜,包括液体及钙化成分,其中液性成分占肿块的大部分,内可见密集的点状强回声,无高度分化的器官、椎骨轴及肢体,彩色多普勒超声示肿块周边稀疏血流信号,而肿块内部未见明显血流信号,也无脐带样血管结构;CT上表现为零星散在骨化或钙化影;在MRI上表现为混杂信号肿块,其特征是肿块内含脂肪信号灶,即T1WI上呈高信号、T2WI上呈中等信号-高信号[11];两者最终通过病理检查区别,畸胎瘤病检结果多为毛发、牙齿、部分肠管,无长骨、肢芽、脊柱以及其他分化完全的器官。胎粪性假性囊肿影像学检查表现为腹部钙化,多包括腹水和气腹,而寄生胎中的钙化发生在椎骨轴和长骨,无腹水和气腹[12]。
四、治疗方式及病理检查寄生胎一经诊断,需尽早手术,以免在患者生长发育过程中肿块与周围组织粘连导致手术困难。有文献报道位于右上腹的寄生胎与胆道粘连可引起术后胆瘘,最终导致患者死亡[13]。根据出生后CT及MRI结果显示,囊性成分占寄生胎50%以上者可选择微创手术,用腹腔镜探查肿块位置后,用穿刺针吸净囊液,再剥离周围囊膜,将肿块从脐部戳卡孔取出。无论是常规开腹手术还是微创手术,都应充分暴露手术视野,辨认供应血管,同时还需要完整切除寄生胎及囊膜,本组中有2例可见肠系膜上动脉分支血管进入病灶,1例由腹主动脉分支供血。回顾文献也证实,寄生胎供血血管多来源于腹主动脉或肠系膜上动脉分支。有文献报道肿块未完整切除可导致术后复发恶性肿瘤,因此有必要术后长期随访,定期进行影像学和血生化检查[14]。Hoeffel[10]回顾了87例寄生胎病例资料,指出寄生胎无大脑和心脏,但几乎所有胎儿都存在椎骨和四肢(91%和82.5%),且下肢比上肢发达。在寄生胎中相对不常发现中枢神经系统(55.8%)、胃肠道(45%)、血管(40%)或泌尿生殖道(26.5%)。寄生胎中发现心脏、肺、肾上腺、胰腺、脾脏和淋巴结的更少,但也有少许病例报道[3, 9]。本组病例9例寄生胎均无大脑和心脏,可见椎体、长骨或肢芽,其中2例病理检查发现肠管组织。
五、结论综上所述,寄生胎一经诊断需尽早治疗,产前超声可以作为产前诊断寄生胎的重要影像学技术,通过动态观察胎儿腹部寄生胎的变化并做出相应的对策,对产前咨询具有重要指导意义,同时对于鉴别寄生胎与畸胎瘤至关重要。产后对胎儿进行X线、CT、MRI检查可以进一步证实产前诊断,为产后及时处理病情提供准备时间。根据患者腹腔内寄生胎的大小以及囊实性比例,可以根据情况选择微创手术切除寄生胎,减小传统开放手术对患者的伤害,易于术后恢复。
| [1] |
Tiwari C, Shah H, Kumbhar V, et al. Fetus in fetu: two cases and literature review[J]. Dev Period Med, 2016, 20(3): 174-177. |
| [2] |
Hong SS, Goo HW, Jung MR, et al. Fetus in fetu: three-dimensional imaging using multidetector CT[J]. AJR Am J Roentgenol, 2002, 179(6): 1481-1483. DOI:10.2214/ajr.179.6.1791481 |
| [3] |
龙白果, 王玲, 黎玲玲, 等. 产前超声诊断胸颈口腔寄生胎伴心脏结构1例[J]. 中华超声影像学杂志, 2018, 27(6): 478. Long BG, Wang L, Li LL, et al. Prenatal ultrasonic diagnosis of fetus in fetu with cardiac structure in chest, neck and mouth: one case report[J]. Chin J Ultrasonography, 2018, 27(6): 478. DOI:10.3760/cma.j.issn.1004-4477.2018.06.004 |
| [4] |
刘登辉, 肖雅玲, 李勇, 等. 小儿肠系膜寄生胎1例[J]. 临床小儿外科杂志, 2017, 16(4): 414-415. Liu DH, Xiao YL, Li Y, et al. Fetus in fetus of pediatric mesentery: one case report[J]. J Clin Ped Sur, 2017, 16(4): 414-415. DOI:10.3969/j.issn.1671-6353.2017.04.025 |
| [5] |
仇利. 胎儿骶尾部寄生胎合并畸胎瘤1例[J]. 中国介入影像与治疗学, 2016, 13(6): 388. Qiu L. Sacrococcygeal parasitic fetus plus teratoma in fetus: one case report[J]. Chin J Interv Imaging Ther, 2016, 13(6): 388. DOI:10.13929/j.1672-8475.2016.06.017 |
| [6] |
Miura S, Miura K, Yamamoto T, et al. Origin and mechanisms of formation of fetus-in-fetu: two cases with genotype and methylation analyses[J]. Am J Med Genet A, 2006, 140(16): 1737-1743. DOI:10.1002/ajmg.a.31362 |
| [7] |
Lee SY, Ng WT, Yan KW, et al. Case report of fetus-in-fetu diagnosed in a neonate with trisomy 21[J]. Pediatr Int, 2002, 44(2): 189-191. DOI:10.1046/j.1328-8067.2001.01515.x |
| [8] |
Hing A, Corteville J, Foglia RP, et al. Fetus in fetu: molecular analysis of a fetiform mass[J]. Am J Med Genet, 1993, 47(3): 333-341. DOI:10.1002/ajmg.1320470308 |
| [9] |
Ji Y, Chen S, Zhong L, et al. Fetus in fetu: two case reports and literature review[J]. BMC Pediatr, 2014, 14: 88. DOI:10.1186/1471-2431-14-88 |
| [10] |
Hoeffel CC, Nguyen KQ, Phan HT, et al. Fetus in fetu: a case report and literature review[J]. Pediatrics, 2000, 105(6): 1335-1344. DOI:10.1542/peds.105.6.1335 |
| [11] |
李继亮, 杨昌义, 田茂尧, 等. 《请您诊断》病例65答案: 腹膜后两具寄生胎[J]. 放射学实践, 2012, 27(7): 813-814. Li JL, Yang CY, Tian MY, et al. Answer to Case 65 of "Disease Diagnosing": two retroperitoneal fetus-in-fetuses[J]. Radiol Practice, 2012, 27(7): 813-814. DOI:10.13609/j.cnki.1000-0313.2012.07.019 |
| [12] |
Ji Y, Song B, Chen S, et al. Fetus in fetu in the scrotal sac: case report and literature review[J]. Medicine (Baltimore), 2015, 94(32): e1322. DOI:10.1097/MD.0000000000001322 |
| [13] |
Taher HMA, Abdellatif M, Wishahy AMK, et al. Fetus in fetu: lessons learned from a large multicenter cohort study[J]. Eur J Pediatr Surg, 2020, 30(4): 343-349. DOI:10.1055/s-0039-1698765 |
| [14] |
Hopkins KL, Dickson PK, Ball TI, et al. Fetus-in-fetu with malignant recurrence[J]. J Pediatr Surg, 1997, 32(10): 1476-1479. DOI:10.1016/s0022-3468(97)90567-4 |
 2021, Vol. 20
2021, Vol. 20


