2. 浙江大学医学院附属儿童医院体外循环及生命支持科(浙江省杭州市, 310052)
2. Department of Extracorporeal Circulation & Life Supports, The Children's Hospital, Zhejiang University School of Medicine, Hangzhou 310052, China
体外膜肺氧合(extracorporeal membrane oxygenation, ECMO)是一种有创的高级生命支持技术, 可明显改善可逆性严重心肺衰竭患儿的存活率, 目前国内已积极开展。ECMO应用的第一步需建立有效的循环通道, 因小儿股动静脉特殊解剖, ECMO治疗小儿重症疾病多数采用颈动脉和颈内静脉插管。但颈部血管存在解剖变异或在紧急心肺复苏胸外按压(cardiopulmonary resuscitation, CPR)下存在插管困难等情况, 故需要熟练的技术才能建立有效的循环通道。本研究回顾分析了2009年11月至2019年2月在浙江大学医学院附属儿童行颈部插管建立ECMO患儿的临床资料, 总结经验如下。
材料与方法 一、临床资料回顾分析2009年11月至2019年2月在浙江大学医学院附属儿童医院经右侧颈部插管行ECMO治疗的重症患儿70例, 其中男童39例, 女童31例, 疾病类型包括暴发性心肌炎30例, 呼吸衰竭21例, 膈疝6例, 肺动脉高压4例, 其他为脓毒血症、大面积烧伤、脑死亡患儿。有9例(27.1%)死亡。70例ECMO治疗患儿的年龄、体重、病种、ECMO持续时间、并发症以及转归情况见表 1、表 2。
| 表 1 70例ECMO患儿一般资料 Table 1 General profiles of 70 ECMO children |
|
|
| 表 2 70例ECMO患儿疾病类型分布情况 Table 2 Disease distribution of 70 ECMO children |
|
|
1.插管前准备:包括人员(固定外科插管医师、灌注师、ICU医师及护士)、设备(合适的导管、体外膜肺、按压板等)、体位(仰卧位、头朝向左侧并颈部后方加垫能清晰显示右侧胸锁乳突肌、头侧靠近病床顶端)以及药物(强心药、镇痛镇静药)。
2.插管:于充分镇静、镇痛、肌松及呼吸机支持下, 选择右侧胸锁乳突肌旁2~3 cm横切口, 分离皮下组织, 于胸锁乳突肌中部钝性分开肌肉组织, 无需切断肌肉组织, 可见颈内静脉, 用组织剪分离颈内静脉后, 于颈内静脉内侧可见迷走神经和颈动脉, 避免损伤神经组织, 再予组织剪分离颈动脉, 结扎血管的远心端并固定, 近心端套线备用。置管前长度定位为:动脉下端定位于胸骨角上方0.5 cm, 静脉下端定位于胸肋角, 定位后在插管上做相应标记。插管前肝素确认, 血管近心端切开后置入导管至相应标记处, 并予以套线固定。
3.插管后转机:应充分确认动静脉连接无误后开始运转ECMO, 并充分止血, 防止术后渗血, 观察流量是否满意以及患儿生命体征, 同时行B超或X线检查定位插管位置无误后固定ECMO插管, 防止长时间ECMO后管道位置变化。
4.特殊情况下插管:CPR下颈动静脉插管时尽量用剪刀分离, 少用电刀分离, 边按压边分离, 插管时需停止按压, 同时注意表浅静脉出血; 新生儿血管细, 插管时避免暴力, 采用螺旋式进管, 防止血管撕裂; 血管畸形置管时插管头端进入后不能进入右心房, 可再往近心端分离, 通过锁骨下静脉插管; 原有颈内静脉中心置管再置管, 可以拔出颈内静脉置管再置管或者通过颈内置管分离颈内静脉再置管。
5. ECMO撤离的拔管处理:ECMO管理人员确认患儿符合脱离ECMO指征后, 充分麻醉后剪除所有缝线, 吸除血凝块, 剪断结扎线, 于ECMO停机后, 将插管拔出, 同时用丝线双重结扎动脉静脉近心端, 碘伏反复冲洗创面, 剪除皮肤及皮下坏死组织, 分层缝合伤口。
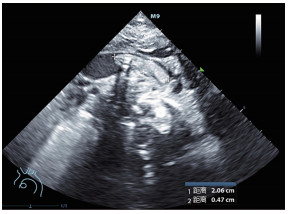
结果70例行右侧颈部插管ECMO治疗的患儿中, 1例颈动脉缺如转腋动脉插管, 2例颈动脉插管失败后转股动脉和腋动脉插管, 其余患儿均插管成功。3例因静脉狭窄扩大切口远端插管, 1例新生儿静脉撕裂扩大切口远端插管, 18例在准备和建立ECMO过程中突发心搏骤停, 在CPR 5~30 min的同时行体外膜肺氧合插管(extracorporeal membrane oxygenation, ECMO-CPR)。1例术后出现声音嘶哑、呛咳, 随访2年后好转但未恢复正常, 考虑治疗插管时损伤迷走神经; 1例动脉插管过深至左室, 导致左室功能不全以及心律失常, 调整后好转; 1例静脉插管过深在心房内打折, 调整后位置正常; 1例动脉插管末端出现血栓(图 1), 予以更换动脉插管以及溶栓后血栓消失, 未见明显后遗症; 3例切口创面渗血, 予以重新清创缝合后好转。
|
图 1 主动脉弓血栓形成 Fig.1 Thrombosis of aortic arch |
ECMO能挽救严重心肺功能衰竭的生命, 其主要有两种支持模式, 即静脉-静脉转流模式和动脉-静脉转流。建立ECMO常用置管通路是颈总动脉和颈内静脉、股动静脉以及主动脉右心房。对于儿童ECMO的建立大部分采用颈部插管, Johnson等[1]发现64%的儿童ECMO建立采用颈总动脉和颈内静脉插管。股动静脉插管主要由于不能选择大的动脉插管, 易致远端肢体缺血, 从而达不到流量要求, 不适合5岁以下儿童[2, 3]。由于股动静脉离胸部按压区远, 故在CPR时可优先选择股动静脉插管。颈部插管方式可以通过切开血管插管以及经皮血管穿刺插管。切开血管插管相对安全有效, 但创伤大、切口长; 经皮血管插管创伤小且瘢痕小, 但存在血肿以及假性动脉瘤的风险。本组患儿均采用切开血管插管, 并且由固定的外科医生插管。有学者认为撤离ECMO后颈部动脉修补和结扎在脑部并发症上没有明显差别, 颈部血管结扎不会增加颅脑损伤的风险[4-6]。也有学者认为颈部插管存在颅脑损伤风险, 还有待于进一步研究证实[7-9]。本组患儿均在撤机后行颈部血管结扎, 未予以修补, 也有部分学者采用该技术[10]。
小儿颈部血管解剖结构存在特殊性, 特别是新生儿颈部血管纤细易撕裂可致大出血。而ECMO建立的第一步需要快速有效地建立循环通道, 因此熟悉小儿颈部血管特殊性以及熟练掌握插管技术非常重要。在分离颈部血管时无需切断胸锁乳突肌, 减少对颈部肌肉的影响, 钝性分开胸锁乳突肌中间纤维组织即可见颈部血管。进一步分离时需注意避开迷走神经, 建议多使用剪刀进行分离, 特别是对正在行CPR的患儿, 由于颈部离胸部按压处近, 胸廓按压会影响颈部血管分离, 并且按压会导致颈内静脉及浅表静脉曲张明显, 如果此时使用电刀分离血管更容易导致神经损伤和血管破裂。本文中1例撤离ECMO后出现声音嘶哑, 喝水呛咳, 主要由于早期在ECMO-CPR时频繁使用电刀导致迷走神经损伤。
插管直径的选择对于颈部插管非常重要。如果直径较小可导致建立ECMO后流量达不到预期, 如果直径过大会增加插管难度同时增加血管撕裂的可能性, 因此应根据患儿体重和血管大小选择相应的插管直径。插管时需要调整插管与血管的角度, 尽可能使插管与血管的交角为零, 同时需要分离相应血管的长度>1.5 cm, 顺着血管的走向送管, 送管避免牵拉血管导致血管扭曲, 遇到阻力切忌强行送管, 可以尝试螺旋式进管或者先退管后再送管, 如果还是不能顺利到达相应位置, 建议更换直径更小的管道, 同时需要B超排除是否存在血管畸形[11, 12]。对于新生儿ECMO插管过程需要更加谨慎, 本组1例新生儿先天性膈疝患儿静脉插管时遇到阻力后再用力后出现静脉撕裂, 往近心端扩大切口再次分离静脉后顺利插管。
血管插管深度关系到ECMO转机的流量, 理想的动脉插管深度是至主动脉弓与无名动脉交界处, 静脉插管下端至右心房与下腔静脉交界处。动脉插管过深至升主动脉则可致心室后负荷增加, 增加心脏负担; 如至左心室则可致心律失常, 从而影响心功能。本组1例患儿因为早期插管后未能及时复查心脏彩超而导致术后出现持续心律失常和左心功能不全, 后调整动脉插管位置后心律失常立即好转。动脉插管如在无名动脉与主动脉弓开口上方接近右锁骨下动脉时, 会造成ECMO血流优势灌注右上肢而致全身灌注不足。静脉插管过深或过浅均会导致静脉回流不佳而影响ECMO回流障碍。因此, ECMO插管前需确认插管的深度, 动脉下端以胸骨角为标志, 静脉下端以胸骨下角为标志, 置管后需复查心脏彩超或者胸片以明确插管深度。
ECMO撤离时拔管应彻底清理切口周围血块, 去除坏死组织, 予结扎血管近心端。部分ECMO患儿转机时间长, 周围组织粘连紧密, 血管近心端原结扎处缺血坏死易造成出血, 需仔细分离, 必要时在近心端予以缝扎处理。有文献报道ECMO撤离颈部拔管后3周出现无名动脉假性动脉瘤, 并且压迫气管, 考虑动脉插管时损伤血管内膜, 从而形成假性动脉瘤, 需要急诊手术切除, 本组未见此类并发症[13]。
总之, 右侧颈动脉、颈内静脉切开插管在小儿ECMO治疗中是安全有效的, 但需要固定的外科操作医师, 并熟练掌握各种插管技术, 防止插管并发症发生。
| [1] |
Johnson K, Jarboe MD, Mychaliska GB, et al. Is there a best approach for extracorporeal life support cannulation:a review of the extracorporeal life support organization[J]. J Pediatr Surg, 2018, 53(7): 1301-1304. DOI:10.1016/j.jpedsurg.2018.01.015 |
| [2] |
Garcia AV, Jeyaraju M, Ladd MR, et al. Survey of the American Pediatric Surgical Association on cannulation practices in pediatric ECMO[J]. J Pediatr Surg, 2018, 53(9): 1843-1848. DOI:10.1016/j.jpedsurg.2017.11.046 |
| [3] |
Kurkluoglu M, Hynes CF, Alfares FA, et al. Choice of peripheral venoarterial extra-corporeal membrane oxygenation cannulation site in patients above 15 kilograms[J]. J Card Surg, 2015, 30(5): 461-465. DOI:10.1111/jocs.12538 |
| [4] |
Duggan EM, Maitre N, Zhai A, et al. Neonatal carotid repair at ECMO decannulation:patency rates and early neurologic outcomes[J]. J Pediatr Surg, 2015, 50(1): 64-68. DOI:10.1016/j.jpedsurg.2014.10.029 |
| [5] |
应力阳, 熊启星, 叶莉芬, 等. 小儿右侧颈动、静脉体外膜肺氧合致颅脑损伤多因素分析[J]. 中华小儿外科杂志, 2016, 37(6): 405-410. Ying LY, Xiong QX, Ye LF, et al. Multi-factorial analysis of cerebral injury in children with a ligation of right carotid artery after extracorporeal membrane oxygenation[J]. Chin J Ped Surg, 2016, 37(6): 405-410. DOI:10.3760/cma.j.issn.0253-3006.2016.06.002 (in Chinese) |
| [6] |
Henzler C, Zöllner FG, Weis M, et al. Cerebral perfusion after repair of congenital diaphragmatic hernia with common carotid artery occlusion after ECMO therapy[J]. In Vivo, 2017, 31(4): 557-564. DOI:10.21873/invivo.11094 |
| [7] |
Teele SA, Salvin JW, Barrett CS, et al. The association of carotid artery cannulation and neurologic injury in pediatric patients supported with venoarterial extracorporeal membrane oxygenation[J]. Pediatr Crit Care Med, 2014, 15(4): 355-361. DOI:10.1097/PCC.0000000000000103 |
| [8] |
Hervey-Jumper SL, Annich GM, Yancon AR, et al. Neurological complications of extracorporeal membrane oxygenation in children[J]. J Neurosurg Pediatr, 2011, 7(4): 338-344. DOI:10.3171/2011.1.PEDS10443 |
| [9] |
O'Brien, Nicole F, Hall MW. Extracorporeal membrane oxygenation and cerebral blood flow velocity in children[J]. Pediatric Critical Care Medicine, 2013, 14(3): e126-e134. DOI:10.1097/pcc.0b013e3182712d62 |
| [10] |
Ellis WC, Scafer M, Barrett CS, et al. Vascular anatomical considerations and clinical decision making during insertion of the Avalon Elite Dual Lumen single-site veno-venous ECMO cannula in children weighing less than 20 kg[J]. Perfusion, 2019, 34(4): 267-271. DOI:10.1177/0267659118815104 |
| [11] |
Lamers LJ, Rowland DG, Seguin JH, et al. The effect of common origin of the carotid arteries in neurologic outcome after neonatal ECMO[J]. J Ped Surg, 2004, 39(4): 532-536. DOI:10.1016/j.jpedsurg.2003.12.005 |
| [12] |
Murthy S, MacDonald C, Honjo O, et al. Innominate artery aneurysm after cannulation for extracorporeal membrane oxygenation via the right carotid artery[J]. Intensive Care Med, 2013, 39(11): 2038-2039. DOI:10.1007/s00134-013-3070-1 |
| [13] |
Jacobs JP, Goldman AP, Cullen S, et al. Carotid artery pseudoaneurysm as a complication of ECMO[J]. Ann Vasc Surgery, 1997, 11(6): 630-633. DOI:10.1007/s100169900102 |
 2020, Vol. 19
2020, Vol. 19


