2. 滁州市第一人民医院儿外科(安徽省滁州市, 239000)
2. Department of Pediatric Surgery, The First People's Hospital of Chuzhou, Chuzhou, 239000, China
儿童骨髓炎主要发生于长骨骨骺端, 多为血源性感染。手和足肢体远端骨髓炎虽然不常见, 但常与周围软组织感染有关, 特别是在穿透性创伤后[1]。如果感染没有得到有效控制, 病程迁延形成慢性骨髓炎, 病灶及其周围血供被破坏, 生物膜形成, 骨质大量流失, 可进一步形成死骨, 最后造成永久的骨质缺损[2]。本文回顾性分析2015年1月至2019年1月由浙江大学医学院附属儿童医院收治的肢体远端骨髓炎患儿临床资料, 对其临床表现、诊治过程及预后进行总结和分析。
材料与方法 一、临床资料2015年1月至2019年1月共收治18例肢体远端骨髓炎患儿, 其中男童10例, 女童8例。年龄1岁6个月至12岁2个月, 平均93.1个月。病灶位于手部者7例, 其中4例位于左手, 3例位于右手; 病灶位于足部者11例, 其中1例位于左足, 10例位于右足。发病前有明确外伤史13例:铁钉或木刺等尖锐物扎入皮肤2例, 刀割伤或门等夹伤肢体致开放性损伤9例, 机器绞伤伴开放性骨折1例, 拔倒刺引发甲沟炎1例; 另5例患儿未诉有明确外伤史。无外伤史病例的临床表现为发热、肢体局部红肿、疼痛、相邻关节僵硬, 入院前病程5~10 d, 平均8.4 d。有外伤史病例中, 6例病程为7~20 d, 平均12.7 d, 临床表现为肢体局部红肿、疼痛、相邻关节僵硬; 7例病程为1~12个月, 平均3.6个月, 除上述临床表现外, 还有局部皮肤破溃、窦道形成、持续液体渗出等体征。
二、实验室和影像学检查18例患儿入院后完善血常规、超敏C反应蛋白、红细胞沉降率、血培养和创面标本培养等实验室检查。同时在门诊或住院部完善X线和MRI等影像学检查。骨髓炎典型的X线检查表现为骨质形态不规则, 骨密度减低, 周围软组织肿胀, 部分患儿显示骨质破坏, 甚至骨质缺损; MRI检查表现为软组织肿胀, 骨质改变为片状的T1WI呈低或稍低信号, T2WI呈高信号。
三、治疗方法结合患儿外伤史、临床症状、体征、X线和MRI检查, 诊断为骨髓炎。患儿一经确诊, 给予足量、广谱抗生素治疗, 并根据药敏结果调整用药。住院期间以静脉用药为主, 出院后改口服, 总疗程6~8周。住院期间7例患儿保守治疗, 11例行手术治疗, 手术方法主要选择病灶彻底清创、骨开窗引流、真空封闭引流(vacuum sealing drainage, VSD)负压吸引术。
结果 一、实验室检查结果18例患儿中8例白细胞和中性粒细胞绝对值较正常值升高, 10例红细胞沉降率高于正常值。3例血培养结果阳性, 均为金黄色葡萄球菌。11例手术中留取创面标本, 其中10例培养结果阳性:包括7例金黄色葡萄球菌感染, 2例铜绿假单胞菌感染, 1例化脓性链球菌A感染(表 1)。
| 表 1 18例手和足骨髓炎病灶分布及临床资料 Table 1 Distribution and clinical data of 18 cases of hand and foot osteomyelitis |
|
|
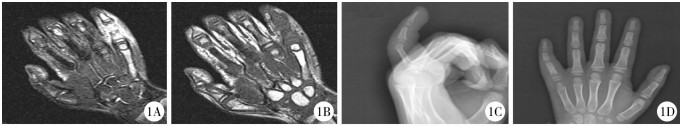
4例患儿入院前病程少于10 d, X线检查显示骨质无明显改变, 仅周围软组织稍肿胀; 其余14例X线检查显示骨质形态不规则, 骨密度减低, 周围软组织肿胀, 部分显示骨质破坏, 甚至骨质缺损。MRI检查均表现为软组织肿胀, 骨质改变为片状的T1WI呈低或稍低信号, T2WI呈高信号, 在脂肪抑制序列更明显(图 1、图 2)。
|
图 1 左手小指骨髓炎 Fig.1 Left hand pinky osteomyelitis A:MRI T1像, 小指指骨呈高信号, 其余指骨低信号; B:MRI T2像, 小指指骨呈低信号, 其余指骨呈高信号; C-D:X线表现为小指指骨骨密度不均, 骨质破坏 |
|
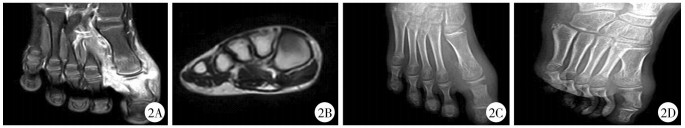
图 2 右足踇趾骨髓炎 Fig.2 Right foot toe osteomyelitis A:MRI T1像, 踇趾趾骨呈高信号, 其余趾骨呈低信号; B:MRI T2像, 踇趾趾骨呈低信号, 其余趾骨呈高信号; C-D:X线表现为踇趾趾骨骨密度不均, 骨质破坏 |
7例患儿经保守治疗, 11例行手术治疗。6例足跗骨骨髓炎患儿行病灶彻底清创、骨开窗引流、VSD负压吸引术。一次VSD负压吸引引流约7 d, 拆除后查看创面情况, 如果没有大片坏死组织和脓性渗出, 可以定期换药, 待创面新鲜肉芽组织生成后再行二期缝合, 缝合时注意清除死腔。如果拆除VSD负压吸引装置发现创面不理想, 继续清创加VSD负压吸引引流。其余5例手指和足趾骨髓炎患儿, 因VSD负压吸引装置安装维持困难, 仅行病灶彻底清创、骨开窗引流术, 定期创面换药。7例因入院前病程超过1个月, 局部皮肤已破溃, 持续液体渗出, 影像学检查死骨形成, 手术时将死骨彻底清除。
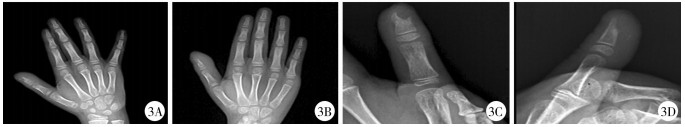
所有患儿经治疗后临床症状和体征得到改善:局部红肿消退, 肢体疼痛感消失, 无液体渗出, 创面愈合良好。出院后门诊或电话随访, 随访时间5个月至4年, 其中5例失访, 13例临床症状和体征消失, 未见复发, 影像学复查提示骨质改变好转。但随访中发现3例手指外观畸形, 即手指短缩或不正常弯曲, 其中2例手指有麻木感, 手指灵活性降低, X线检查显示指骨部分缺失(图 3)。
|
图 3 右手拇指骨髓炎 Fig.3 Right thumb osteomyelitis A-B:X线, 拇指远节骨密度不均匀, 骨质破坏; C-D:3个月后复查X线, 拇指远节骨质缺损 |
儿童手和足肢体远端骨髓炎的发生更多与周围软组织感染有关, 入院前常常有肢体外伤史。儿童由于缺乏对危险的判断和认知, 手和足经常接触危险事物而造成损伤。如果家长未予重视及时就医, 肢体远端软组织可发生感染, 引起骨髓炎。本组18例病例中, 13例患儿有明确的外伤史。
有外伤史, 患儿肢体远端出现红肿、疼痛, 或伴有脓性渗出, 病理超过7 d时, 应警惕骨髓炎的风险。尽早检查血常规、超敏C反应蛋白、血沉和血培养加药敏(最好在未使用抗生素前), 同时行X线和MRI检查[4]。手和足肢体远端骨髓炎早期诊断不易, 实验室检查结果常为阴性, 即使创面标本培养也只有约50%的病例能检查出病原菌[5]。X线是临床上最常用的影像学检查, 易操作且成本低, 但是出现骨质密度不均匀、片状高密度影等征象时通常感染已发作10~14 d[6]。而MRI通常在感染发作3~5 d内就可检测到骨髓炎样改变, 其敏感性和特异性高达90%。既往外伤史、临床症状和体征结合MRI检查结果能提高早期肢体远端骨髓炎的诊断[6]。
目前关于治疗骨髓炎的最佳抗生素种类、途径和持续时间仍没有统一的认识。但大多数研究认为骨髓炎的治疗疗程大约为6周[7]。细菌培养和药敏试验对抗菌药物的选择具有重要的指导意义。研究表明葡萄球菌仍然是骨髓炎的主要致病菌, 而近年来革兰氏阴性菌感染呈增长趋势, 包括铜绿假单胞菌、大肠埃希菌和鲍曼不动杆菌等[8]。Taylor等[9]研究发现, 骨髓炎感染与生物膜密切相关, 生物膜可以增强致病菌的活力和提高致病菌对抗生素的抵抗力, 使抗生素的杀菌效果欠佳, 治疗过程漫长, 感染反复[10]。同时致病菌在生物膜内分泌相关可溶性因子, 破坏正常成骨和破骨代谢平衡, 加速骨溶解, 从而破坏骨质, 造成死骨形成和骨缺损[11]。万古霉素和美罗培南能有效抑制、破坏生物膜[12]。目前临床上针对革兰氏阴性菌感染的骨髓炎, 首选美罗培南; 对革兰氏阳性菌感染的骨髓炎, 采用万古霉素或利奈唑胺的治疗效果最佳[13]。
手和足肢体远端骨髓炎是否需要手术?本研究的经验, 有以下情况者需行手术治疗:①肢体持续疼痛难忍, 影响睡眠; ②影像学检查提示骨膜掀起, 骨膜下积液或骨质破坏严重, 甚至死骨形成; ③应用抗生素治疗后临床症状、体征以及实验室检查结果无明显改善; ④病程迁延超过1个月, 局部皮肤破溃, 伴液体渗出或窦道形成。VSD负压吸引技术在骨髓炎治疗中已得到广泛应用, 其在感染控制和创面愈合等方面较传统灌洗引流优势明显[14]。故建议儿童负压维持在0.01 MPa左右。VSD负压吸引装置一般7 d左右需拆除或更换。
儿童肢体远端急性骨髓炎如果缺乏正规的治疗, 很多会转变为慢性骨髓炎。而慢性骨髓炎的并发症较其本身更可怕, 主要包括:皮肤软组织缺损、肢体外观畸形(如手指短缩或弯曲)、肢体灵活性降低、感觉异常、骨缺损、窦道形成和反复感染[15]。其病情复杂, 病程漫长, 容易复发。针对肢体远端慢性骨髓炎, 建议在清除骨髓炎病灶, 修复病灶缺损创面的同时能重建运动功能和感觉功能[16]。手术方式采用扩大清创、彻底清除病灶, 辅以载抗生素硫酸钙人工骨填充植入, 软组织缺损予一期皮瓣移植修复。Mckee等[17]研究表明, 在治疗慢性骨髓炎中, 使用抗生素浸渍的可吸收骨替代物(妥布霉素浸渍的医用硫酸钙), 相当于根除感染的手术治疗, 并且可以减少随后的外科手术次数。
综上所述, 儿童手和足肢体远端骨髓炎大部分有明确外伤史, 造成局部感染, 进一步引起骨髓炎。因此, 对于有外伤史、肢体远端红肿痛和活动受限、病程超过一周的患儿, 应引起重视, 需进一步行X线和MRI检查, 明确是否存在骨髓炎。骨髓炎早期的诊治对患儿的预后非常重要, 如不能早期诊断、早治疗, 将形成慢性骨髓炎, 后期常常存在骨质破坏, 甚至造成永久的骨质缺损, 引起肢体畸形和感觉活动异常等并发症。
| [1] |
Reilly KE, Linz JC, Stern PJ, et al. Osteomyelitis of the tubular bones of the hand[J]. J Hand Surg Am, 1997, 22(4): 644-649. DOI:10.1016/S0363-5023(97)80122-0 |
| [2] |
El-Rosasy MA. Ilizarov treatment for pseudarthrosis of the tibia due to haematogenous osteomyelitis[J]. J Pediatr Orthop B, 2013, 22(3): 200-206. DOI:10.1097/BPB.0b013e328360268b |
| [3] |
Lee R, Lee HY, Kim JH, et al. Acute osteomeylitis in the hand due to dog bite injury:a report of 3 cases[J]. Arch of Plast Surg, 2017, 44(5): 444-448. DOI:10.5999/aps.2017.44.5.444 |
| [4] |
Chen WL, Chang WN, Chen YS, et al. Acute community-acquired osteoarticular infections in children:high incidence of concomitant bone and joint involvement[J]. J Microbiol Immunol Infect, 2010, 43(4): 332-338. DOI:10.1016/S1684-1182(10)60051-5 |
| [5] |
Cassat JE, Skaar EP. Recent advances in experimental models of osteomyelitis[J]. Expert Rev Anti Infect Ther, 2013, 11(12): 1263-1265. DOI:10.1586/14787210.2013.858600 |
| [6] |
Pineda C, Espinosa R, Pena A. Radiographic imaging in osteomyelitis:the role of plain radiography, computed tomography, ultrasonography, magnetic resonance imaging, and scintigraphy[J]. Semin Plast Surg, 2009, 23(2): 80-89. DOI:10.1055/s-0029-1214160 |
| [7] |
Lazzarini L, Lipsky BA, Mader JT. Antibiotic treatment of osteomyelitis:what have we learned from 30 years of clinical trials?[J]. Int J Infect Dis, 2005, 9(3): 127-138. DOI:10.1016/j.ijid.2004.09.009 |
| [8] |
Carvalho VC, Oliveira PR, Dal-Paz K, et al. Gram-negative osteomyelitis:clinical and microbiological profile[J]. Braz J Infect Dis, 2012, 16(1): 63-67. |
| [9] |
Taylor PK, Yeung AT, Hancock RE. Antibiotic resistance in Pseudomonas aernginosa biofilms:towards the development of novel anti-biofilm therapies[J]. J Biotechnol, 2014, 191: 121-130. DOI:10.1016/j.jbiotec.2014.09.003 |
| [10] |
Kostakioti M, Hadjifrangiskou M, Hultgren SJ. Bacterial biofilms:development, dispersal, and therapeutic strategies in the dawn of the postantibiotic era[J]. Cold Spring Har Perspect Med, 2013, 3(4): a010306. DOI:10.1101/cshperspect.a010306 |
| [11] |
Beck-Broichsitter BE, Smeets R, Heiland M.Current concepts in pathogenesis of acute and chronic osteomyelitis[J].Curr Opin Infect Dis, 2015, 28(3):240-245.DOI:10.1097.QCO.0000000000000155.
|
| [12] |
Hassan A, Usman J, Kaleem F, et al. Evaluation of different detection methods of biofilm formation in the clinical isolates[J]. Braz J Infeet Dis, 2011, 15(4): 305-311. DOI:10.1016/S1413-8670(11)70197-0 |
| [13] |
Humm G, Noor S, Bridgeman P, et al. Adjuvant treatment of chronic osteomyelitis of the tibia following exogenous trauma using OSTEOSETT:a review of 21 patients in a regional trauma centre[J]. Strategies Trauma Limb Reconstr, 2014, 9(3): 157-161. DOI:10.1007/s11751-014-0206-y |
| [14] |
宋宝健, 王强, 冯伟, 等. 持续冲洗结合负压封闭引流治疗儿童急性血源性骨髓炎[J]. 临床小儿外科杂志, 2017, 16(3): 238-241. Song BJ, Wang Q, Feng W, et al. Efficacy of continuous douche plus vacuum sealing drainage for pediatric acute hematogenous osteomyelitis[J]. J Clin Ped Sur, 2017, 16(3): 238-241. DOI:10.3969/j.issn.1671-6353.2017.03.009 (in Chinese) |
| [15] |
张志强, 张自明. 儿童血源性骨髓炎诊治进展[J]. 国际骨科学杂志, 2017, 38(3): 166-169. Zhang ZQ, Zhang ZM. Progress in diagnosis and treatment of blood-borne osteomyelitis in children[J]. Inter J Orthop, 2017, 38(3): 166-169. DOI:10.3969/j.issn.1673-7083.2017.03.006 (in Chinese) |
| [16] |
俞华军, 黄凯, 马苟平, 等. 踇趾腓侧皮瓣修复拇指骨髓炎病灶清除后皮肤软组织缺损[J]. 中华手外科杂志, 2016, 32(4): 277-279. Yu HJ, Huang K, Ma GP, et al. One-stage surgical treatment for thumb osteomyelitis accompanied with soft tissue defects:free flap transplantation from fibular side of big toe[J]. China J Hand Sur, 2016, 32(4): 277-279. DOI:10.3760/cma.j.issn.1005-054X.2016.04.016 (in Chinese) |
| [17] |
Mckee MD, Li-Bland EA, Wild LM, et al. A prospective, randomized clinical trial comparing an antibiotic-impregnated bioabsorbable bone substitute with standard antibiotic-impregnated cement beads in the treatment of chronic osteomyelitis and infected nonunion[J]. J Orthop Trauma, 2010, 24(8): 483-490. DOI:10.1097/BOT.0b013e3181df91d9 |
 2020, Vol. 19
2020, Vol. 19


