门静脉海绵样变(cavemous transformation of portal vein, CTPV)由Balfour等[1]于1869年首先描述,其发病机制至今不明,大多数学者认为其发生机制为门静脉血流瘀滞、血压升高,而机体为降低门静脉压力,在门静脉周围形成大量侧支血管,从而引发门静脉海绵样变。对于有反复上消化道出血以及脾功能亢进的患者,需手术治疗,手术方法主要包括分流术和断流术[2]。1992年de Ville de Goyet等[3]报告了“肠系膜上静脉-门静脉左主支分流术(Rex手术)”治疗肝外型门静脉高压,此手术方式符合人体生理学特点,被认为是治疗CTPV最为成熟的手术方式。因颈内静脉管径较粗,分支较少,相较于选择门静脉系统血管作为分流血管,选择颈内静脉作为搭桥血管可在一定程度上减少分支点血栓形成,减少术后再次出血的概率。本研究采用颈内静脉作为搭桥血管行Rex手术治疗12例CTPV,取得了良好的临床效果,现总结如下。
材料与方法 一、临床资料收集2015年5月至2018年5月由东莞市儿童医院小儿普外科收治的12例门静脉海绵样变性并门脉高压症患儿作为研究对象,其中男童7例,女童5例,年龄89~180个月,10例有反复上消化道出血病史,其中消化道出血5次及5次以上2例,3~4次5例,3次以下3例;12例均表现为脾功能亢进。12例患儿术前血红蛋白、白细胞以及血小板均有不同程度降低,肝功能各项指标均正常。术前影像学检查提示:食管胃底静脉曲张,门静脉海绵样变,脾脏肿大(表 1)。
|
|
表 1 门静脉海绵样变患儿的临床资料 Table 1 Clinical data of CTPV children |
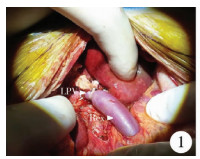
取上腹部弧形切口,长约15 cm,逐层切开各层组织,探查腹腔。取小肠系膜Ⅲ级静脉行静脉插管,测量静脉血压。脐静脉造影观察门静脉肝内部的通畅情况,确定Rex手术的可行性。解剖肝圆韧带,将肝圆韧带游离达门静脉左支远端及通向肝脏Ⅲ、Ⅳ段的分支,如此显露左支的3~4 cm,用小号心耳钳阻断左支及其分支,在与左支的连接处切断肝圆韧带,并向肝中心方向纵行切开,以扩大静脉切口,分离暴露肠系膜上静脉,术中行肝脏活检,取患儿左颈内静脉作间置移植物,取下移植物至于肝素液中留作吻合用,行全身血管肝素化,将移植静脉与门静脉左支作端侧吻合,将移植物与肠系膜上静脉作端侧吻合(图 1),测量门静脉压力,拔管缝扎测量段静脉,予冲洗腹腔,留置腹腔引流管,逐层缝合皮肤。
|
Download:
|
| 图 1 Rex手术过程图 LPV:肝静脉左支;Rex:颈内静脉搭桥 Fig. 1 Process of Rex shunt LPV: left portal vein; Rex: intrajugular vein | |
|
Download:
|
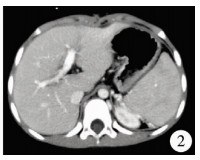
| 图 2 术后CT提示分流血管通畅 Fig. 2 CT: shunting blood vessel patency | |
术后常规行腹部超声检查,主要观察分流血管情况、脾脏大小;定期复查血常规、肝功能等;长期随访患儿生长发育情况。出院后每3个月随访1次,主要行血常规、肝功能以及腹部彩超检查。
四、统计学方法采用SPSS19.0统计软件进行数据整理与分析。对于门静脉压力、血细胞计数、脾脏长度和脾脏厚度等计量资料采用均数±标准差(x±s)表示,手术前后的比较采用配对样本t检验。以P < 0.05为差异有统计学意义。
结 果本组12例患儿术中均采用肠系膜上静脉与门静脉左支搭桥,手术均获得成功。手术时间为380~480 min,平均为(420±33.58)min,术中出血30~150 mL,平均为(76.67±32.85)mL。分流术前测肠系膜上静脉压力为24~37 cm H2O,平均为(32.5±3.7) cm H2O,分流术后降为17~34 cm H2O,平均为(23.5±4.7) cm H2O,分流术前后肠系膜上静脉压力相比,差异有统计学意义(t=5.19,P=0.001)。术后行彩超检查显示分流血管通畅、无狭窄、无回缩。
本组患儿术后随访12~24个月。随访期间患儿影像学检查提示血管吻合口通畅、无狭窄及血栓形成(图 2)。肝功能各项指标均恢复正常。术后复查血细胞计数较术前均有不同程度升高,手术前后白细胞分别为(2.1±0.6)×1012/L和(4.4±2.3)×1012/L,差异有统计学意义(t=3.29,P=0.003);手术前后血红蛋白分别为(65.2±19.5)g/L和(101.2±13.9) g/L,差异有统计学意义(t=5.70,P=0.001);手术前后血小板分别为(70.5±33.1)×109/L和(161.17±66.8)×109/L,差异有统计学意义(t=4.21,P=0.001),见表 2。术后12个月复查脾脏长度、厚度较术前均有缩小,差异有统计学差异(P=0.001),见表 3。随访期间12例患儿均未发生肝性脑病。
|
|
表 2 术前与术后7天血细胞计数比较 Table 2 Comparison of preoperative and postoperative blood cell counts |
|
|
表 3 术前与术后12个月脾脏长度、厚度比较 Table 3 Comparison of splenic length between preoperative and postoperative 12 months |
CTPV由Balfour等[1]于1869年首先描述,其发病机制至今不明,诸多研究认为其可能的发生机制为门静脉血流瘀滞、血压升高,而机体为降低门静脉压力,在门静脉周围形成大量侧支血管。这一代偿性病理改变的意义在于侧支循环血流可绕过阻塞部位而直接汇入肝脏以增加入肝血量,淤塞最终形成门静脉海绵样变。由于门静脉系统压力进行性升高,以致出现食管胃底静脉曲张破裂出血和脾脏肿大、脾功能亢进为主要临床表现的门静脉高压症候群。
CTPV属于肝前型门静脉高压症(extrahepatic portal hypertension, EHPH),常见于儿童,占儿童门静脉高压症的40%左右,其中25% ~40%的患儿可反复出现胃底食管静脉破裂出血,具有危险性大、再出血率高等特点,因此对于此病的诊治一直都是小儿外科的研究重点[4]。随着人类对该疾病的深入研究以及外科技术的发展,CTPV的治疗方向已由原来的控制消化道出血及脾功能亢进逐渐向降低门静脉压、恢复肝脏正常血流灌注、改善肝功能等方面转变。外科治疗CTPV的方法有断流术、各种分流术、联合手术及肝移植术[5]。Rex手术符合患儿生理特点,既降低了门静脉压力,又能保证入肝血流,使静脉血能够入肝,降低肝性脑病的发生率,因此越来越多的医院采用该术式治疗CTPV[6, 7]。肝移植手术是终末期肝病的有效治疗手段,可同时解决肝功能失代偿和门静脉高压等问题,但由于肝源缺乏、费用昂贵而制约了其在临床上应用[8]。
Rex手术的经典术式是在肠系膜上静脉和肝内门静脉左支之间应用颈内静脉进行搭桥,随着治疗经验的积累,该术式逐渐被改进,常使用合适的内脏静脉(如肠系膜下静脉、胃冠状静脉、脾静脉、再通脐静脉、大的结肠静脉等)直接与门静脉左支相连。虽然改良术式只需一个吻合口,简化了手术程序,在一定程度上降低了手术操作的风险,但是相对于颈内静脉而言,内脏静脉较细,分支较多,术后出现血栓、梗阻的概率相应增加[9]。
Rex手术选择合适的分流血管是手术成功的关键。有研究表明只有直径≥ 5 mm的血管才适合做移植血管。李龙等[10]研究发现选择门静脉系统血管作为分流血管直径就算在5 mm以上,也可能发生血栓,导致手术失败,其原因可能与门静脉压力降低导致扩张的分流血管回缩有关。这也是选择门静脉系统血管作为分流血管的弊端之一。我们选择颈内静脉血管是因为其管径较粗,分支较少,可避免分支点血栓形成,同时本研究还发现采用颈内静脉搭桥Rex手术治疗12例CTPV患儿取得了较好的效果。Kim等[11]亦认为分流术后存在较高血栓形成和再出血发生率的重要原因是这些分流术利用继发性扩张的静脉,而非原本较粗的静脉作为分流血管。因此选择颈内静脉作为搭桥血管可以很好地解决这一问题,在一定程度上可以降低分流术后血栓形成和再出血发生率[12]。
虽然说经典的Rex分流术是截取患儿自身一段颈内静脉作为搭桥血管,在一定程度上增加了手术难度,但是由经验丰富的医师进行操作,其术后血栓形成和再出血发生率可大大降低。本组12例患儿均行颈内静脉搭桥Rex手术,手术过程顺利,术后随访患儿未再发生呕血,影像学检查显示分流血管通畅,效果良好。本研究发现分流术后患儿血红蛋白、白细胞、血小板计数升高以及脾脏长度、厚度缩小的原因可能是:分流术后门静脉血流受阻解除,扩张的脾窦缩小,脾内纤维组织增生减少,单核-巨噬细胞增生减少,因此外周血细胞被吞噬数量减少,相应细胞计数随之增加。外周血细胞的增加、脾脏的长度及厚度的缩小也可间接证明分流血管是通畅的[13]。
本研究12例患儿均采用颈内静脉搭桥Rex手术,手术过程顺利,术后随访患儿未再发生呕血。分析其成功原因如下:①颈内静脉管径较粗,平均直径在1 cm以上,并且此管径为颈内静脉真实管径长度,不存在代偿性增粗,因此可以有充分的分流,可尽量减少或避免术后分流血管血栓的形成;②有足够粗的管径是成功的一方面,更重要的是在吻合口的处理上,首先要保证门静脉左支矢状部切开的长度和待吻合血管口径相差不要太大,差距尽量控制在2 mm以内,这样保证血流在搭桥血管内流速相对平稳,减少血栓形成。同样还要保证吻合口处血管内膜对合平整,这对医师技术水平要求较高,可借助手术放大镜进行操作[14]。其次吻合时要保证分流血管的通畅性,不要扭曲、打折; ③12例患儿术前影像学检查均显示门静脉左支开放,无狭窄、变异,这是整个手术可行性的关键及前提;但是,本研究只有12例CTPV患儿,样本量较少,后期需要多中心、大样本量研究进行验证。
综上所述,利用颈内静脉搭桥Rex分流术有一定的手术难度,但其保证了移植血管有足够的管径,且分支少,在一定程度上可降低术后血栓形成和再出血的发生率。由此可见,利用颈内静脉的Rex分流术仍是治疗门静脉海绵样变性的理想术式之一。
| 1 |
Senzolo M, Tibbah J, Cbolongitas E, et al. Transjuguhr intrahepatic portosystemic shunt for portal vein thrombosis with and without cavernous transformation[J]. Aliment Pharmacol Ther, 2006, 23(6): 767-775. DOI:10.1111/j.1365-2036.2006.02820.x. |
| 2 |
刘斐, 王哲, 温哲. Rex分流术治疗小儿肝前性门静脉高压症5例临床分析[J]. 中华肝胆外科杂志, 2016, 22(2): 73-77. DOI:10.3760/cma.j.issn.1007-8118.2016.02.001. Liu F, Wang Z, Wen Z. Rex shunt in pediatric prehepatic portal hypertension:a clinical analysis of 5 cases[J]. Chin J Hepatobiliary Surg, 2016, 22(2): 73-77. DOI:10.3760/cma.j.issn.1007-8118.2016.02.001. |
| 3 |
de Ville de Goyet J, Clapuyt P, Otte JB. Extrahilar mesentericoleft portal shunt to relieve extrahepatic portal hypertension after partial liver transplant[J]. Transplantation, 1992, 53(1): 231-232. |
| 4 |
Dai J, Qi X, Li H, et al. Role of D-dimer in the development of portal vein thrombosis in liver cirrhosis:A Meta-analysis[J]. Saudi J Gastroenterology, 2015, 21(3): 165-174. DOI:10.4103/1319-3767.157567. |
| 5 |
Hneider BL, de Ville de Goyet J, Leung DH, et al. Primary prophylaxis of variceal bleeding in children and the role of MesoRex bypass:Summary of the Baveno Ⅵ Pediatric Satellite Symposium[J]. Hepatology, 2016, 63(4): 1368-1380. DOI:10.1002/hep.28153. |
| 6 |
张金山, 李龙. Rex手术治疗胆总管囊肿术后门静脉海绵样变的应用研究[J]. 临床小儿外科杂志, 2019, 18(12): 1004-1008. DOI:10.3969/j.issn.1671-6353.2019.12.004. Zhang JS, Li L. Efficacy of Rex shunt for portal cavernoma after hepaticojejunostomy in children with choledochal cyst[J]. J Clin Ped Sur, 2019, 18(12): 1004-1008. DOI:10.3969/j.issn.1671-6353.2019.12.004. |
| 7 |
温哲, 张宾宾. 儿童肝前性门静脉高压的术前评估及手术治疗[J]. 临床小儿外科杂志, 2019, 18(12): 994-998. DOI:10.3969/j.issn.1671-6353.2019.12.002. Wen Z, Zhang BB. Preoperative assessments and operations for prehepatic portal hypertension in children[J]. J Clin Ped Sur, 2019, 18(12): 994-998. DOI:10.3969/j.issn.1671-6353.2019.12.002. |
| 8 |
Luo X, Nie L, Zhou B. Transjugular intrahepatic portosystemic shunt for the treatment of portal hypertension in noncirrhotic patients with portal cavernoma[J]. Gastroenterol Res Pract, 2014, 2014: 659-726. DOI:10.1155/2014/659726. |
| 9 |
万岐江, 候蔚蔚, 王忠敏. 经颈静脉肝内门体静脉分流术治疗门静脉高压的临床研究现状与进展[J]. 中国介入影像与治疗学, 2015, 12(3): 186-189. DOI:10.13929/j.1672-8475.2015.03.014. Wan QJ, Hou WW, Wang ZM. Current status and progresses of clinical research of transjugular intrahepatic portosystemic shunt in treatment of portal hypertension[J]. Chin J Interv Imaging, 2015, 12(3): 186-189. DOI:10.13929/j.1672-8475.2015.03.014. |
| 10 |
张金山, 李龙, 刘树立, 等. 小儿肝外门脉高压Rex术后门脉高压复发的临床分析[J]. 中华小儿外科杂志, 2015, 36(12): 894-897. DOI:10.3760/cma.j.issn.0253-3006.2015.12.004. Zhang JS, Li L, Liu SL, et al. Etiology and treatment for recurrent portal hypertension after Rex shunting in children[J]. Chin J Ped Sur, 2015, 36(12): 894-897. DOI:10.3760/cma.j.issn.0253-3006.2015.12.004. |
| 11 |
Kim HB, Pomposelli JJ, Lillehei CW, et al. Mesogonadal shunts for extrahepatic portal vein thrombosis and variceal hemorrhage[J]. Liver Transpl, 2005, 11(11): 1389-1394. DOI:10.1002/lt.20487. |
| 12 |
Di Francesco F, Grimaldi C, de Ville de Goyet J. Meso-Rex bypass-a procedure to cure prehepatic portal hypertension:the insight and the inside[J]. J Am Coll Surg, 2014, 218(2): 23-36. DOI:10.1016/j.jamcollsurg.2013.10.024. |
| 13 |
刘树立, 李龙, 侯文丽, 等. 肠门分流(Rex手术)治疗肝外型门静脉高压的初步研究[J]. 临床小儿外科杂志, 2009, 8(6): 13-16. DOI:10.3969/j.issn.1671-6353.2009.06.005. Liu SL, Li L, Hou WL, et al. Rex shunt for portal hypertension in children with cavernous transformation of portal vein[J]. J Clin Ped Sur, 2009, 8(6): 13-16. DOI:10.3969/j.issn.1671-6353.2009.06.005. |
| 14 |
Rivera J, Fusaro F, de Magnee C, et al. Meso-Rex shunt for immediate portal revascularization in pediatric liver transplantation:first report[J]. Pediatr Transplant, 2012, 16(6): 235-237. DOI:10.1111/j.1399.3046.2011.01576.X. |
 2019, Vol. 18
2019, Vol. 18


