46,XY DSD是指染色体核型为46,XY但性腺性别和(或)表型性别与之不相匹配的一类先天性异常疾病[1]。其临床表现存在较大的个体间异质性, 是一系列难以归类、难以诊断的复杂性疾病。本文从以下几方面就46,XY DSD的内分泌评估和治疗进行探讨, 以期为临床诊治提供参考依据。
一、性腺的胚胎发育在胚胎发育期, 性腺组织中生殖细胞的核型将决定原始性腺组织向睾丸或卵巢分化。正常情况下, 染色体核型为46,XY的人类胚胎在孕第4~5周时就已形成具有双向潜能的尿生殖嵴, 随后在一系列基因(包括SRY、NR5A1、WT1、EMX2、PBX1等)及信号分子的调控下, 原始性腺开始向睾丸分化。直到胚胎发育第7周, 前Sertoli细胞表达SRY并上调SOX9水平, SOX9进一步诱导前Sertoli细胞形成成熟Sertoli细胞, 这个过程可能涉及GATA4、FOG2、NR5A1、WT1等多个基因的共同作用, 同时需要抑制女性生殖道发育的基因共同参与完成。Sertoli细胞形成后诱导Leydig细胞的发育, 在胚胎8~9周Leydig细胞开始产生睾酮和胰岛素样因子3(insulin-like factor 3, INSL3)。睾酮和Sertoli细胞分泌的抗Müllerian管因子(anti-müllerian hormone, AMH)共同导致Müllerian管结构退化, 促进Wolffian管发育为附睾、输精管、精囊;INSL3则促进睾丸的下降。睾酮通过5α还原酶转化为活性更高的双氢睾酮, 二者均作用于雄激素受体, 进而产生一系列生物学效应[2], 最终完成性腺和外生殖器的发育。
二、46,XY DSD病因分类及临床特征诊断方面, 性染色体DSD相对比较容易, 46,XX DSD以先天性肾上腺皮质增生症(congenital adrenal hyperplasia, CAH)为多。相较于前两者, 46,XY DSD遗传背景最为复杂, 诊断及治疗较为困难。不过, 近年来新的诊断技术逐步应用于临床, 46,XY DSD诊断率的精准性得到了大幅提高。任何影响了睾丸分化、睾酮合成或作用的因素, 都可以导致46,XY DSD的形成。46,XY DSD的临床特征及其致病基因见表 1[12, 13]。
|
|
表 1 46,XY DSD睾丸发育不全和雄激素合成或作用障碍的致病基因以及临床特点 Table 1 Pathogenic genes and clinical characteristics of 46, XY DSD patients presenting with testicular hypoplasia or androgen synthesis insufficiently or dysfunction |
对于新生儿和年幼儿存在外生殖器模糊不清、腹股沟包块、阴蒂肥大、阴唇或阴部包块、阴唇融合、尿道口/阴道口异常、小阴茎、隐睾、尿道下裂、家族性尿道下裂、睾丸位置同侧畸形等表现者需疑诊为DSD;约25%的DSD患儿同时还合并身体其他部位畸形, 对于有其他部位畸形者应提高警惕;此外, 对于有家族性不孕不育史、青春期发育延迟、外生殖器手术治疗、死胎、多次流产史、生殖器表型与染色体核型不一致的新生儿也应怀疑DSD。
对于青春期儿童, 通常出现以下3种情况时需要考虑DSD。一是出现原发性闭经(无论是否有乳房发育);二是社会性别为女性者出现男性化表现(胡须、喉结、变声等);三是社会性别为男性者男性化不足, 出现乳房发育、青春期发育延迟等表现。
四、如何对可疑患儿进行评估 (一) 病史采集包括一般情况(何时发现、有无变化、是否治疗、治疗后反应等), 出生史(尤其关注是否存在难产或出生时窒息抢救史), 听力筛查是否正常;能否识别气味, 有无隐睾手术史及唇腭裂手术修复史, 家族史(有无失盐病史、生长发育情况, 重点关注有无青春期发育延迟、有无嗅觉减退及不孕不育家族史)和母亲妊娠分娩史(有无流产及流产原因), 是否为早产儿, 是否近亲结婚, 母亲孕期有无外源性雌、孕激素接触史, 是否保胎, 是否为辅助生殖人工妊娠及生长和智力情况等。
(二) 体格检查除体态、面容和身材比例外, 此处主要指外生殖器及性腺评估, 包括阴茎、睾丸、尿道、生殖皱褶及会阴的评估, 通常采用Prader分级和外生殖器男性化评分(external masculinization score, EMS)进行评估[14-16]。Prader分级标准根据外阴男性化程度及阴道与尿道汇合点的高度分为Ⅰ~Ⅴ型, 以评估外生殖器的解剖状况(接近正常男性或女性)。EMS是另一个分级系统, 可以提供一个更有识别力、更客观的评估方法。该系统通过对阴唇阴囊融合、小阴茎、尿道口位置、性腺位置和是否存在性腺等进行评价, 以判断外生殖器的男性化水平, 但是该分级系统对于中间型的判定需依据临床经验。对于尿道、生殖皱褶和会阴的评估还需系统记录一系列观察结果:①生殖皱褶融合情况(完全开裂、部分融合、融合);②生殖皱褶/着色/对称情况;③发育不全/生殖皱褶缺失情况;④生殖皱褶与生殖结节转位情况;⑤尿道/会阴口(数量/位置以及之间关系)情况;⑥青春期Tanner分期情况;⑦术后瘢痕情况。近年来, 其他的描述法如测量肛门-生殖器距离(anus genitalia diatance, AGD)和EMS(男性化评分)也开始逐渐受到重视。不同的评测法各有不同的评估优势, 在不同的临床对比研究中可选择不同的方法。AGD是指从肛门中点至阴唇系带后侧(或阴囊-会阴连接处)之间的长度, 是一种非侵袭性的检查方法, 操作简便、可靠。其长度越长提示男性化程度越高, 也提示出生前曾暴露于雄激素。EMS是指综合考虑睾丸位置、尿道口位置和阴茎大小的方法[14]。对于性腺的评估必须记录是否可触及性腺、数目以及位置, 如果在阴唇阴囊褶(生殖皱褶)可以触及到性腺, 提示睾丸组织存在;如果两侧均不能触及性腺, 则需要进行进一步的详细评估。在腹股沟区可触及到单侧卵巢的可能性则很小。
此外, 还需关注患儿整体情况, 如:体型、身高、颜面部畸形(唇腭裂、耳位、眼距、颚弓、色素痣、特殊面容)、异常掌纹、盾状胸、发际、心脏畸形、肾脏畸形、四肢畸形、短指(趾)畸形、骨骼畸形、中线发育缺陷、镜像(连带)运动等。
(三) 内分泌评估包括血糖、电解质测定、基础内分泌激素检测和功能试验评价。尽量采用多种性腺激素基础值评估下丘脑-垂体-性腺轴(Hypothalamus-Pituitary-Gonad Axis, HPG轴)、性腺的不同细胞及垂体其他轴系激素分泌情况。基础激素水平测定包括黄体生成素(LH)、促卵泡素(FSH)、泌乳素(PRL)、孕酮(PGN)、睾酮(T)、双氢睾酮(DHT)、雌二醇(E2)、抗苗勒管激素(AMH)、抑制素B(INH-b)、胰岛素样因子-3(INSL3)、脱氢表雄酮(DHEA)、17-羟孕酮(17-OHP)、促肾上腺皮质激素(ACTH)、皮质醇。
激发试验包括标准绒毛膜促性腺激素(HCG)激发试验、HCG延长试验、戈那瑞林(LHRH)激发试验、尿促性素(HMG)激发试验。HCG激发用于评价睾丸间质细胞功能。有多种方法可行, 我们比较推荐以下两种:①标准HCG激发试验:HCG 1 500 IU/次, 每天1次, 共4次, 第5 d抽血查血清睾酮水平。②HCG延长试验:HCG 1 000 IU/次, 隔日1次, 共10次, 第20 d抽血查血清T水平。血清T≥100 ng/dL认为反应良好, < 100 ng/dL认为反应不良。因为短时间的刺激, 不利于反应迟钝的患儿正确评估。LHRH激发试验:禁水, 抽血查性激素6项, 然后按照每次100 μg/m2的剂量给予戈那瑞林, 加生理盐水2 mL缓慢静脉注射, 并分别在给药后30 min、60 min和90 min各取血2 mL测定LH和FSH, 以协助判定HPG轴是否启动。HMG试验则用于评估卵巢功能。
(四) 影像学检查及性腺活检影像学检查主要包括超声(睾丸、盆腔、子宫、卵巢超声), CT和MRI检查也可用于鉴别苗勒管衍生结构。当性腺性别通过影像学检查仍难以确定时, 可利用腹腔镜检查及组织活检判断是否为卵睾、条索状性腺或发育不良的睾丸。需要强调的是, 腹腔镜检查及组织活检均应以诊断为目的, 尽量避免损伤甚至切除性腺。
(五) 遗传学评估包括染色体核型分析和基因诊断。染色体核型分析是DSD鉴别流程中至关重要的一步, 芝加哥国际共识中对DSD的分类即依赖于染色体核型分析结果, 因此对所有患者, 在初诊时必需行染色体核型分析。
如前所述, DSD病因繁多, 大部分患者仅通过临床表现和常规的辅助检查难以确诊。特别是很多疾病并无高特异性的生物学标志物。近年来, 随着遗传学技术不断进步, 基因检测技术有了长足发展并逐步应用于临床, 对揭示病因、明确诊断和判断预后均起到重要作用。46,XY DSD多由于性腺分化或发育过程中相关基因突变导致, 遗传背景复杂, 涉及基因广泛, 国内外对该组疾病进行了大量深入的研究[17]。至今已明确的与46,XY DSD致病有关的基因包括:WT1、CBX2、NR5A1、SRY、SOX9、MAP3K1、DHH、ARX、TSPYL1、MAMLD1、DMRT、ATRX、DAX1、WNT4、GATA4、ZFPM2、HHAT、DHCR7、LHCGR、StAR、CYP11A1、HSD3B2、CYP17、POR、CYB5A、HSD17B3、SRD5A2、AR、AMH、AMHR等, 这些基因涉及到睾丸的形成和发育、雄激素的合成与转化以及多种激素受体的功能调控。不同致病基因导致的46,XY DSD临床表现、治疗方式有所不同, 尽早明确其分子诊断并给予及时治疗, 对于改善患者的预后及提高生活质量非常重要。此外, 根据不同致病基因的遗传方式, 可对患儿及其父母提供相应的遗传咨询, 为优生优育提供依据。不过遗憾的是, 尽管遗传学技术有了显著的进步, 通过基因分子水平能够明确诊断的患者已经达到一定比例, 基因检测技术在国内的应用也日益广泛。然而此方面的应用规范、遗传咨询范围、伦理行为的界定、人权与法规、未成年保护法的实施、个体器官的拥有和侵犯等等法律问题尚未引起我国相关的医学和法学专家的关注。因此, 此领域的科学发展和随之而来的问题也逐渐凸显, 研究和解决这些问题仍然任重道远。
国家儿童医学中心北京儿童医院内分泌遗传代谢团队对46,XY DSD进行了部分基因研究[4, 18-20], 相关研究有助于提高我们对疾病的认识。但正是由于存在诸多未解决的问题(尤其是法律和伦理问题的争议), 因此在儿科医学处理中以评估为主, 以建议为多。
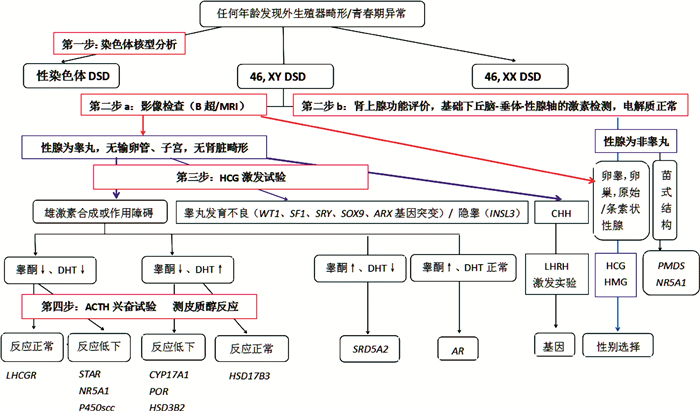
五、如何依据评估结果做出病因诊断临床上, 不同病因导致的46,XY DSD在临床表现上具有很大的重叠, 因此对其进行诊断和鉴别诊断极为重要。在进行详细病史询问及体格检查的基础上, 依据染色体核型分析结果, 确定为46,XY DSD者在接受标准HCG刺激后, 可根据睾酮及其前体物质水平对测定结果进行分类和鉴别, 见图 1[12]。
|
Download:
|
| 图 1 46,XY诊断流程图 注 DSD:性发育异常;CHH:先天性低促性腺激素性性腺功能减退症; PMDS:苗勤管永存综合征。 Fig. 1 | |
对本病的治疗包括以下方面:一是社会性别的选择和判定, 这需要综合考虑患者临床表型的严重程度、自身的心理性别倾向、家庭及社会的认可度等多种因素, 有些患者需进行外生殖器整形术、乳房整形术等以达到符合所选社会性别的目的, 并长期进行激素替代治疗来维持第二性征。其次, 对于性腺发育不全或腹腔内性腺(睾丸未降至正常阴囊内)的患者, 既往文献报道性腺恶变机率增加, 是否需进行性腺切除、手术时机以及方式需要慎重考量。第三, 针对不同类型46,XY DSD的伴随症状, 也需要进行及时的治疗, 本病引起的性别判定困难、排尿异常、第二性征异常、性功能障碍、生育能力下降等因素均可造成患者出现严重的心理障碍, 表现为自信心不足、抑郁、焦虑甚至自杀倾向等, 影响患儿的学习和生活。综合以上观点, 我们认为在临床选择治疗策略时, 应坚持分级和个体化管理。具体如下:(1)风险分级评估:①是否危及生命;②是否影响功能;③是否影响外观;④是否可以等待。(2)治疗分级:①去除危及生命因素(例如休克或肿瘤);②解决和改善功能:首先应保护性腺生殖功能, 其次考虑非生殖功能;③外观修补:择期进行;④坚持保守原则:依据患儿现有的器官组织决定, 不建议早期行性腺摘除手术。对于此类患者的治疗需要内分泌科、妇产科、泌尿外科、整形外科、医学心理科、遗传学科等多学科合作, 共同制定方案使患者最大限度受益, 这也是现今国内外DSD诊疗中所追求的共同目标[12, 21]。
| 1 |
Lee PA, Houk CP, Ahmed SF, et al. Consensus statement on management of intersex disorders.International Consensus Conference on Intersex[J]. Pediatrics, 2016, 118(2): e488-e500. DOI:10.1542/peds.2006-0738. |
| 2 |
Ahmed SF, Bashamboo A, Lucas-Herald A, et al. Understanding the genetic aetiology in patients with XY DSD[J]. Br Med Bull, 2013, 106(1): 67-89. DOI:10.1093/bmb/ldt008. |
| 3 |
Chernin G, Vega-Warner V, Schoeb DS, et al. Genotype/phenotype correlation in nephrotic syndrome caused by WT1 mutation[J]. Clin J Am Soc Nephrol, 2010, 5(9): 1655-1662. DOI:10.2215/CJN.09351209. |
| 4 |
Yanning S, Lijun F, Chunxiu G. Phenotype and molecular characterizations of 30 children from China with NR5A1 mutations[J]. Front Pharmacol, 2018, 9(1): 1-9. DOI:10.3389/fphar.2018.01224. |
| 5 |
Werner R, Merz H, Birnbaum W, et al. 46, XY Gonadal dysgenesis due to a homozygous mutation in Desert Hedgehog (DHH) identified by exome sequencing[J]. J Clin Endocrinol Metab, 2015, 100(7): E1022-E1029. DOI:10.1210/jc.2015-1314. |
| 6 |
Sirisena ND, Mcelreavey K, Baashamboo A, et al. A child with a novel de novo mutation in the aristaless domain of the aristaless-related homeobox (ARX) gene presenting with ambiguous genitalia and psychomotor delay[J]. Sex Dev, 2014, 8(4): 156-159. DOI:10.1159/000365458. |
| 7 |
Ruiz-Arana IL, Hubner A, Cetingdag C, et al. A novel hemizygous mutation of MAMLD1 in a patient with 46, XY complete gonadal dysgenesis[J]. Sex Dev, 2015, 9(2): 80-85. DOI:10.1159/000371603. |
| 8 |
Baxter RM, Arboleda VA, Lee H, et al. Exome sequencing for the diagnosis of 46, XY disorders of sex development[J]. J Clin Endocrinol Metab, 2015, 100(2): E333-E344. DOI:10.1210/jc.2014-2605. |
| 9 |
Machado AZ, Da ST, Frade CE, et al. Absence of inactivating mutations and deletions in the DMRT1 and FGF9 genes in a large cohort of 46, XY patients with gonadal dysgenesis[J]. Eur J Med Genet, 2012, 55(12): 690-694. DOI:10.1016/j.ejmg.2012.07.012. |
| 10 |
Jezela-Stanek A, Fisher C, Szarras-Czqpnik M, et al. X-linked alpha thalassaemia/mental retardation syndrome:a case with gonadal dysgenesis caused by a novel mutation in ATRX gene[J]. Clin Dysmorphol, 2009, 18(3): 168-171. DOI:10.1097/MCD.0b013e32832a9ea5. |
| 11 |
Barbaro M, Oscarson M, Schoumans J, et al. Isolated 46, XY gonadal dysgenesis in two sisters caused by a Xp21.2 interstitial duplication containing the DAX1 gene[J]. J Clin Endocrinol Metab, 2007, 92(8): 3305-3313. DOI:10.1210/jc.2007-0505. |
| 12 |
Ahmed FS, Achermann JC, Arlt W, et al. Society for Endocrinology UK guidance on the initial evaluation of an infant or an adolescent with a suspected disorder of sex development[J]. Clin Endocrinol, 2016, 84(8): 771-788. DOI:10.1111/cen.12857. |
| 13 |
Xiaoya Ren, Di Wu, Chunxiu Gong. A case of Persistent Müllerian Duct Syndrome and the Literature Review[J]. Exp Ther Med, 2017, 14(6): 5779-5784. DOI:10.3892/etm.2017.5281. |
| 14 |
巩纯秀, 李乐乐. 性发育异常的诊疗规程-基于大量临床实践和400余例46, XY性发育异常基因研究[J]. 中华实用儿科临床杂志, 2017, 32(20): 8-12. DOI:10.3760/cma.j.issn.2095-428X.2017.20.001. Gong CX, Li LL. Procedure of Diagnosis and treatment for Disorders of Sex Development[J]. Chin J Appl Clin Pediatr, 2017, 32(20): 8-12. DOI:10.3760/cma.j.issn.2095-428X.2017.20.001. |
| 15 |
巩纯秀, 秦淼, 武翔靓. 儿科内分泌医生对性发育异常患儿的评估和管理[J]. 中华循证儿科杂志, 2014, 9(2): 140-149. DOI:10.3969/j/issn.1673-5501.2014.02.011. Gong CX, Qin M, Wu XY. Evaluation and management of pediatric endocrinologists for children with sexual dysplasia[J]. Chinese Journal of Evidence-Based Pediatrics, 2014, 9(2): 140-149. DOI:10.3969/j/issn.1673-5501.2014.02.011. |
| 16 |
巩纯秀, 秦淼. 儿科内分泌医师对性发育障碍患者处理方法探讨[J]. 中国实用儿科杂志, 2013, 28(10): 725-730. Gong CX, Qin W. Discussion on the treatment of pediatric endocrinologists in patients with sexual developmental disorders[J]. Chinese Journal of Practical Pediatrics, 2013, 28(10): 725-730. |
| 17 |
Alhomaidah D, McGowan R, Ahmed SF. The current state of diagnostic genetics for conditions affecting sex development[J]. Clin Genet, 2017, 91(2): 157-162. DOI:10.1111/cge.12912. |
| 18 |
Wang Y, Gong C, Wang X, et al. AR mutations in 28 patients with androgen insensitivity syndrome (Prader grade 0-3)[J]. Sci China Life Sci, 2017, 60(7): 700-706. DOI:10.1007/s11427-017-9084-9. |
| 19 |
秦淼, 巩纯秀.特发性低促性腺激素性性腺功能减退症临床特点及突变分析KALl与FGFRl基因[J].中华儿科杂志, 2014, 52(12): 942-947.DOI: 10.3760/cma.j.issn.0578-1310.2014.12.014. Qin M, Gong C, Qi Z, et al.Children with idiopathic hypogonadotropic hypogonadism: clinical data analysis and mutations analysis of KAL1 and FGFR1 gene[J].Chin J Pediatr, 2014, 52(12): 942-947.DOI: 10.3760/cma.j.issn.0578-1310.2014.12.014. |
| 20 |
WangY, Gong C, Qin M, et al. Clinical and genetic features of 46 young male paediatric patients with congenital hypogonadotropic hypogonadism (CHH)[J]. Clin Endocrinol (Oxf), 2017, 1-10. DOI:10.1111/cen.13451. |
| 21 |
Massanyi EZ, Dicarlo HN, Migeon CJ, et al. Review and management of 46, XY disorders of sex development[J]. J Pediatr Urol, 2013, 9(3): 368-379. DOI:10.1016/j/jpurol.2012.12.002. |
 2019, Vol. 18
2019, Vol. 18


