神经母细胞瘤是小儿最常见的颅外实体肿瘤,是5岁以下儿童死亡的主要原因之一[1]。该病主要起源于胚胎期交感神经系统中的神经嵴祖细胞,发生部位较广,以肾上腺最为常见,其临床表现复杂多样,具有起病隐匿、恶性程度高、异质性高、转移早、易复发以及预后差等特点[2, 3]。尽管目前神经母细胞瘤的治疗方法有手术、高强度化疗、放疗、免疫治疗以及自体干细胞移植等,但高危组患儿的5年生存率仍低于50%[4, 5]。大多数患儿容易复发,预后不良,在国际神经母细胞瘤风险组分析中复发性转移性神经母细胞瘤5年生存率仅为8%[6]。单纯手术或者加大放、化疗的强度已经很难有效提高神经母细胞瘤的治疗效果。因此,根据神经母细胞瘤的分子生物学特性寻找更为有效的靶向干预方法,已成为神经母细胞瘤治疗领域的热点。G蛋白耦联受体-血管紧张素受体样蛋白J受体(putative receptor protein related to angiotensin receptor ATl, APJ)是由377个氨基酸组成的多肽,属于G蛋白偶联受体(G protein coupled receptor, GPCR),目前已知的APJ唯一的天然内源性配体是Apelin[7]。大量研究表明Apelin/APJ系统与肿瘤之间存在一定的相关性,这说明Apelin/APJ系统可能参与了肿瘤的发生、发展。Apelin/APJ系统被发现在多种恶性肿瘤中处于激活状态,其作用是促进肿瘤细胞增殖以及肿瘤血管生成[8-10]。神经母细胞瘤是严重威胁儿童健康的常见肿瘤之一,但其与Apelin/APJ系统的关系仍不清楚。本研究通过检测Apelin/APJ系统在小儿神经母细胞瘤组织中的表达,初步探讨其在该病发生发展过程中的作用。
材料与方法 一、标本来源标本取自2015年12月至2016年9月湖南省儿童医院普外科收治的Ⅳ期或Ⅳs期神经母细胞瘤患儿,原发部位均为肾上腺,肿块扩大切除后留取肿瘤组织及癌旁正常肾上腺组织,冻存于-80℃冰箱。所有病例经术后病理检查诊断为小儿神经母细胞瘤,术前均未接受放疗或化疗。其中男童6例,女童4例;年龄最小者8个月,年龄最大者5岁6个月。所有标本收取前均已签署知情同意书。
二、免疫组织化学法检测神经母细胞瘤中Apelin及APJ表达所有标本经过固定,石蜡包埋,4 μm连续切片,常规进行免疫组化染色SP法。Apelin(ab59469)及APJ抗体(ab214369)购自Abcam公司,生物素标记的二抗及SP免疫组化染色试剂盒均购自武汉博士德生物工程有限公司。以磷酸缓冲液(PBS)代替一抗作为阴性对照,同时设空白对照,以证实高表达的组织切片作为阳性对照,着色为淡黄色、棕黄色或褐色的细胞为阳性。采用Image Pro-Plus (Media Cybernetics Inc, USA)图像分析软件进行图像分析。
三、Real-time PCR检测组织中Apelin及APJ的mRNA表达组织标本经液氮研磨成粉末后,根据说明书采用Trizol法提取组织总RNA,利用逆转录试剂盒(Invitrogen公司)将RNA逆转录成cDNA,并以cDNA为模板,进行real-time PCR检测。Apelin引物(F:CTGCTCTGGCTCTCCTTGAC; R:GAATTTCCTCCGACCTCCCTG-3),APJ引物(F:CACCTGGTGAAGACGCTGTA; R:TAGGGGATGGAnTrCTCGTG)均由上海博尚生物有限公司合成。反应体系:模板cDNA 2 μL,2×SYBR Premix Ex TaqTM Ⅱ(购自宝生物公司) 10 μL,上、下游引物各0.8 μL,ddH2O 6.4 μL。反应条件:95 ℃预变性5 min;95 ℃变性15 s,60 ℃退火延伸30 s,40个循环。采用2-ΔΔCt分析法计算mRNA的相对表达量。
四、蛋白质提取和蛋白质印迹分析组织标本研磨成粉末后,立即加入组织裂解液(50 mmoL/L Tris-Cl、1 mmoL/L EDTA、2 % SDS、5 mmoL/L DTT、10 mmoL/L PMSF),冰上裂解30 min,超声粉碎,4 ℃,13 000 g离心去除细胞碎片,收集上清液,用BCA方法测定蛋白质浓度。100 V恒压SDS-PAGE蛋白电泳,每孔上样量约50 μg,电泳结束后200 mA恒流电转移至硝酸纤维素膜,5%脱脂奶粉在室温下封闭1~2 h,加入单抗,4℃孵育过夜,TBST洗膜后加入Ig-HRP标记的二抗室温孵育1 h,ECL化学发光法检测。以β-Actin蛋白作为内参,通过Image J图像分析软件统计分析蛋白条带结果。其中Apelin(ab59469)及APJ抗体(ab214369)购自Abcam公司,BCA蛋白质测定试剂、化学发光试剂购自Piercer Chemical Co.Rockford公司。硝酸纤维素膜、蛋白质Marker、丙烯酰胺等购自Sigma公司。
五、人Apelin-36 ELISA检测同期收集NB患儿及健康儿童血浆,1 000 g离心30 min去除颗粒。根据ELISA检测试剂盒说明进行操作,主要为加入稀释后的标准品及待测样品50 μL于反应孔内,立即加入50 μL生物素标记的抗体,37℃温育1 h,震荡洗涤,每孔加入80 μL亲和链酶素-HRP,37℃温育30 min。震荡洗涤,每孔加入底物A、B各50 μL,轻轻震荡混匀,37℃避光孵育10 min。取出酶标板,迅速加入50 μL终止液,在450 nm波长处测定各孔的OD值。人Apelin-36 ELISA检测试剂盒(RAB0018)购自sigma公司。
六、统计学处理采用SPSS 17.0软件进行统计学分析,计量数据采用均数±标准差(x±s)表示,两组间比较采用t检验,以P < 0.05为差异有统计学意义。
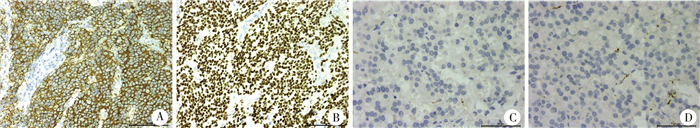
结 果 一、Apelin/APJ蛋白在神经母细胞瘤中的表达情况免疫组化结果显示Apelin蛋白主要定位于神经母细胞瘤的细胞浆,呈强阳性表达,而APJ蛋白则主要在肿瘤胞核内,呈棕黄色颗粒,强阳性或中等阳性表达,两者均在癌旁肾上腺组织中呈阴性或者弱阳性表达,见图 1。
|
Download:
|
| 图 1 免疫组化检测神经母细胞瘤组织中Apelin及APJ的表达 注 A:Apelin蛋白在肿瘤细胞浆内呈强阳性表达(IHC×200);B:APJ蛋白在肿瘤细胞核内呈强阳性表达(IHC×200);C:Apelin蛋白在癌旁肾上腺组织中呈阴性表达(IHC×400);D:APJ蛋白在癌旁肾上腺组织中呈阴性表达(IHC×400) Fig. 1 Expressions of Apelin and APJ in neuroblastoma and adjacent adrenal tissues | |
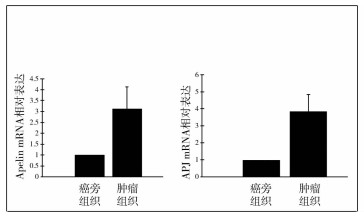
qRT-PCR结果显示,与癌旁肾上腺组织相比,小儿神经母细胞瘤组织中的Apelin及APJ的mRNA表达水平显著升高(t=10.94,P < 0.05;t=7.83,P < 0.05),见图 2。
|
Download:
|
| 图 2 神经母细胞瘤和瘤旁肾上腺组织中Apelin和APJ mRNA的表达水平(x±SD, n=10) Fig. 2 mRNA of Apelin and APJ were detected in neuroblastoma and adjacent adrenal tissues(x±SD, n=10) | |
利用Western blot对神经母细胞瘤中Apelin及APJ蛋白的表达水平进行检测,结果显示在小儿神经母细胞瘤组织中Apelin及APJ蛋白的表达水平均显著高于癌旁组织(t=11.30,P < 0.05;t=12.36,P < 0.05),见图 3。

|
Download:
|
| 图 3 神经母细胞瘤和瘤旁组织中Apelin和APJ蛋白的表达水平(x±SD, n=10) Fig. 3 Expressions of Apelin and APJ were detected by Western blot in neuroblastoma and adjacent adrenal tissues(x±SD, n=10) | |
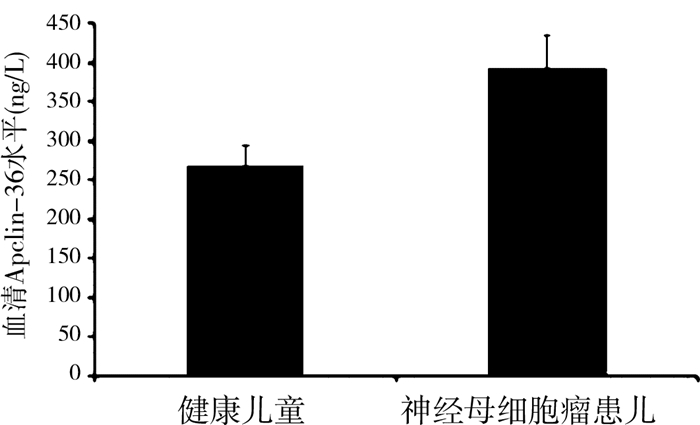
同期收集10例神经母细胞瘤患儿的血液样本,对照组健康儿童血液样本来自湖南省儿童医院健康体检的儿童。由于Apelin-36是Apelin的成熟形式,常用其水平的高低来反映体内整个Apelin的水平,采用ELISA法检测了血浆中Apelin-36的水平。结果显示神经母细胞瘤患儿血浆Apelin-36的水平显著高于健康儿童对照组的水平(t=7.12,P < 0.05),见图 4。
|
Download:
|
| 图 4 神经母细胞瘤患儿和健康儿童血浆Apelin-36的水平(x±SD, n=10) Fig. 4 Expression of plasma Apelin-36 in neuroblastoma children and healthy controls(x±SD, n=10) | |
神经母细胞瘤是严重威胁儿童健康的恶性肿瘤,该病起病隐匿,恶性程度高,转移早,易复发,预后差。由于NB具有较高的异质性,患儿的临床表现差异很大,小部分患儿可表现出良性转归甚至自然消退,而更多的则是呈恶性进展,预后不良,严重危害着儿童的身心健康。到目前为止,NB的发病机制尚未完全阐明,虽然针对NB的治疗手段较多,但其临床治疗效果并不理想。国际上NB患儿的治疗以其危险度分层为依据,推行个体化治疗,远期生存率有一定的提高,但仍不满意。正因为如此,探讨NB的发病机制对提高NB的早期确诊率和治疗效果具有重大的意义,是临床、科研工作者面临的极具挑战性课题。
APJ受体属于人类的G蛋白偶联受体(G protein-coupled receptor, GPCR)家族成员,含有7个α螺旋跨膜结构域,Apelin蛋白目前已知的APJ的唯一内源性配体。Apelin来源于内源性前原蛋白的C端,内源性前原蛋白酶解能够产生Apelin-12、Apelin-13、Apelin-17和Apelin-36。随着其配体的发现,Apelin/APJ系统的位置和功能越来越清楚[11, 12]。研究表明,该系统在肺、肾、肾上腺、大脑、脾脏、胎盘等正常组织中也有表达,具有调节血压、介导神经内分泌应激反应、促进单核细胞粘附于人脐静脉内皮细胞、诱导正性肌力作用以及抑制胶原和凝血酶诱导的血小板聚集等重要生理功能。Apelin/APJ系统与多种疾病有关,包括心脏病、糖尿病、慢性肾脏疾病、肝脏疾病、肥胖症和癌症,大量研究表明Apelin/APJ系统可作为这些疾病的潜在治疗靶点[13-16]。研究发现,Apelin在1/3以上的人类肿瘤中表达上调,且其含量与肿瘤的分期和转移密切相关[17]。除此以外,越来越多的研究表明Apelin/APJ系统参与包括肺癌、胃肠道肿瘤、乳腺癌、前列腺癌、口腔鳞癌和妇科肿瘤等多种肿瘤的发生和发展。
Apelin/APJ系统在成人血管壁中呈强阳性表达,在多种人类肿瘤中处于激活状态,促进肿瘤血管生成是该系统参与肿瘤形成的重要机制之一。Kalin等[18]发现Apelin/APJ信号传导对胚胎血管生成至关重要,在脑肿瘤如恶性神经胶质瘤的微血管增殖中显著上调,Aapelin/APJ可以刺激肿瘤血管的形成和功能成熟。体内实验发现Apelin过表达可以增强小鼠肿瘤组织的血管化及促进体内肿瘤生长[17]。Lacquaniti等[19]报道肿瘤患者的血清Apelin水平显著高于健康受试者的血清Apelin水平,并且随肿瘤分期进展(从Ⅱ期到Ⅳ期)逐渐增加。与既往研究一致,本研究显示与癌旁肾上腺组织相比,Apelin与APJ在小儿Ⅳ期或Ⅳs期NB组织中多为强阳性表达,且其mRNA及蛋白表达水平均明显高于癌旁组织,而患儿血浆Apelin-36的水平也相对高于健康儿童。虽本研究的样本数不多,因为短期内同时收集较多数量的癌组织和癌旁正常肾上腺组织存在难度。但是,本研究初步发现了Apelin/APJ系统在小儿NB中处于激活状态,并可能作为一个癌基因,参与小儿NB的发生发展,但其在小儿NB中的具体作用机制尚需进一步研究。
实体肿瘤的生长和转移很大程度上依赖于新生血管的生成,鉴于Apelin/APJ系统在肿瘤血管生成中的作用,该系统已被认定为新的抗癌治疗靶点。后期随着样本量的增加,Apelin/APJ与NB分期分危的关联以及其与预后的关系有待进一步研究证实。针对Apelin/APJ系统的分子靶向治疗有望成为NB治疗的新策略。
| 1 |
Moreno L, Caron, Geoerger B, et al. Accelerating drug development for neuroblastoma-New Drug Development Strategy:an Innovative Therapies for Children with Cancer, European Network for Cancer Research in Children and Adolescents and International Society of Paediatric Oncology Europe Neuroblastoma project[J]. Expert Opin Drug Discov, 2017, 12(8): 801-811. DOI:10.1080/17460441.2017.1340269. |
| 2 |
Schulte JH, Eggert A. Neuroblastoma[J]. Crit Rev Oncog, 2015, 20(3-4): 245-270. DOI:10.1615/CritRevOncog.2015014033. |
| 3 |
Tatekawa Y. Unusual differentiation to pheochromocytoma-like cells in an adrenal neuroblastoma after chemotherapy:a case report and literature review[J]. Fetal Pediatr Pathol, 2015, 34(5): 322-327. DOI:10.3109/15513815. |
| 4 |
Yu AL, Gilman AL, Ozkaynak MF, et al. Anti-GD2 antibody with GM-CSF, interleukin-2, and isotretinoin for neuroblastoma[J]. N Engl J Med, 2010, 363(14): 1324-1334. DOI:10.1056/NEJMoa0911123. |
| 5 |
Valteau-Couanet D, Le Deley MC, Bergeron C, et al. Long-term results of the combination of the N7 induction chemotherapy and the busulfan-melphalan high dose chemotherapy[J]. Pediatr Blood Cancer, 2014, 61(6): 977-981. DOI:10.1002/pbc.24713. |
| 6 |
London WB, Castel V, Monclair T, et al. Clinical and biologic features predictive of survival after relapse of neuroblastoma:a report from the International Neuroblastoma Risk Group project[J]. J Clin Oncol, 2011, 29(24): 3286-3292. DOI:10.1200/JCO.2010.34.3392. |
| 7 |
Tatemoto K, Hosoya M, Habata Y, et al. Isolation and characterization of a novel endogenous peptide ligand for the human APJ receptor[J]. Biochem Biophys Res Commun, 1998, 251(2): 471-476. DOI:10.1006/bbrc.1998.9489. |
| 8 |
Lacquaniti A, Altavilla G, Picone A, et al. Apelin beyond kidney failure and hyponatremia:a useful biomarker for cancer disease progression evaluation[J]. Clin Exp Med, 2015, 15(1): 97-105. DOI:10.1007/s10238-014-0272-y. |
| 9 |
Yang L, Su T, Lv D, et al. ERK1/2 mediates lung adenocarcinoma cell proliferation and autophagy induced by apelin-13[J]. Acta Biochim Biophys Sin (Shanghai), 2014, 46(2): 100-111. DOI:10.1093/abbs/gmt140. |
| 10 |
Lv D, Li H, Chen L. Apelin and APJ, a novel critical factor and therapeutic target for atherosclerosis[J]. Acta Biochim Biophys Sin (Shanghai), 2013, 45(7): 527-533. DOI:10.1093/abbs/gmt040. |
| 11 |
Domazet I, Holleran BJ, Richard A, et al. Characterization of Angiotensin Ⅱ Molecular Determinants Involved in AT1 Receptor Functional Selectivity[J]. Mol Pharmacol, 2015, 87(6): 982-995. DOI:10.1124/mol.114.097337. |
| 12 |
Machura E, Ziora K, Ziora D, et al. Serum apelin-12 level is elevated in schoolchildren with atopic asthma[J]. Respir Med, 2013, 107(2): 196-201. DOI:10.1016/j.rmed.2012.10.026. |
| 13 |
Luo X, Liu J, Zhou H, et al. Apelin/APJ system:A critical regulator of vascular smooth muscle cell[J]. J Cell Physiol, 2018, 233(7): 5180-5188. DOI:10.1002/jcp.26339. |
| 14 |
Huang Z, Wu L, Chen L. Apelin/APJ system:A novel potential therapy target for kidney disease[J]. J Cell Physiol, 2018, 233(5): 3892-3900. DOI:10.1002/jcp.26144. |
| 15 |
Lv SY, Cui B, Chen WD, et al. Apelin/APJ system:A key therapeutic target for liver disease[J]. Oncotarget, 2017, 8(67): 112145-112151. DOI:10.18632/oncotarget.22841. |
| 16 |
Wu L, Chen L, Li L. Apelin/APJ system:A novel promising therapy target for pathological angiogenesis[J]. Clin Chim Acta, 2017, 466: 78-84. DOI:10.1016/j.cca.2016.12.023. |
| 17 |
Sorli SC, Le Gonidec S, Knibiehler B, et al. Apelin is a potent activator of tumour neoangiogenesis[J]. Oncogene, 2007, 26(55): 7692-7699. DOI:10.1038/sj.onc.1210573. |
| 18 |
Kälin RE, Kretz MP, Meyer AM, et al. Paracrine and autocrine mechanisms of apelin signaling govern embryonic and tumor angiogenesis[J]. Dev Biol, 2007, 305(2): 599-614. DOI:10.1016/j.ydbio.2007.03.004. |
| 19 |
Lacquaniti A, Altavilla G, Picone A, et al. Apelin beyond kidney failure and hyponatremia:a useful biomarker for cancer disease progression evaluation[J]. Clin Exp Med, 2015, 15(1): 97-105. DOI:10.1007/s10238-014-0272-y. |
 2019, Vol. 18
2019, Vol. 18


