新生儿胃穿孔(neonatal gastric perforation, NGP)是一种罕见病,多发生于5日龄内的新生儿,病死率较高[1, 2]。虽然一些风险因素(如早产、鼻导管吸氧、胃部解剖异常等)与NGP的发生发展及预后存在相关性,但目前NGP的发病原因尚不完全清楚[3, 4]。该病的首发症状以腹部表现为主,可迅速发展为休克[5]。因此,NGP的早期鉴别和及时处理对降低该病的病死率有重要意义。本研究旨在分析NGP患儿的发病原因及疾病特征,并探讨手术干预效果及预后状况,为NGP的治疗干预提供参考依据。
材料与方法 一、临床资料以2010年9月至2016年12月上海交通大学附属儿童医院普外科和新生儿科收治并行手术治疗的13例NGP患儿为研究对象。其中男7例(53.85%),女6例(46.15%);出生胎龄30~40周,平均胎龄(34.77±3.30)周;足月儿4例(30.77%),早产儿9例(69.23%);出生时体重(2316.92±618.54)g;低出生体重7例(53.85%),正常出生体重6例(46.15%)。研究正式开展前均获患儿监护人的知情同意及医院医学伦理委员会批准。收集患儿性别、胎龄、入院日龄、出生体重、首发症状、相关检查结果、入院时血清pH值、是否吸氧、是否留置胃管、出现症状到手术的时间、穿孔位置、穿孔长度、手术方式、合并消化道畸形、病理及预后等临床资料进行分析。
二、手术方案13例胃壁修补术患儿术前均留置胃管,其中11例经鼻导管吸氧,均予禁食、补液、抗感染、营养支持等治疗。13例手术均取左上腹横切口,进入腹腔后探查全腹部,吸尽腹腔内渗液及胃内容物后均发现胃壁不同位置穿孔。切除穿孔边缘处坏死组织至正常胃壁,间断缝合修补胃壁,并适当游离网膜组织以覆盖吻合口,检查无吻合口漏后用温生理盐水反复冲洗腹腔,腹腔小网膜囊内留置负压引流管,置胃管于胃内适当位置,关闭腹腔。术中均同时探查远端肠管,仅1例合并膈疝,术中同时行膈疝修补术,其余12例均成功实施一期胃壁修补术。
结 果 一、基本情况13例患儿术前X线片均提示大量气腹。首发症状为腹胀者8例,气促、呼吸困难者4例,胃出血者1例。术前血气分析提示酸中毒(pH<7.35)8例(61.54%),发病日龄为(2.46±1.51)d,发病至手术的间隔时间为(21.54±28.57)h,其中出现症状到手术的时间隔<24 h者11例,≥24 h者2例。4例术后出现并发症,1例首次胃壁修补术时未探及合并十二指肠膈膜,于第一次手术后3周行十二指肠探查,并行膈膜切除术及肠吻合术;2例双胞胎兄弟术后均因出现二次吻合口漏及行多次胃穿孔修补术,且均于末次手术中同时行胃造瘘术(蕈状引流管自胃内引至腹壁外)及空肠营养管置入术,术后恢复后均行上消化道GI造影确定无幽门及其他上消化道梗阻,再依次拔除胃造瘘蕈状管、空肠营养管;1例患儿入院后因乳糜胸行床旁双侧胸腔闭式引流,后行胃前壁修补术,术后4 d因胃内胃管导致医源性胃后壁穿孔,再次行胃壁修补术,术后出现心力衰竭、呼吸衰竭等, 家属放弃治疗,于二次手术后3周死亡。
二、病理及预后13例(100%)NGP患儿术中均发现胃壁穿孔,与术前X线片气腹诊断结果相符。2例(15.38%)合并其他消化道畸形,其中1例为膈疝; 1例为十二指肠膈膜(于第2次手术过程中发现)。穿孔部位:胃大弯(图 1)5例,胃前壁3例,胃后壁2例,胃小弯2例; 同时位于胃前壁和胃后壁1例(胃后壁穿孔为医源性);穿孔长度<2 cm者2例(15.38%),2~5 cm(不含5 cm)者6例(46.15%),≥5 cm者5例(38.46%)。84.61%的患儿于发病后24 h内行手术治疗,13例均行一期胃壁修补术;5例(38.46%)患儿术后出现并发症(包括伤口感染1例、吻合口漏合并伤口感染2例、医源性胃穿孔1例,十二指肠梗阻1例)。术后出现胃壁肌层缺损9例,胃壁肌层发育不良1例,胃壁缺血坏死3例。13例NGP患儿的临床资料见表 1。
|
Download:
|
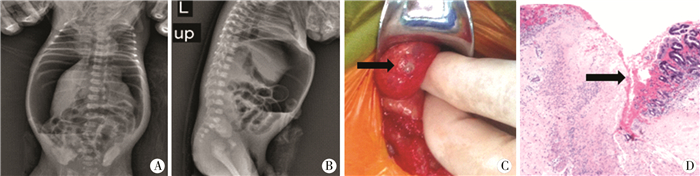
| 图 1 1例穿孔部位位于胃大弯的患儿 A、B图均为腹部X线立位片,提示腹腔内大量游离气体; C图箭头所指处为胃前壁穿孔;D图为HE染色高倍镜下100倍视野,箭头所指为胃壁肌层断裂。 Fig. 1 1 case of perforation in the stomarch A, B:Radiographic examination showed large amounts of free air within abdomen; C:Perforation of gastric wall; D:H& E staining (100×magnification) showed a rupture of musculature defect of gastric wall. | |
|
|
表 1 13例NGP患儿的临床资料 Table 1 Clinical profiles of 13 NGP patients |
术后存活12例,死亡1例。死亡患儿为早产低出生体重儿,伴呼吸性酸中毒、胸腔积液、低蛋白血症,且患儿出现症状至手术时间过长(4 d),首次手术后因医源性胃管损伤致胃后壁出现新发穿孔,行二次修补术,手术后出现感染性休克、败血症,家属放弃抢救最终导致患儿死亡。其余12例存活患儿随访1~6年,其生长发育正常,预后良好。
讨 论 一、临床表现新生儿胃穿孔早期临床表现多为呕吐、少哭少动、拒奶,典型体征为呼吸急促、进行性腹胀、腹膜炎体征、肠鸣音减弱甚至消失;晚期表现较危重(包括中毒性休克、呼吸衰竭等)[1, 6-7]。本组病例术前腹部X线检查结果均提示气腹。因此,术前腹部X线检查是该病重要的诊断方法,可疑征象包括大量气腹、液气腹、胃泡消失等。如新生儿(尤其是早产儿)、低出生体重儿生后数日出现气促、精神反应差、呕吐、不明原因的严重腹胀、胃内出血等,同时X线检查提示大量气腹,需警惕胃穿孔发生的可能性。
二、NGP发生发展的病理机制自1941年国外学者Herbut首次发现先天性胃壁结构缺失可能会导致胃穿孔以来,国内外针对NGP的病因学开展了多方面研究[8]。据报道,胃酸生成过多、压力性溃疡、腹部创伤、胃壁缺血后坏死等因素均可引发NGP[9, 10]。有学者发现,NGP患儿中早产儿的比例较高[11, 12]。其发生机制主要包括:先天性胃壁肌层发育不良或缺损、胃壁缺血后坏死、胃远端梗阻及医源性伤害等[13]。另有学者认为感染、急性胃扩张、消化性溃疡等因素亦可引起胃穿孔。新生儿胃穿孔的病因通常并不单一,本研究纳入的NGP患儿中术后胃壁肌层缺损者达9例,由此可推测胃壁肌层缺损是其主要病因,当喂奶、哭吵或呕吐时,患儿胃内压升高,可引起肌层缺损裂隙处破裂或穿孔。2例双胞胎病例均诊断为缺血坏死,猜测可能与孕期中存在双胎输血综合征致胃壁血供受影响有关。2例合并胃远端梗阻(膈疝、十二指肠膈膜)病例,远端梗阻致近端肠管、胃扩张,胃内压升高,致使胃壁肌层撕裂或分离,最终导致黏膜坏死而发生穿孔。因此,术中有必要探查患儿是否合并其他消化道畸形,并解除胃远端梗阻。另外1例因胃管机械力作用导致术后其他部位胃壁发生穿孔,故医源性损伤同样应引起重视。
三、治疗方法新生儿胃穿孔的主流治疗方法为手术去除坏死组织,同期行可靠的胃壁肌层修补。而对于多次吻合口漏的病例,建议根据术中情况酌情行胃造瘘术,可有效降低胃内压力,配合放置空肠营养管及术后早期肠内营养等措施,可在一定程度上提高患儿生存率[14]。本研究中2例双胞胎患儿均采用该方法进行治疗,随访至今2例患儿生长发育均正常。
由于胃穿孔后短时间内即可出现气腹,可致患儿心肺功能受损,随着病情发展,毒素吸收,全身情况迅速恶化,导致愈后不良。因此,本研究中,出现临床症状至手术时间间隔大于24 h者预后较差,可能与早产、毒素吸收、感染性休克、呼吸及多脏器功能衰竭等因素有关,致使该病的病死率可达45% ~58%[15]。因此,术前纠正新生儿呼吸性酸中毒、积极控制感染、确诊后尽早手术尤其重要;同时配合术后监护及综合治疗,可改善新生儿胃穿孔的预后。
| 1 |
卢朝祥, 谢卫科, 王琪, 等. 82例新生儿消化道穿孔诊治分析[J]. 临床小儿外科杂志, 2016, 15(2): 193-195, 201. DOI:10.3969/j.issn.1671-6353.2016.02.025. Lu ZX, Xie WK, Wang Q, et al. Clinical analysis of diagnosis and treatment in neonatal gastrointestinal perforation[J]. Clinical Pediatric Surgery, 2016, 15(2): 193-195, 201. DOI:10.3969/j.issn.1671-6353.2016.02.025. |
| 2 |
St-Vil D, LeBouthillier G, Luks FI, et al. Neonatal gastrointestinal perforations[J]. J Pediatr Surg, 1992, 27(10): 1340-1342. DOI:10.10.16/0022-3468(92)90292-f. |
| 3 |
Byun J, Kim HY, Noh SY, et al. Neonatal gastric perforation: A single center experience[J]. World J Gastrointest Surg, 2014, 6(8): 151-155. DOI:10.4240/wjgs.v6.i8.151. |
| 4 |
Antabak A, Bogović M, Vuković J, et al. Postoperative gastric perforation in a newborn with duodenal atresia[J]. J Neonatal Surg, 2016, 5(4): 62. DOI:10.21699/jns.v5i4.469. |
| 5 |
Gupta G, Kumar S, Gupta S, et al. Neonatal gastric perforations: are they really spontaneous?[J]. Indian J Surg, 2014, 76(4): 319-320. DOI:10.1007/s12262-013-0980-7. |
| 6 |
Saraç M, Bakal Ü, Aydın M, et al. Neonatal gastrointestinal perforations: the 10-year experience of a reference hospital[J]. Indian J Surg, 2017, 79(5): 431-436. DOI:10.1007/s12262-016-1565-z. |
| 7 |
Reyna-Sepulveda F. Neonatal sleeve gastrectomy for multiple gastric perforations: a case report[J]. J Neonatal Surg, 2017, 6(1): 10. DOI:10.21699/jns.v5i3.355. |
| 8 |
Herbut PA. Congenital defect in musculature of stomach with rupture in newborn infant[J]. Arch Pathol, 1943, 36: 91. |
| 9 |
Touloukian RJ, Posch JN, Spencer R. The pathogenesis of ischemic gastroenterocolitis of the neonate: selective gut mucosal ischemia in asphyxiated neonatal piglets[J]. J Pediatr Surg, 1972, 7(2): 194-205. DOI:10.1016/0022-3468(72)90496-4. |
| 10 |
Ohshiro K, Yamataka A, Kobayashi H, et al. Idiopathic gastric perforation in neonates and abnormal distribution of intestinal pacemaker cells[J]. J Pediatr Surg, 2000, 35(5): 673-676. DOI:10.1053/jpsu.2000.5940. |
| 11 |
Terui K, Iwai J, Yamada S, et al. Etiology of neonatal gastric perforation: a review of 20 years' experience[J]. Pediatr Surg Int, 2012, 28(1): 9-14. DOI:10.1007/s00383-011-3003-4. |
| 12 |
Sato M, Hamada Y, Kohno M, et al. Neonatal gastrointestinal perforation in Japan: a nationwide survey[J]. Pediatr Surg Int, 2017, 33(1): 33-41. DOI:10.1007/s00383-016-3985-z. |
| 13 |
Yang CY, Lien R, Fu RH, et al. Prognostic factors and concomitant anomalies in neonatal gastric perforation[J]. J Pediatr Surg, 2015, 50(8): 1278-1282. DOI:10.1016/j.jpedsurg.2015.04.007. |
| 14 |
Aydin M, Deveci U, Taskin E, et al. Percutaneous peritoneal drainage in isolated neonatal gastric perforation[J]. World J Gastroenterol, 2015, 21(45): 12987-12988. DOI:10.3748/wjg.v21.i45.12987. |
| 15 |
Kshirsagar AY, Vasisth GO, Ahire MD, et al. Acute spontaneous gastric perforation in neonates: a report of three cases[J]. Afr J Paediatr Surg, 2011, 8(1): 79-81. DOI:10.4103/0189-6725.78935. |
 2018, Vol. 17
2018, Vol. 17


