嵌顿性腹股沟斜疝是小儿外科常见的腹部急症,发病率约为17%,常见于1岁以下的婴幼儿,其特征为不能还纳至腹腔的腹股沟包块[1-2]。任何腹腔内器官和组织均可嵌顿于疝囊内,小肠为常见的嵌顿物,患儿常有哭闹、腹痛、呕吐等急腹症表现,临床上易于判断识别[3]。相比于男性患儿,女性嵌顿疝内容物多为卵巢,其症状与体征均不典型,尤其婴幼儿会阴部脂肪层较厚,腹股沟包块容易被家长忽视,导致最佳诊疗时机被延误,最终发展为嵌顿卵巢缺血坏死,影响患儿未来的生育能力[4-5]。本研究旨在探讨女性婴幼儿腹股沟嵌顿疝发生卵巢绞窄坏死的相关因素。
材料与方法 一、临床资料回顾性分析中国医科大学附属深圳市儿童医院普外二科2014年2月至2020年12月诊断为腹股沟嵌顿疝并行急诊手术治疗的79例女性婴幼儿临床资料,嵌顿内容物为卵巢(或包含卵巢)。纳入标准:①术后诊断为卵巢滑动疝;②疝内容物为卵巢或包含卵巢;③年龄<3岁;④临床资料完整,签署知情同意书。排除标准:①仅行手法复位或择期手术;②嵌顿物为肠管、大网膜等其他器官及组织等;③合并其他先天性疾病如两性畸形者。79例患儿就诊时年龄19~938 d,中位年龄94 d,嵌顿侧别为左侧55例,右侧24例;嵌顿时间2.5~338 h,中位嵌顿时间26.5 h。有肠管嵌顿史3例,均行嵌顿疝手法复位。患儿均行腹腔镜下腹股沟嵌顿疝修补术,均术中证实嵌顿内容物为卵巢或包含卵巢,其中19例因卵巢绞窄坏死行卵巢切除术,术后病理证实为坏死卵巢组织。本研究经中国医科大学附属深圳市儿童医院伦理委员会审批。
二、研究方法根据术中探查所见将患儿分为卵巢绞窄坏死组(19例)与卵巢未坏死组(60例),收集两组患儿临床资料,包括:①年龄、体重、出生体重、嵌顿史、手法复位史及母亲孕产史;②发病至手术的时间、手术方式、住院时长以及是否伴有发热、呕吐、腹胀等临床表现,体查是否发现腹股沟区红肿;③血常规、白细胞计数、腹股沟超声卵巢血流信号及卵巢体积,卵巢体积采用椭球体计算公式:V=0.523×长(cm)×宽(cm)×高(cm);④嵌顿部位、嵌顿内容物及是否有卵巢及附件扭转等。
三、统计学处理使用SPSS 23.0进行统计学分析。服从正态分布的计量资料采用x±s进行描述,组间比较采用两独立样本t检验;不服从正态分布的计量资料采用M(Q1,Q3)进行描述;组间比较采用秩和检验;计数资料采用频数和率进行描述,组间比较采用χ2检验;采用Logistic回归分析筛选女性婴幼儿腹股沟嵌顿疝致卵巢坏死的相关因素,并绘制相关因素的ROC曲线;P<0.05为差异有统计学意义。
结果 一、两组患儿各项临床指标比较两组患儿年龄、早产儿及低体重儿占比、嵌顿侧别、有无嵌顿史、发病至手术时长、临床表现(哭闹、发热、呕吐)、术中发现多器官嵌顿所占比例等情况比较,差异均无统计学意义(P>0.05);而腹股沟红肿、白细胞计数、超声图像中卵巢血流信号、卵巢体积及术中发现卵巢扭转所占比例比较,差异具有统计学意义(P<0.05)。见表 1。
| 表 1 卵巢未坏死组与卵巢坏死组女性婴幼儿腹股沟嵌顿疝的相关因素分析 Table 1 Analysis of factors associated with non-necrotic and necrotic groups |
|
|
将单因素分析结果中有统计学意义的5个变量纳入二元Logistic回归模型进行多变量分析,结果显示,卵巢未坏死组与卵巢坏死组在卵巢体积、超声图像中卵巢血流信号及卵巢扭转情况上比较,差异有统计学意义(P<0.05),即卵巢未显示血流信号(OR=5.942)、卵巢扭转(OR=5.470)及卵巢体积增大(OR=8.065)影响卵巢坏死的危险因素。见表 2。
| 表 2 女性婴幼儿腹股沟嵌顿疝卵巢坏死相关因素的多因素分析结果 Table 2 Multivariate analysis of risk factors of ovarian necrosis in female infants with incarcerated inguinal hernia |
|
|
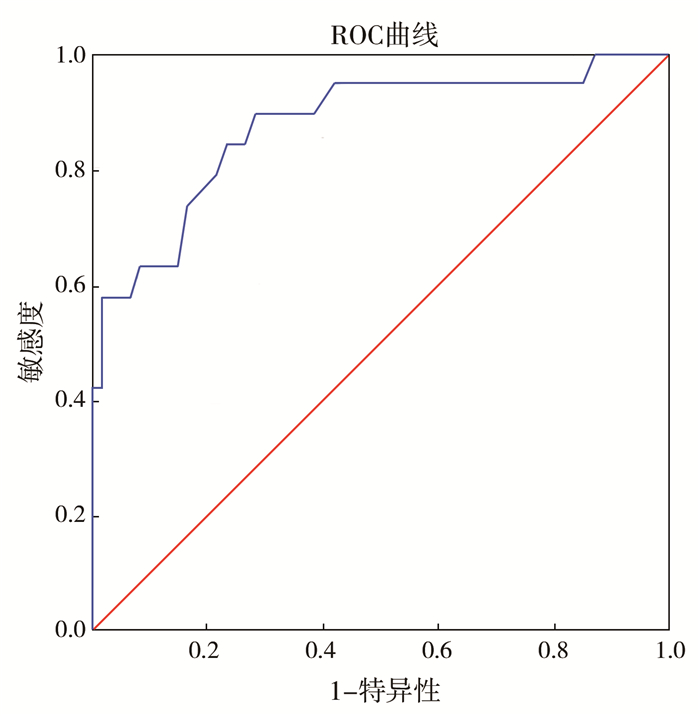
为进一步探究卵巢体积变化对卵巢绞窄坏死的影响,我们选择了多因素分析中OR值最大的相关因素(即卵巢体积),绘制了卵巢体积诊断卵巢绞窄坏死的ROC曲线。结果显示,卵巢体积≥2.02 cm3预测卵巢绞窄坏死的曲线下面积为0.874(95%CI:0.774~0.977, P<0.001),敏感度为89.5%,特异性为71.7%。见图 1。
|
图 1 通过卵巢体积诊断79例女性婴幼儿腹股沟嵌顿疝卵巢绞窄坏死的ROC曲线 Fig.1 ROC curve for strangulated ovarian necrosis as diagnosed by ovarian volume in 79 female neonates and toddlers with incarcerated inguinal hernia 注 接受者操作特性曲线(receiver operating characteristic curve,ROC) |
女性婴幼儿容易发生卵巢嵌顿的机制尚不明确,有学者认为与女性骨盆的椭圆形态和盆腔容积有关。年龄小的患儿盆腔容积相对较小,两侧子宫附件位置距离内环口较近,一旦卵巢经内环口突入狭窄的腹股沟管,自行还纳至腹腔将非常困难,发生绞窄坏死的风险随之增加[6-7]。若术中证实卵巢坏死并予切除,患儿将在一定程度上丧失生育能力。因此,有必要分析女性婴幼儿腹股沟嵌顿疝发生卵巢坏死的相关因素,以便及时有效处理。
股沟管卵巢嵌顿的女性患儿中仅有0.7%的患儿因卵巢缺血坏死而予以切除[8]。这种巨大差异可能是由于国内外学者在各自研究中对卵巢嵌顿的定义不同所造成。随着疝内容物嵌顿时间的延长,其血运障碍会进一步恶化,最终导致组织坏死。本研究结果显示,大部分卵巢坏死患儿发病至手术的时间<24 h,因此不能以嵌顿时间的长短作为判断卵巢坏死的依据。Kumar等[9]认为,低孕龄、低出生体重可能是造成卵巢绞窄坏死的潜在影响因素。有研究表明,卵巢绞窄的患儿通常会在腹股沟区出现局部红肿包块。本研究发现,卵巢绞窄坏死组中有8例(8/19,42.1%)患儿出现腹股沟区红肿包块;而卵巢未坏死组中,仅有9例(9/60, 15.0%)出现腹股沟区红肿包块。术中探查发现,卵巢未坏死组中的9例患儿卵巢肿胀、淤血明显,术后随访中2例出现卵巢较对侧不同程度发育迟缓,而卵巢轻度水肿的患儿无明显的腹股沟区红肿包块。
本研究结果显示,79例患儿中有19例(19/79,24.1%)发生卵巢绞窄坏死并接受卵巢切除术,与之前大部分研究中的发生率(2% ~33%)一致[7]。最近一项研究表明,血白细胞计数有助于识别卵巢扭转引起的炎症反应[10]。本研究发现,卵巢坏死组与未坏死组之间白细胞计数差异有统计学意义,卵巢坏死组中有12例(12/19, 63.2%)发生卵巢嵌顿坏死,且卵巢坏死组中卵巢扭转的发生率明显较卵巢未坏死组高(52.6%比10.0%)。因此,我们认为,嵌顿卵巢突入腹股沟管后其正常解剖位置发生改变,由于卵巢和输卵管原有的带蒂结构易使卵巢发生扭转,从而增加卵巢绞窄坏死的风险。本研究通过多因素分析证实,卵巢扭转是卵巢绞窄坏死的独立相关因素。白细胞计数升高可能是由于嵌顿卵巢扭转或绞窄坏死所致,也不排除患儿合并上呼吸道感染的可能,需进一步研究证实。
彩色多普勒超声是小儿腹股沟嵌顿疝最常用和最重要的辅助检查方法,不仅可分辨嵌顿物的性质,还可了解嵌顿物的血流分布情况,判断嵌顿组织活性[11]。有学者认为,彩色多普勒超声对卵巢血运评估的准确性受许多因素影响,如卵巢双重血供、儿童血管较细致灌注不足、卵巢位置较深等,因此其对卵巢血流的评估存在一定的局限性。在本研究多因素分析结果中,卵巢血流信号是卵巢绞窄坏死的一项重要因素。79例患儿中有28例术前超声未显示卵巢明显血流信号,尽管其诊断卵巢坏死的假阳性率偏高(9/69,13.0%),但彩色多普勒超声能够较为准确判断嵌顿物是否为卵巢,当提示卵巢血运情况欠佳时,可及早进行干预治疗。
最近Chen等[12]一项针对32例年龄小于1岁腹股沟卵巢嵌顿疝患儿的研究表明,卵巢体积、是否合并多发性囊肿及卵巢扭转角度是卵巢绞窄坏死的重要相关因素。本研究中没有合并卵巢囊肿的病例,与之前文献报道一致的是,本研究结果显示卵巢坏死组卵巢体积明显大于非卵巢坏死组,多因素分析结果表明,卵巢体积是影响卵巢绞窄坏死的独立相关因素。进一步对卵巢体积进行ROC曲线分析显示,卵巢体积≥2.02 cm3时需警惕卵巢绞窄坏死。一项评估各阶段儿童正常卵巢体积的研究表明,婴幼儿平均卵巢体积为1.05~1.06 cm3[13]。卵巢体积增大可能与卵巢扭转后血供及淋巴回流受阻有关,因此当发现卵巢体积增大时,临床医生应警惕卵巢扭转,予及时诊治以避免卵巢绞窄坏死。
综上所述,腹股沟嵌顿疝作为女性婴幼儿常见的外科急症之一,内容物为不包含肠管的单纯卵巢嵌顿时临床表现多不典型,腹股沟出现红肿包块可能预示预后不良。超声检查为首选的影像学诊断方法,卵巢体积增大、无明显血流信号是卵巢坏死的相关因素;卵巢体积≥2.02 cm3时,应高度警惕卵巢发生坏死的可能性。
利益冲突 所有作者均声明不存在利益冲突
作者贡献声明 文献检索为王子涵, 论文调查设计为王子涵、罗玉、王斌,数据收集与分析王子涵、刘冬、罗玉、廖亚娟、张曦耘,论文结果撰写为王子涵,论文讨论分析为王子涵
| [1] |
马明第, 李昭铸, 张泽楠, 等. 小儿腹股沟嵌顿疝合并石骨症1例并文献复习[J]. 临床小儿外科杂志, 2020, 19(3): 282-284. Ma MD, Li ZZ, Zhang ZN, et al. Inguinal incarcerated hernia with osteopetrosis in children: a case report with a literature review[J]. J Clin Ped Sur, 2020, 19(3): 282-284. DOI:10.3969/j.issn.1671-6353.2020.03.018 |
| [2] |
Chang SJ, Chen JYC, Hsu CK, et al. The incidence of inguinal hernia and associated risk factors of incarceration in pediatric inguinal hernia: A nationwide longitudinal population-based study[J]. Hernia, 2016, 20(4): 559-563. DOI:10.1007/s10029-015-1450-x |
| [3] |
张翔, 张宏伟, 殷易钰, 等. 两种手术方法治疗婴幼儿腹股沟嵌顿疝肠坏死临床比较[J]. 临床小儿外科杂志, 2016, 15(6): 598-601. Zhang X, Zhang HW, Yin YJ, et al. Two surgical approaches for intestinal necrosis of incarcerated inguinal hernia in infants: a report of 71 cases[J]. J Clin Ped Sur, 2016, 15(6): 598-601. DOI:10.3969/j.issn.1671-6353.2016.06.020 |
| [4] |
Boley SJ, Cahn D, Lauer T, et al. The irreducible ovary: a true emergency[J]. J Pediatr Surg, 1991, 26(9): 1035-1038. DOI:10.1016/0022-3468(91)90668-j |
| [5] |
Cam C, Celik C, Sancak A, et al. Inguinal herniorrhaphy in childhood may result in tubal damage and future infertility[J]. Arch Gynecol Obstet, 2009, 279(2): 175-176. DOI:10.1007/s00404-008-0654-z |
| [6] |
张雪琴. 女性婴幼儿嵌顿性腹股沟斜疝致附件坏死的诊治分析[J]. 中华临床医师杂志(电子版), 2019, 13(12): 914-917. Zhang XQ. Diagnosis and treatment of accessory necrosis caused by incarcerated inguinal hernia in female infants[J]. Chinese Journal of Clinicians (Electronic Edition), 2019, 13(12): 914-917. DOI:10.3877/cma.j.issn.1674-0785.2019.12.008 |
| [7] |
Bronsther B, Abrams MW, Elboim C. Inguinal hernias in children: a study of 1, 000 cases and a review of the literature[J]. J Am Med Womens Assoc, 1972, 27(10): 522-525. |
| [8] |
Dolgin S. Inguinal hernia in girls: A retrospective analysis of over 1000 patients[J]. J Pediatr Surg, 2021, 56(1): 203. DOI:10.1016/j.jpedsurg.2020.08.028 |
| [9] |
Kumar VH, Clive J, Rosenkrantz TS, et al. Inguinal hernia in preterm infants (< or=32-week gestation)[J]. Pediatr Surg Int, 2002, 18(2-3): 147-152. DOI:10.1007/s003830100631 |
| [10] |
Nissen M, Sander V, Rogge P, et al. Neutrophil to lymphocyte ratio and platelet to lymphocyte ratio might predict pediatric ovarian torsion: a single-institution experience and review of the literature[J]. J Pediatr Adolesc Gynecol, 2021, 34(3): 334-340. DOI:10.1016/j.jpag.2020.12.003 |
| [11] |
Fleischer AC, Brader KR. Sonographic depiction of ovarian vascularity and flow: current improvements and future applications[J]. J Ultrasound Med, 2001, 20(3): 241-250. DOI:10.7863/jum.2001.20.3.241 |
| [12] |
Chen Y, Peng XZ, Lu W, et al. Risk factors for strangulated ovarian hernia in female infants: the role of ovarian volume[J]. Curr Med Sci, 2018, 38(6): 1032-1037. DOI:10.1007/s11596-018-1980-4 |
| [13] |
Garel L, Dubois J, Grignon A, et al. US of the pediatric female pelvis: a clinical perspective[J]. Radiographics, 2001, 21(6): 1393-407. DOI:10.1148/radiographics.21.6.g01nv041393 |
 2022, Vol. 21
2022, Vol. 21


